TẠP CHÍ Y HỌC VIỆT NAM TẬP 488 - THÁNG 3 - SỐ 2 - 2020
193
TÀI LIỆU THAM KHẢO
1. Ferretti A., Monaco E., Giannetti S. và cộng
sự. (2011). A medium to long-term follow-up of
ACL reconstruction using double gracilis and
semitendinosus grafts. Knee Surg Sports Traumatol
Arthrosc, 19(3), 473–478.
2. Webster K.E., Feller J.A., Hartnett N. và cộng
sự. (2016). Comparison of Patellar Tendon and
Hamstring Tendon Anterior Cruciate Ligament
Reconstruction: A 15-Year Follow-up of a Randomized
Controlled Trial. Am J Sports Med, 44(1), 83–90.
3. Sajovic M., Vengust V., Komadina R. và cộng
sự. (2006). A prospective, randomized
comparison of semitendinosus and gracilis tendon
versus patellar tendon autografts for anterior
cruciate ligament reconstruction: five-year follow-
up. Am J Sports Med, 34(12), 1933–1940.
4. Ahldén M., Kartus J., Ejerhed L. và cộng sự.
(2009). Knee laxity measurements after anterior
cruciate ligament reconstruction, using either
bone-patellar-tendon-bone or hamstring tendon
autografts, with special emphasis on comparison
over time. Knee Surg Sports Traumatol Arthrosc,
17(9), 1117–1124.
5. Ibrahim S.A.-R., Al-Kussary I.M., Al-Misfer
A.R.K. và cộng sự. (2005). Clinical evaluation of
arthroscopically assisted anterior cruciate ligament
reconstruction: patellar tendon versus gracilis and
semitendinosus autograft. Arthroscopy, 21(4),
412–417.
6. Karikis I., Desai N., Sernert N. và cộng sự.
(2016). Comparison of Anatomic Double- and
Single-Bundle Techniques for Anterior Cruciate
Ligament Reconstruction Using Hamstring Tendon
Autografts: A Prospective Randomized Study With
5-Year Clinical and Radiographic Follow-up. The
American Journal of Sports Medicine, 44(5), 1225–
1236.
7. Zaffagnini S., Marcacci M., Lo Presti M. và
cộng sự. (2006). Prospective and randomized
evaluation of ACL reconstruction with three
techniques: a clinical and radiographic evaluation
at 5 years follow-up. Knee Surg Sports Traumatol
Arthrosc, 14(11), 1060–1069.
8. Gifstad T., Sole A., Strand T. và cộng sự.
(2013). Long-term follow-up of patellar tendon
grafts or hamstring tendon grafts in endoscopic
ACL reconstructions. Knee Surg Sports Traumatol
Arthrosc, 21(3), 576–583.
9. Keays S.L., Bullock-Saxton J.E., Keays A.C. và
cộng sự. (2007). A 6-year follow-up of the effect
of graft site on strength, stability, range of motion,
function, and joint degeneration after anterior
cruciate ligament reconstruction: patellar tendon
versus semitendinosus and Gracilis tendon graft.
Am J Sports Med, 35(5), 729–739.
ĐÁNH GIÁ THỬ NGHIỆM ĐỘC TÍNH TẾ BÀO
CỦA MẢNH VÁ HỘP SỌ PEEK
Lê Thị Hồng Nhung*, Lưu Đình Mùi**, Nguyễn Lai Thành***
TÓM TẮT50
Nghiên cứu thử nghiệm đánh giá độc tính tế bào
của mảnh vá hộp sọ do Viện nghiên cứu và phát triển
vật liệu y sinh - Công ty cổ phần y sinh Ngọc Bảo chế
tạo từ vật liệu y sinh polyether ether ketone (PEEK).
Mục tiêu:
đánh giá khả năng gây độc cho tế bào thận
phôi người (HEK 293) của chất liệu mảnh xương sọ
PEEK.
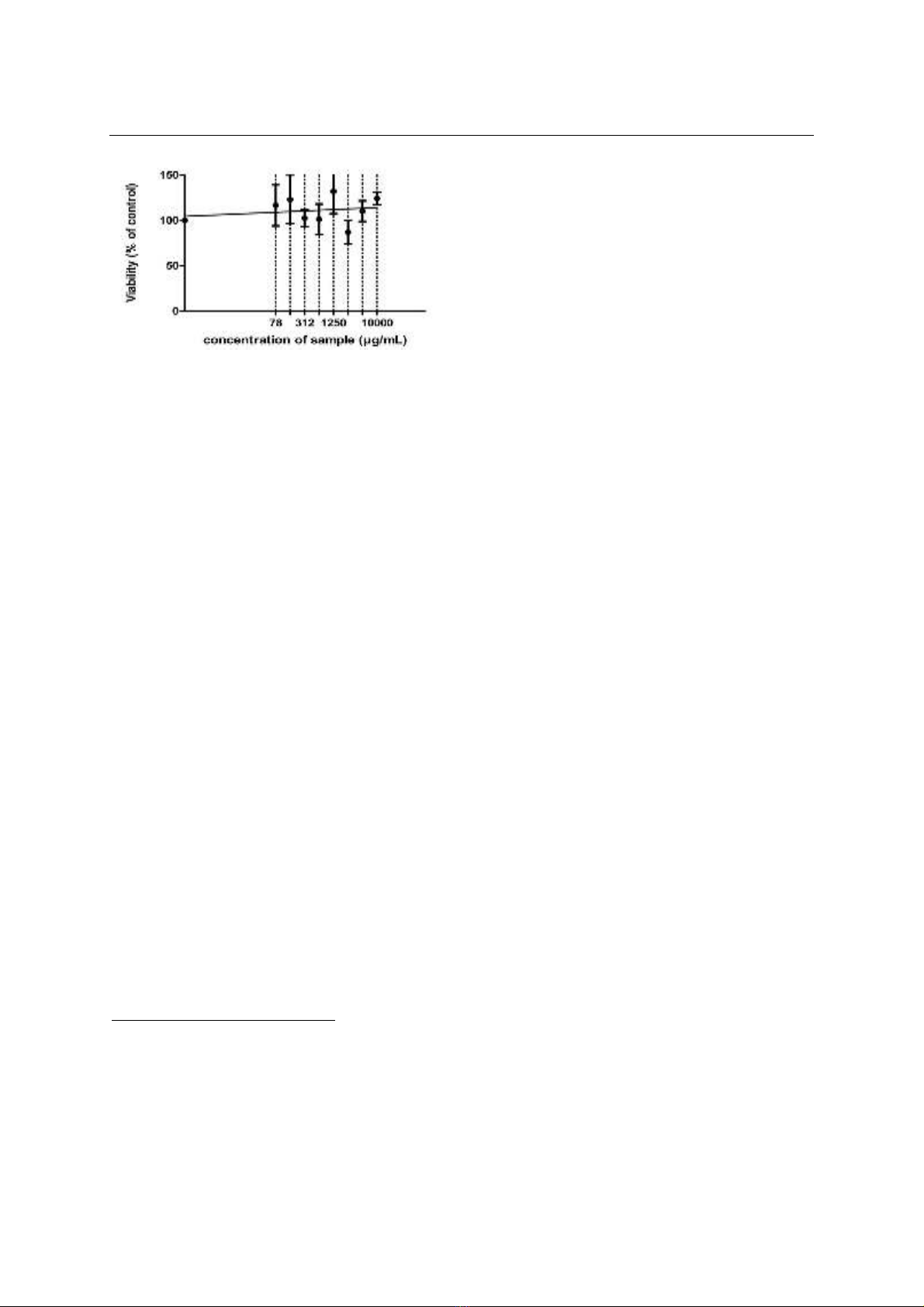
Vật liệu, phương pháp:
cho phơi nhiễm bột
mảnh xương sọ PEEK với tế bào HEK 293 ở các dải
nồng độ và thời gian tang dần.
Kết quả:
Tế bào ở tất
cả các giếng đều có hình thái tế bào và mức độ tăng
sinh bình thường hoàn toàn tương đương với đối
chứng. Kết luận: Vật liệu xương sọ nhân tạo PEEK
không có tác động độc tính gây chết trên dòng tế bào
HEK293 và có thể được coi là an toàn ở mức độ tế bào.
Từ khóa:
Độc tính tế bào, mảnh sọ PEEK, tạo
hình hộp sọ
*Trường đại học Y Hà Nội
**Viện Nghiên cứu và Phát triển vật liệu Y sinh
***Đại học Quốc gia Hà Nội
Chịu trách nhiệm chính: Lê Thị Hồng Nhung
Email: nhunglehmu@gmail.com
Ngày nhận bài: 9.01.2020
Ngày phản biện khoa học: 26.2.2020
Ngày duyệt bài: 10.3.2020
SUMMARY
INVITRO EVALUATION OF CYTOTOXICITY
OF PEEK SKULL IMPLANT
Experimental research on the cytotoxicity to
evaluate the skull PEEK implants was created by the
Institute for Research and Development of biomedical
materials Inst - Biomedical joint stock company Ngoc
Bao from the biomedical material polyether ether
ketone (PEEK). Target: Assess the cytotoxicity of PEEK
skull implant material to human embryos kidney 293
(HEK 293). Material, method: to skull implants PEEK
powder exposure with HEK cells 293 in the strips of
concentration and duration of the gradual tangent. The
result: cells in all wells have cell morphology and
normal levels of proliferation are equivalent to the
opposite. Conclusion: The material of skull implant
PEEK does not have a lethal toxic effect on the HEK293
cell and can be considered safe at the cellular level.
Keywords:
cytotoxicity, PEEK skull implant,
cranioplasty
I. ĐẶT VẤN ĐỀ
Độc tính tế bào (cytotoxicity) là yếu tố quan
trọng đối với một sản phẩm cấy ghép y tế theo
ISO 10993 và TCVN. Mảnh vá hộp sọ PEEK là
sản phẩm được chế tạo từ vật liệu y sinh
polyether ether ketone (PEEK). Đây là một loại