CHUYÊN ĐỀ: HỘI THẢO PHÒNG CHỐNG UNG THƯ HÀ NỘI 2024
134
KẾT QUẢ ĐIỀU TRỊ UNG THƯ CỔ TỬ CUNG GIAI ĐOẠN TIẾN TRIỂN,
TÁI PHÁT, DI CĂN BẰNG PHÁC ĐỒ HÓA CHẤT PACLITAXEL – PLATIN
KẾT HỢP BEVACIZUMAB TẠI BỆNH VIỆN UNG BƯỚU HÀ NỘI
Đinh Thị Hải Duyên1, Lê Văn Quảng2
TÓM TẮT17
Mục tiêu: Đánh giá kết quả điều trị và tác
dụng không mong muốn của phác đồ paclitaxel –
platin kết hợp bevacizumab trên bệnh nhân ung
thư cổ tử cung giai đoạn tiến triển, tái phát, di
căn tại bệnh viện Ung Bướu Hà Nội.
Đối tượng và phương pháp nghiên cứu:
Nghiên cứu mô tả hồi cứu kết hợp tiến cứu tiến
hành trên bệnh nhân ung thư cổ tử cung tái phát,
tiến triển, di căn được điều trị phác đồ TC
(paclitaxel-carboplatin/cisplatin) kết hợp
bevacizumab tại bệnh viện Ung Bướu Hà Nội từ
01/2020 đến 01/2024.
Kết quả: 51 bệnh nhân dủ tiêu chun tham
gia nghiên cứu. Bệnh nhân tái phát sau điều trị
hay gặp nhất ở giai đoạn III là 18/51 bệnh nhân,
chiếm 35,3%. Có 9/51 (17,6%) bệnh nhân di căn
xa ngay tại thời điểm chn đoán. Về đáp ứng,
11/51 (21,5%) bệnh nhân đạt đáp ứng hoàn toàn,
28/51 (54,9%) bệnh nhân đạt đáp ứng một phần,
tỷ lệ bệnh nhân đạt kiểm soát bệnh là 88,2%.
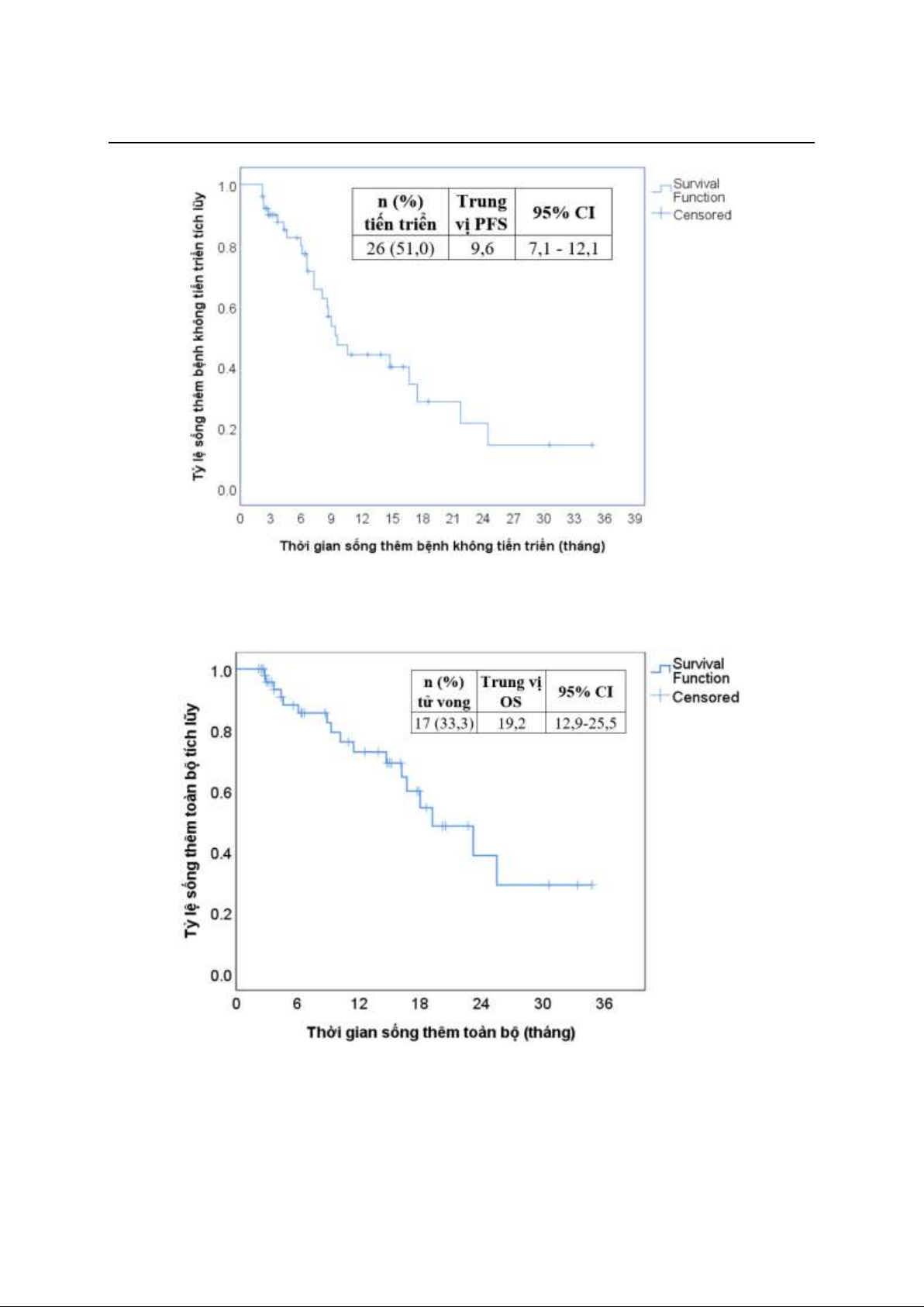
Trung vị thời gian sống thêm bệnh không tiến
triển (PFS) là 9,2 tháng, trung vị thời gian sống
thêm toàn bộ (OS) là 19,2 tháng. Tác dụng không
mong muốn chủ yếu gặp ở độ 1 và 2. Các tác
dụng không mong muốn thường gặp là buồn nôn,
1Bệnh viện Ung Bướu Hà Nội
2Bệnh viện K
Chịu trách nhiệm chính: Đinh Thị Hải Duyên
Email: dinhhaiduyen1986@gmail.com
Ngày nhận bài: 18/09/2024
Ngày phản biện khoa học: 26/09/2024
Ngày duyệt bài: 09/10/2024
hạ bạch cầu trung tính, tiêu chảy và thiếu máu,
lần lượt là 21/51 (41,2%), 18/51 (35,3%), 15/51
(29,4%) và 14/51 (27,5%) bệnh nhân. Ghi nhận
7/51 (13,7%) bệnh nhân có chảy máu và 2/51
(3,9%) bệnh nhân có THA độ 2 trong quá trình
điều trị bevacizumab.
Kết luận: Phác đồ paclitaxel-platin kết hợp
bevacizumab cho kết quả điều trị khả quan và
tương đối an toàn.
Từ khóa: Ung thư cổ tử cung, Bevacizumab, TC
SUMMARY
TREATMENT OUTCOMES OF
PATIENTS WITH PROGRESSIVE,
RECURRENT, METASTATIC
CERVICAL CANCER USING TC
CHEMOTHERAPY REGIMEN PLUS
BEVACIZUMAB AT HANOI
ONCOLOGY HOSPITAL
Objectives: To evaluate the treatment
outcomes and toxicity of the TC chemotherapy
regimen plus bevacizumab in patients with
advanced, recurrent, and metastatic cervical
cancer at Hanoi Oncology Hospital.
Subjects and Methods: A retrospective and
prospective descriptive study was conducted on
patients with recurrent, advanced, metastatic
cervical cancer treated with TC regimen
(paclitaxel-carboplatin/cisplatin) combined with
bevacizumab at Hanoi Oncology Hospital from
January 2020 to January 2024.
Results: 51 eligible patients were enrolled.
Patients who relapsed after treatment were most
commonly in stage III, for 35.3% (18/51). There