Ngày nhận bài: 17-12-2024 / Ngày chấp nhận đăng bài: 24-12-2024 / Ngày đăng bài: 28-12-2024
*Tác giả liên hệ: Vũ Thanh Thảo. Khoa Dược, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam.
E-mail: vuthanhthao@ump.edu.vn.
© 2024 Bản quyền thuộc về Tạp chí Y học Thành phố Hồ Chí Minh.
https://www.duoc.tapchiyhoctphcm.vn 55
ISSN : 1859-1779
Nghiên cứu Dược học
Tạp chí Y học Thành phố Hồ Chí Minh - Dược học;27(6):55-63
https://doi.org/10.32895/hcjm.p.2024.06.07
Nghiên cứu kỹ thuật multiplex RT-QPCR để kiểm tra chỉ
tiêu Staphylococcus aureus và Pseudomonas aeruginosa
trong mỹ phẩm
Trần Quang Ngọc Dũng1, Lê Văn Hoài Trân1, Lê Văn Thanh2, Trịnh Túy An1, Vũ Thanh Thảo1,3,*
1Trung tâm Khoa học Công nghệ Dược Sài Gòn, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh,
Việt Nam
2Bệnh viện Chợ Rẫy, Thành phố Hồ Chí Minh, Việt Nam
3Khoa Dược, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam
Tóm tắt
Đặt vấn đề: Theo hướng dẫn của TCVN 13634:2023, chỉ tiêu Staphylococcus aureus (S. aureus) và Pseudomonas
aeruginosa (P. aeruginosa) là yêu cầu bắt buộc trong kiểm tra giới hạn nhiễm khuẩn của mỹ phẩm. Kỹ thuật mutiplex
RT-qPCR cho phép phát hiện nhanh và đồng thời các vi sinh vật chỉ thị dựa trên các gen đặc hiệu với độ nhạy và chính
xác cao.
Mục tiêu: Ứng dụng kỹ thuật multiplex RT-qPCR để kiểm tra chỉ tiêu S. aureus và P. aeruginosa trong mỹ phẩm.
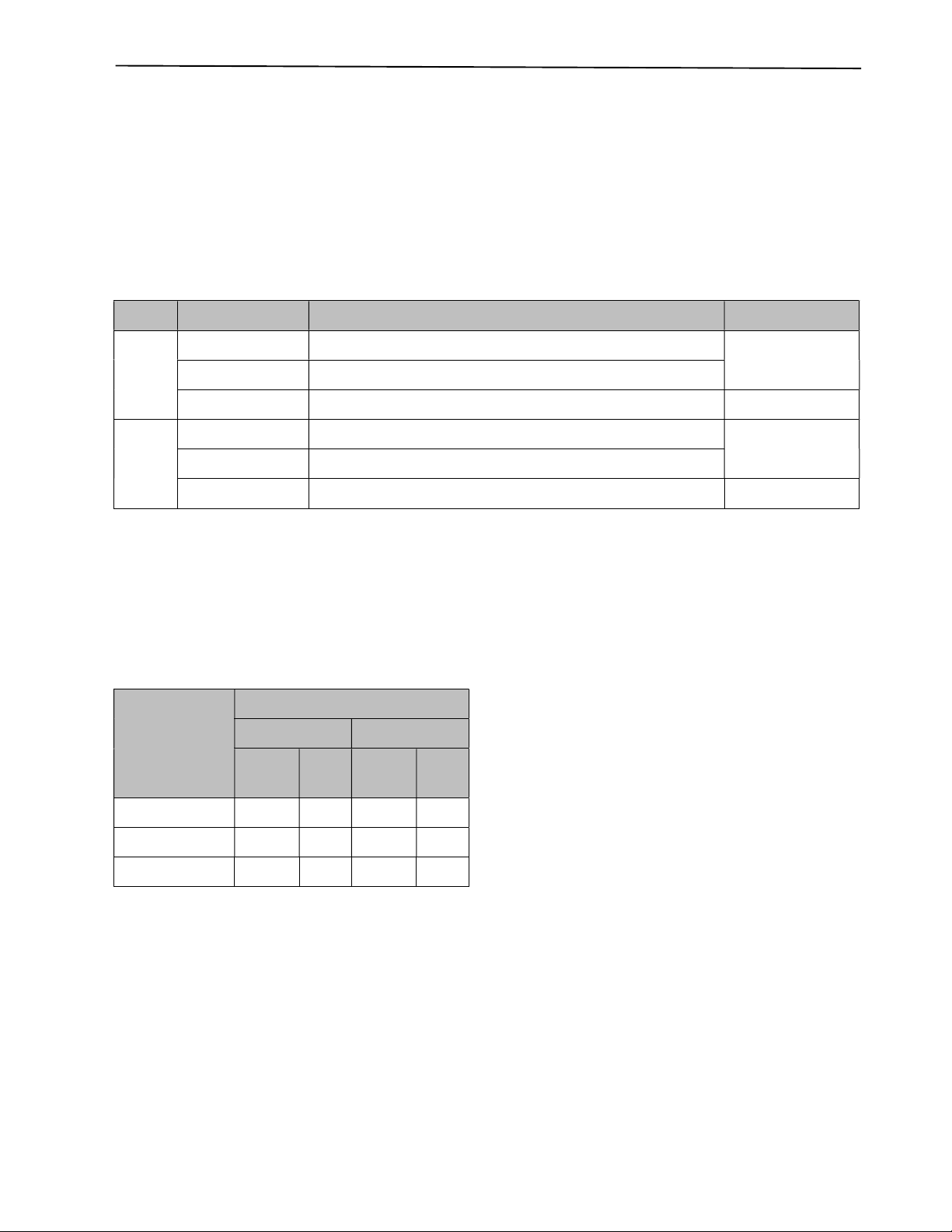
Đối tượng và phương pháp nghiên cứu: Mồi và đoạn dò được đánh giá in vitro để lựa chọn nồng độ thích hợp. Quy trình
định tính các vi khuẩn bằng mutiplex RT-qPCR được thẩm định độ đặc hiệu, tính tuyến tính và độ chính xác theo hướng
dẫn của Broeders. Sau đó, hiệu quả pháp hiện của phương pháp multiplex RT-PCR được so sánh với phương pháp vi
sinh trên 30 mẫu mỹ phẩm giả định.
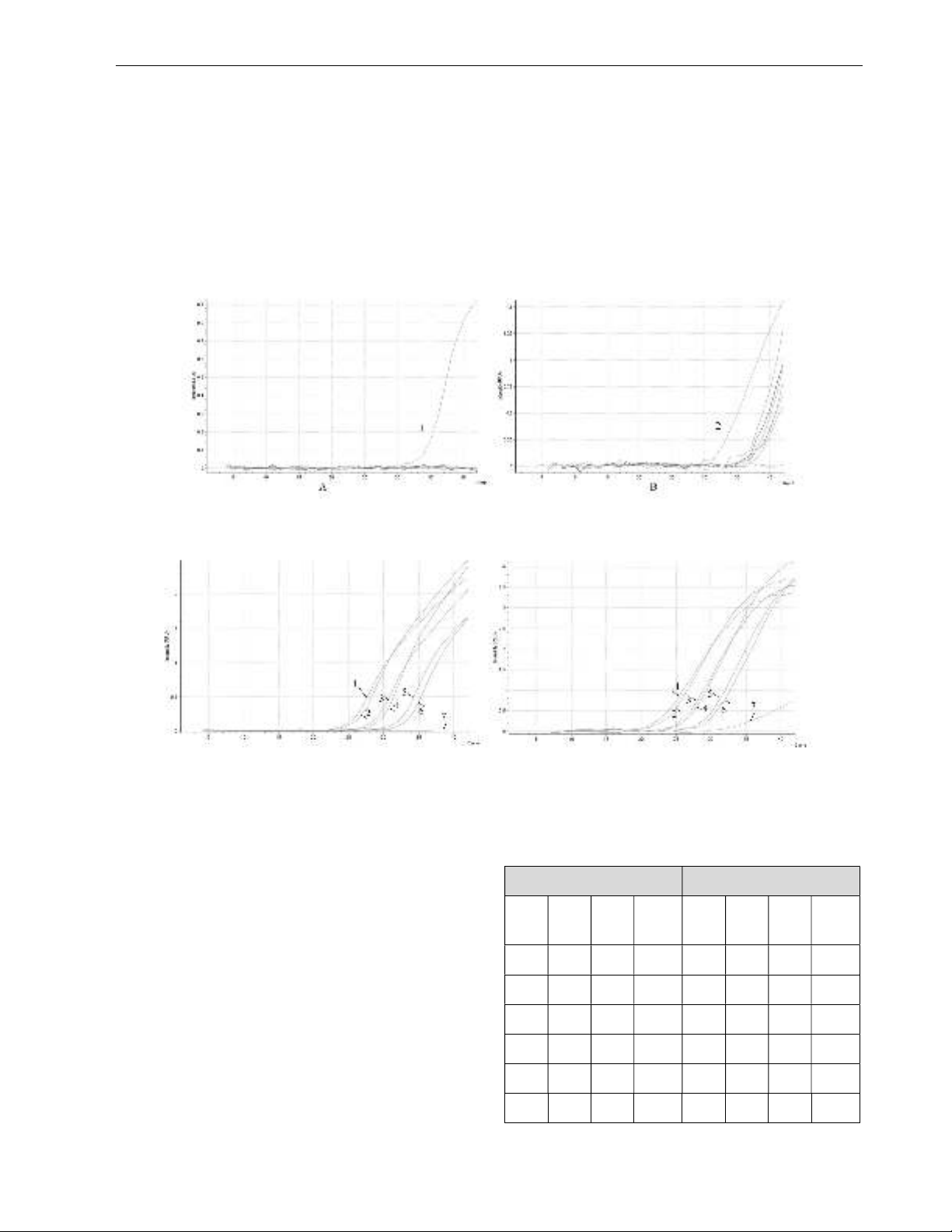
Kết quả: Kết quả thu được chứng minh rằng phương pháp multiplex RT-qPCR, sử dụng cặp mồi gyrB_F/gyrB_R (400
nM) với đoạn dò gyrB_P-GS (200 nM) đối với S. aureus và cặp mồi pbp-2_F/pbp-2_R (400 nM) với đoạn dò pbp-2 P-
GS (200 nM) đối với P. aeruginosa, đạt được độ đặc hiệu, tính tuyến tính và độ chính xác (RSD< 25%). Phương pháp
multiplex RT-qPCR phát hiện S. aureus và P. aeruginosa cho thấy có hiệu quả phát hiện tương đương với phương pháp
vi sinh theo TCVN 13634:2023 trên mẫu mỹ phẩm giả định.
Kết luận: Kỹ thuật mutiplex RT-qPCR có thể áp dụng để kiểm tra chỉ tiêu S. aureus và P. aeruginosa trong giới hạn nhiễm
vi sinh vật của mỹ phẩm.
Từ khóa: mutiplex RT-qPCR; Staphylococcus aureus; Pseudomonas aeruginosa; giới hạn nhiễm vi sinh vật