Đ C NG ÔN T P KI M TRA T NG H P MÔN HÓA 9Ề ƯƠ Ậ Ể Ổ Ợ
Câu 1: Cho các phát bi u sau:ể
(1) Các nguyên t thu c nhóm IA là kim lo i ki m.ố ộ ạ ề
(2) Các mu i c a ố ủ
3
Fe +
ch th hi n tính oxi hóa.ỉ ể ệ
(3) V i đn ch t là phi kim ch t nào có đ âm đi n l n h n thì ho t đng m nh h n ch t có đ âm ớ ơ ấ ấ ộ ệ ớ ơ ạ ộ ạ ơ ấ ộ
đi n nh h n.ệ ỏ ơ
(4) Có th đi u ch Al b ng cách đi n phân nóng ch y mu i AlClể ề ế ằ ệ ả ố 3.
(5) Th ch cao nung có th đc dùng đ đúc t ng và bó b t khi gãy x ng.ạ ể ượ ể ượ ộ ươ
S đáp án đúng là :ố
A.1B.2C.3D.4
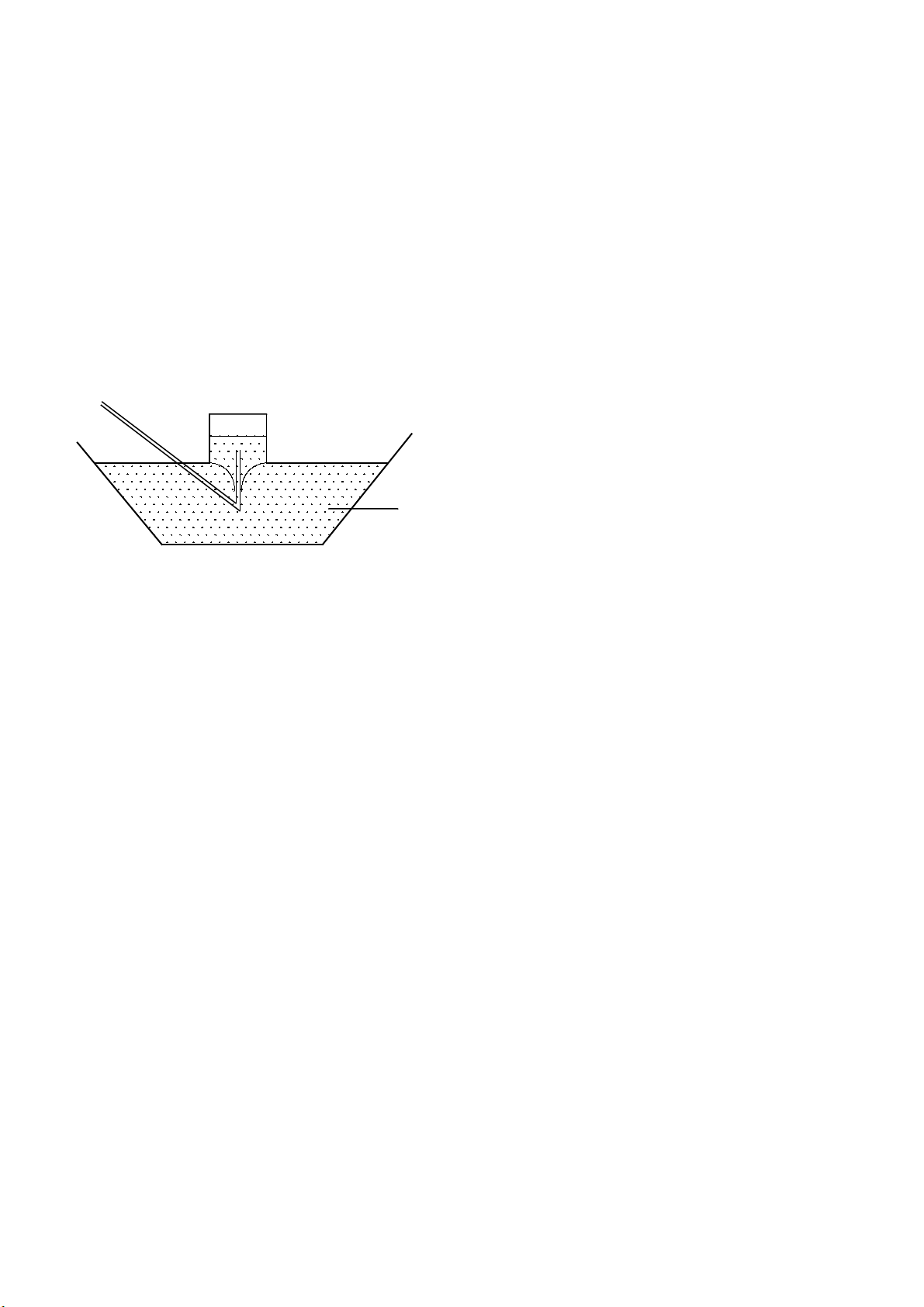
Câu 2: Hình v sau mô t các cách thu khí th ng đc s d ng khi đi u ch và thu khí trong phòng ẽ ả ườ ượ ử ụ ề ế
thí nghi m. V i mô hình đó ta có th dùng đ thu đc nh ng khí nào trong các khí sau: Hệ ớ ể ể ượ ữ 2, C2H2 , NH3
, SO2 , HCl , N2.
A. HCl, SO2, NH3B. H2, N2 , C2H2C. H2 , N2, NH3D. N2, H2
Câu 3:Trong các thí nghi m sau:ệ
(1) S c etilen vào dung d ch brom trong CClụ ị 4.
(2) Cho phenol vào dung d ch đun nóng ch a đng th i HNOị ứ ồ ờ 3 đc và Hặ2SO4 đc.ặ
(3) Cho axit stearic vào dung d ch Ca(OH)ị2.
(4) Cho phenol vào n c brom.ướ
(5) Cho anilin vào n c brom.ướ
(6) Cho glyxylalanin vào dung d ch NaOH loãng, d .ị ư
(7) Cho HCOOH vào dung d ch AgNOị3/NH3.
S thí nghi m có k t t a xu t hi n làố ệ ế ủ ấ ệ
A.6B.3C.4D.5
Câu 4: S đng phân là ancol th m ng v i CTPT Cố ồ ơ ứ ớ 9H12O là :
A.17 B.18 C.19 D.20
Câu 5 : Cho các phát bi u sau:ể
(1) Trong ph n ng hóa h c thì ph n ng nhi t phân là ph n ng oxi hóa kh .ả ứ ọ ả ứ ệ ả ứ ử
(2) Supe photphat kép có thành ph n ch g m Caầ ỉ ồ (H2PO4)2.
(3) Amophot là m t lo i phân h n h p.ộ ạ ỗ ợ
(4) Có th t n t i dung d ch có các ch t: Fe(NOể ồ ạ ị ấ 3)2, H2SO4, NaCl.
(5) Đ dung d ch ch a NHổ ị ứ 4Cl vào dung d ch ch a NaAlOị ứ 2 th y k t t a xu t hi n.ấ ế ủ ấ ệ
(6) Nh ng ch t tan hoàn toàn trong n c là nh ng ch t đi n ly m nh.ữ ấ ướ ữ ấ ệ ạ
(7) Ch t mà tan trong n c t o thành dung d ch d n đc đi n là ch t đi n ly.ấ ướ ạ ị ẫ ượ ệ ấ ệ
(8) Cho khí Cl2 qua gi y t m qu tím m (màu tím) th y gi y bi n thành màu đ.ấ ẩ ỳ ẩ ấ ấ ế ỏ
S phát bi u đúng là :ố ể
A.5B.4C.3D.2
1
H2O





