PHÒNG GD & ĐT
HUY N VĂN BÀNỆ
K THI CH N HOC SINH GIOI L P 6,7,8Ỳ Ọ Ơ CÂP HUY NỆ
NĂM HOC 2019 – 2020
Môn thi: Hóa h c 8ọ
Th i gian lam bai: 150 phut, không kê th i gian giao đê ơ ơ
(Đ thi g m có ề ồ 02 trang, 10 câu)
Bài 1. (1,5 đi m)ể
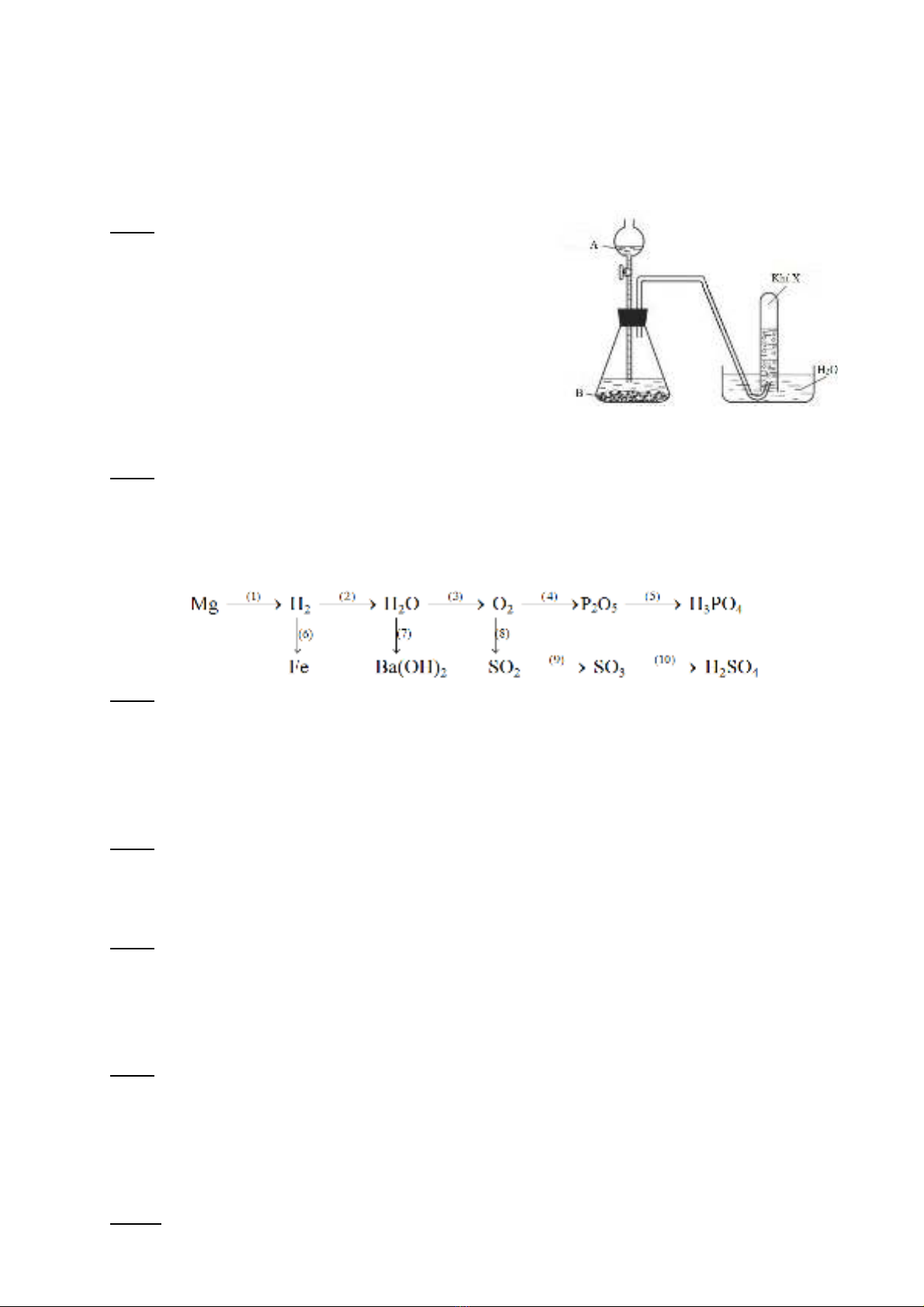
1. Hình bên mô t h th ng thi t b dùngả ệ ố ế ị
đi u ch khí X trong phòng thí nghi m.ề ế ệ
a. Khí X là khí gì? Nêu nguyên t c chung đắ ể
đi u ch khí X b ng thi t b này.ề ế ằ ế ị
b. Xác đnh các ch t A, B t ng ng và vi tị ấ ươ ứ ế
ph ng trình ph n ng x y ra.ươ ả ứ ả
2. Cho l n l t 4 ch t r n Na, Fe, CaO, Pầ ượ ấ ắ 2O5 vào 4 c c đng n c và cho gi yố ự ướ ấ
qu tím vào 4 c c. Nêu hi n t ng và vi t các ph ng trình ph n ng x y ra (n u có).ỳ ố ệ ượ ế ươ ả ứ ả ế
Bài 2. (3,5 đi m)ể
1. B ng ph ng pháp hóa h c, hãy nh n bi t các ch t r n màu tr ng đng riêngằ ươ ọ ậ ế ấ ắ ắ ự
bi t trong các l m t nhãn g m: Pệ ọ ấ ồ 2O5; CaO; NaCl; Na2O.
2. Vi t các PTHH th c hi n chuy n hóa sau (ghi rõ đi u ki n ph n ng, n uế ự ệ ể ề ệ ả ứ ế
có):
Bài 3. (2,5 đi m)ể
H n h p B g m hai khí: cacbon oxit và hiđro có t kh i đi v i Hỗ ợ ồ ỉ ố ố ớ 2 là 10,75. Để
kh hoàn toàn m gam Feử3O4 nung nóng c n v a đ V lít h n h p B ( đktc). K t thúcầ ừ ủ ỗ ợ ở ế
ph n ng thu đc 16,8 gam Fe.ả ứ ượ
a. Tính thành ph n ph n trăm v th tích c a m i khí trong h n h p B.ầ ầ ề ể ủ ỗ ỗ ợ
b. Tính V và m.
Bài 4. (2,0 đi m)ể
Dùng khí H2 d đ kh hoàn toàn m gam m t oxit s t, sau ph n ng thu đcư ể ử ộ ắ ả ứ ượ
5,4 gam n c. L y toàn b l ng kim lo i thu đc trên hòa tan vào dung d ch HClướ ấ ộ ượ ạ ượ ở ị
d thì thu đc 25,4 gam mu i. Tìm công th c oxit s t và tính giá tr c a m?ư ượ ố ứ ắ ị ủ
Bài 5. (2,0 đi m)ể
1. L p công th c hóa h c c a h p ch t t o b i s t và oxi, bi t c 7 ph n kh iậ ứ ọ ủ ợ ấ ạ ở ắ ế ứ ầ ố
l ng s t thì k t h p v i 3 ph n kh i l ng oxi.ượ ắ ế ợ ớ ầ ố ượ
2. Hòa tan hoàn toàn 27,84 gam m t oxit s t c n dùng v a đ 480 ml dung d chộ ắ ầ ừ ủ ị
HCl 2M. Xác đnh công th c hóa h c c a oxit s t nói trên.ị ứ ọ ủ ắ
Bài 6. (2,0 đi m)ể
Cho lu ng khí hiđro đi qua ng thu tinh ch a 20 g b t đng (II) oxit (màu đen)ồ ố ỷ ứ ộ ồ
nhi t đ cao. Sau m t th i gian ph n ng thu đc 16,8 g ch t r n.ở ệ ộ ộ ờ ả ứ ượ ấ ắ
a. Nêu hi n t ng ph n ng x y ra.ệ ượ ả ứ ả
b. Tính hi u su t ph n ng.ệ ấ ả ứ
c. Tính s lít khí hiđro đã tham gia kh đng (II) oxit trên đktc.ố ử ồ ở
Câu 7. (2,5 đi m)ể