SỞ GD&ĐT QUẢNG NGÃI
TRƯỜNG THPT QUANG TRUNG
(Đề thi có 04 trang)
KỲ THI THỬ TỐT NGHIỆP THPT NĂM 2025
Bài thi: KHOA HỌC TỰ NHIÊN
Môn thi thành phần: HÓA HỌC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Họ, tên thí sinh: .....................................................................
Số báo danh: ..........................................................................
• Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al =
27; P=31; S = 32; C1 = 35,5; K = 39; Fe = 56; Cu = 64; Zn= 65; Ag=108; Ba = 137.
• Các thể tích khí đều đo ở điều kiện tiêu chuẩn; giả thiết các khí sinh ra không tan trong nước.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 16.
Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Cho các yếu tố sau:
1. nồng độ chất. 2. áp suất. 3. xúc tác. 4. nhiệt độ. 5. diện tích tiếp xúc.
Những yếu tố ảnh hưởng đến tốc độ phản ứng nói chung là
A. 1, 2, 3, 4. B. 2, 3, 4, 5. C. 1, 3, 5. D. 1, 2, 3, 4, 5.
Câu 2. Chất nào sau đây là chất điện li mạnh?
A. CH3COOH. B. C2H5OH. C. H2O. D. NaCl.
Câu 3. Các số oxi hóa có thể có của nitrogen là
A. 0, +1, +2, +3, +4, +5. B. -3, 0 , +1, +2, +3, +5.
C. 0, +1, +2, +5. D. -3, 0 , +1, +2, +3, +4, +5.
Câu 4. Hiện tượng các chất có cấu tạo và tính chất hoá học tương tự nhau, phân tử hơn kém nhau
một hay nhiều nhóm methylen (–CH2–) được gọi là hiện tượng
A. đồng phân. B. đồng vị. C. đồng đẳng. D. đồng khối.
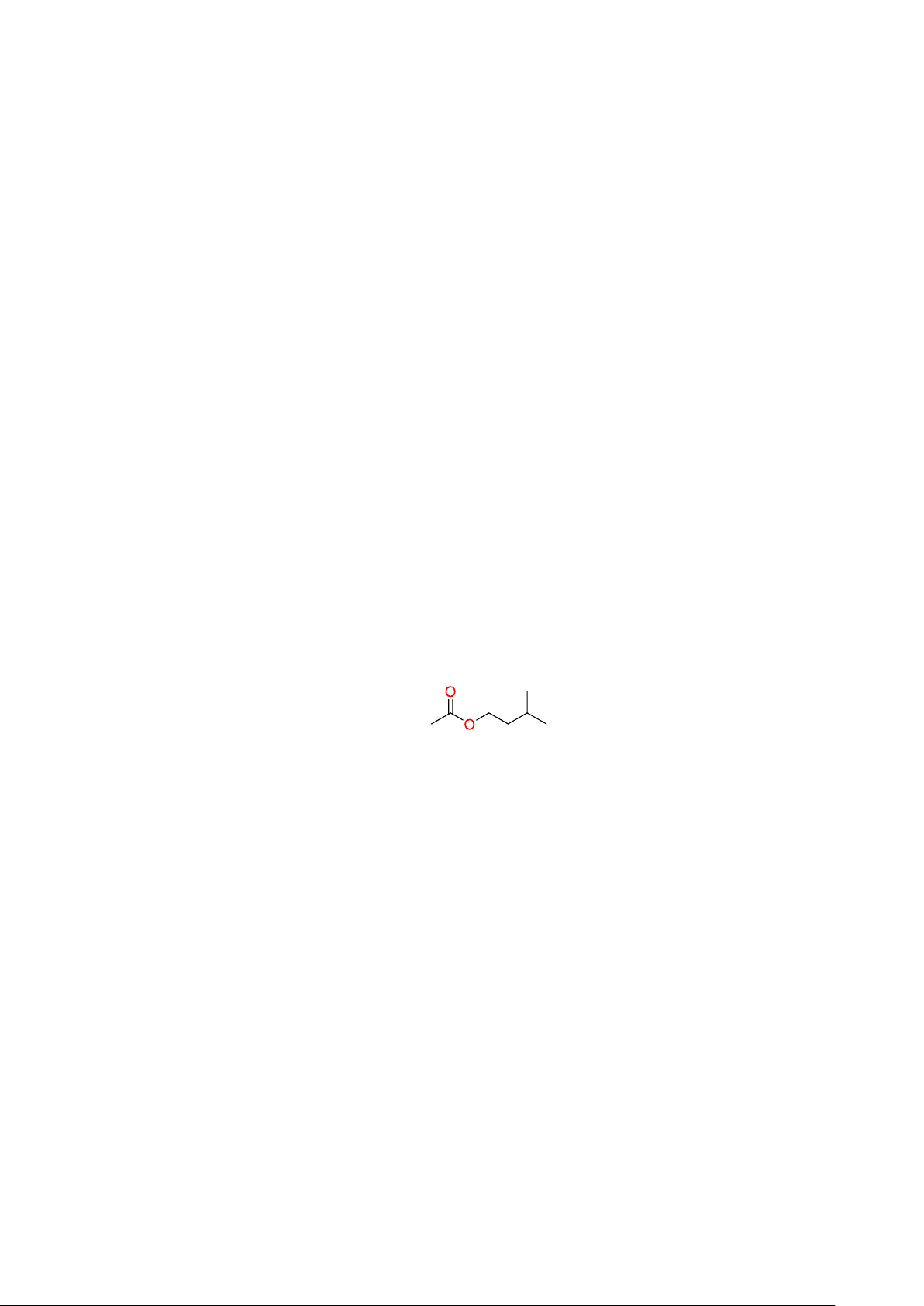
Câu 5. Công thức cấu tạo thu gọn nào phù hợp với khung phân tử của ester ở hình dưới?
A. CH3COOCH2CH2CH(CH3)2. B. CH3OOCCH2CH2CH(CH3)2.
C. HCOOCH2CH2CH(CH3)2. D. CH3COOCH2C(CH3)3.
Câu 6. Phát biểu nào sau đây đúng?
A. Glucose là chất rắn, màu trắng ở điều kiện thường.
B. Hồ tinh bột có phản ứng với dung dịch iodine tạo hợp chất màu xanh tím.
C. Cellulose thuộc loại monosaccarite
D. Saccharose là thành phần chủ yếu, tạo vị ngọt sắc trong mật ong.
Câu 7. Ở điều kiện thường, chất nào sau đây là chất rắn?
A. Đimethylamine. B. Ethylamine. C. Glycine. D. Methylamine.
Câu 8. Phát biểu nào sau đây là sai?
A. Dung dịch Glutamic acid làm quì tím chuyển màu hồng.
B. Amino acid là hợp chất hữu cơ tạp chức.
C. Dung dịch glycine không làm đổi màu phenolphtalein.
D. Aniline tác dụng với nước bromine tạo thành kết tủa vàng.
Câu 9. Amino acid đầu N trong phân tử peptide Gly-Val-Glu-Ala là
A. Alanine. B. Glycine. C. glutamic acid. D. Valine.
Câu 10. Vật liệu tổng hợp X là chất vô định hình, cách điện tốt, bền với acid, được dùng làm vật
liệu cách điện, ống dẫn nước, vải che mưa,… Vật liệu X là