
1/17/2018
1
1
VẬT LÝ ĐẠI CƯƠNG
Giảng viên: TS. Nguyễn Văn Nghĩa
Email: nguyenvannghia@hau.edu.vn
Mobile: 0913812008
ĐỀ CƢƠNG CHI TIẾT HỌC PHẦN
1. Thông tin chung về môn học:
- Tên học phần: VẬT LÝ ĐẠI CƢƠNG
-Số tín chỉ: 02 TC LT: 02 TH: 0
-Số tiết học:30 tiết
2. Tài liệu học tập:
-Vật lý đại cƣơng Tập 1: Cơ nhiệt
- Bài tập Vật lý Đại cƣơng: Tập 1
-Vật lý đại cƣơng Tập 2: Điện – Dao động – Sóng
- Bài tập Vật lý Đại cƣơng: Tập 2
(Lƣơng Duyên Bình chủ biên, NXB Giáo dục)
- Tham khảo:
Bài giảng VLDC –Bộ môn Vật lý
2
3. Nội dung môn học:
Phần Nhiệt
Chương 1: Các định luật thực nghiệm chất khí (3T)
1.1. Khái niệm
1.2. Các định luật thực nghiệm
1.3. Phương trình trạng thái của khí lý tưởng
Chương 2: Thuyết động học phân tử (3T)
2.1. Thuyết động học phân tử
2.2. Nội năng khí lý tưởng
2.3. Định luật phân bố Bônzman
Chương 3: Nguyên lý I nhiệt động học (3T)
3.1. Nội năng của hệ nhiệt động. Công và nhiệt
3.2. Nguyên lý I nhiệt động học
3.3. Dùng nguyên lý I để khảo sát các quá trình cân bằng
Chương 4: Nguyên lý II nhiệt động học (3T)
4.1. Hạn chế của nguyên lý I
4.2. Quá trình thuận nghịch và không thuận nghịch
4.3. Nguyên lý II
4.4. Chu trình Cácnô và định lý. Biểu thức định lượng
nguyên lý II
Chương 5: Khí thực (3T –Tự học)
5.1. Phương trình trạng thái khí thực
5.2. Nghiên cứu khí thực bằng thực nghiệm
5.3. Nội năng khí thực và hiệu ứng Jun – Tômxơn
Phần Điện
Chương 1: Trường tĩnh điện (4T)
1.1. Khái niệm
1.2. Định luật Culông
1.3. Điện trường
1.4. Điện thông và địnhlý Ôxtôgratsky-Gaux
1.5. Điện thế
Chương 2: Vật dẫn (3T)
2.1. Điều kiện vật dẫn cân bằng tĩnh điện
2.2. Hiện tượng điện hưởng
2.3. Điện dung vật dẫn và tụ điện
2.4. Năng lượng điện trường
Chương 3: Những định luật cơ bản của dòng không đổi (Tự
đọc)
3.1. Bản chất dòng điện
3.2. Những đại lượng đặc trưng của dòng không đổi
3.3. Định luật Ôm thuần điện trở
3.4. Định luật Kiarôkhốp
Chương 4: Từ trường không đổi (4T)
4.1. Tương tác từ và định luật Ampe
4.2. Cảm ứng từ và cường độ từ trường
4.3. Từ thông và định lý Ôxtôgratsky-Gaux
4.4. Định lý dòng toàn phần
4.5. Tác dụng của từ trường lên hạt điện chuyển động
Chương 5: Cảm ứng điện từ (4T)
5.1. Định luật cảm ứng điện từ
5.2. Hiện tượng tự cảm
5.3. Hiện tượng hỗ cảm
5.4. Năng lượng từ trường
4. Phương pháp đánh giá học phần:
Điểm quá trình: 02/10
Điểm thi kết thúc học phần: 08/10
* Thi kết thúc: + Hình thức thi: Viết tự luận
+ Thời gian thi: 60 phút
CHƯƠNG I. NHỮNG ĐỊNH LUẬT THỰC NGHIỆM
§1. MỘT SỐ KHÁI NIỆM.
§2. CÁC ĐỊNH LUẬT THỰC NGHIỆM CỦA CHẤT KHÍ.
§3. PHƯƠNG TRÌNH TRẠNG THÁI CỦA KHÍ LÍ TƯỞNG.
3
PHẦN NHIỆT HỌC
1. Thông số trạng thái và phương trình trạng thái.
4
+Nếu tính chất của vật biến đổi => trạng thái vật biến đổi =>
trạng thái vật đƣợc
xác định bằng tập hợp các tính chất
.
+Mỗi tính chất đƣợc đặc trƣng bằng một đại lƣợng vật lý –
các đại lƣợng vật lý
đƣợc gọi là các thông số trạng thái.
+Chỉ có một số thông số trạng thái là những thông số độc lập các thông số trạng thái
còn lại là những thông số phụ thuộc.
+
Phƣơng trình nêu mối liên hệ các thông số trạng thái gọi là phƣơng trình
trạng thái.
+Với khối khí: trạng thái đƣợc xác định bởi:V, Pvà T. Trong đó có 2 thông số độc lập
=> pt trạng thái của một khối khí là:
0),,( TVPf
§1. MỘT SỐ KHÁI NIỆM.
2. Khái niệm về nhiệt độ và áp suất.
5
+
Áp suất: có giá trị bằng lực nén vuông góc lên một đơn vị diện tích :
Đơn vị áp suất:
1 N/m2(= 1 Pa); at; atm; mmHg (còn gọi là torr); psi; bar
1 at = 736 mmHg = 9,81.104 N/m2;
1 atm =1,033 at = 760mmHg = 1,013.105N/m2;
Áp suất khí quyển: P0=1,033at = 760mmHg
+
Nhiệt độ
:
Nhiệt độ là đại lƣợng vật lý đặc trƣng cho mức độ chuyển động hỗn loạn của phân tử
của các vật
Hay dùng hai thang đo nhiệt độ: thang nhiệt độ bách phân hay nhiệt độ Xenxiuyt (ký hiệu t0C),
thang nhiệt độ tuyệt đối (ký hiệu T0K):
n
S
F
P
273 tT
6
Nghiên cứu chất khí bằng thực nghiệm tìm ra sự liên hệ giữa hai
trong ba thông số P, V, Tbằng cách xét các quá trình biến đổi trạng thái của
khối khí, khi giữ 1 thông số không đổi.Có 3 quá trình:
a) đẳng nhiệt: T = const
b) đẳng tích: V = const
c) đẳng áp: P = const
§2. CÁC ĐỊNH LUẬT THỰC NGHIỆM CỦA CHẤT KHÍ.
1/17/2018
2
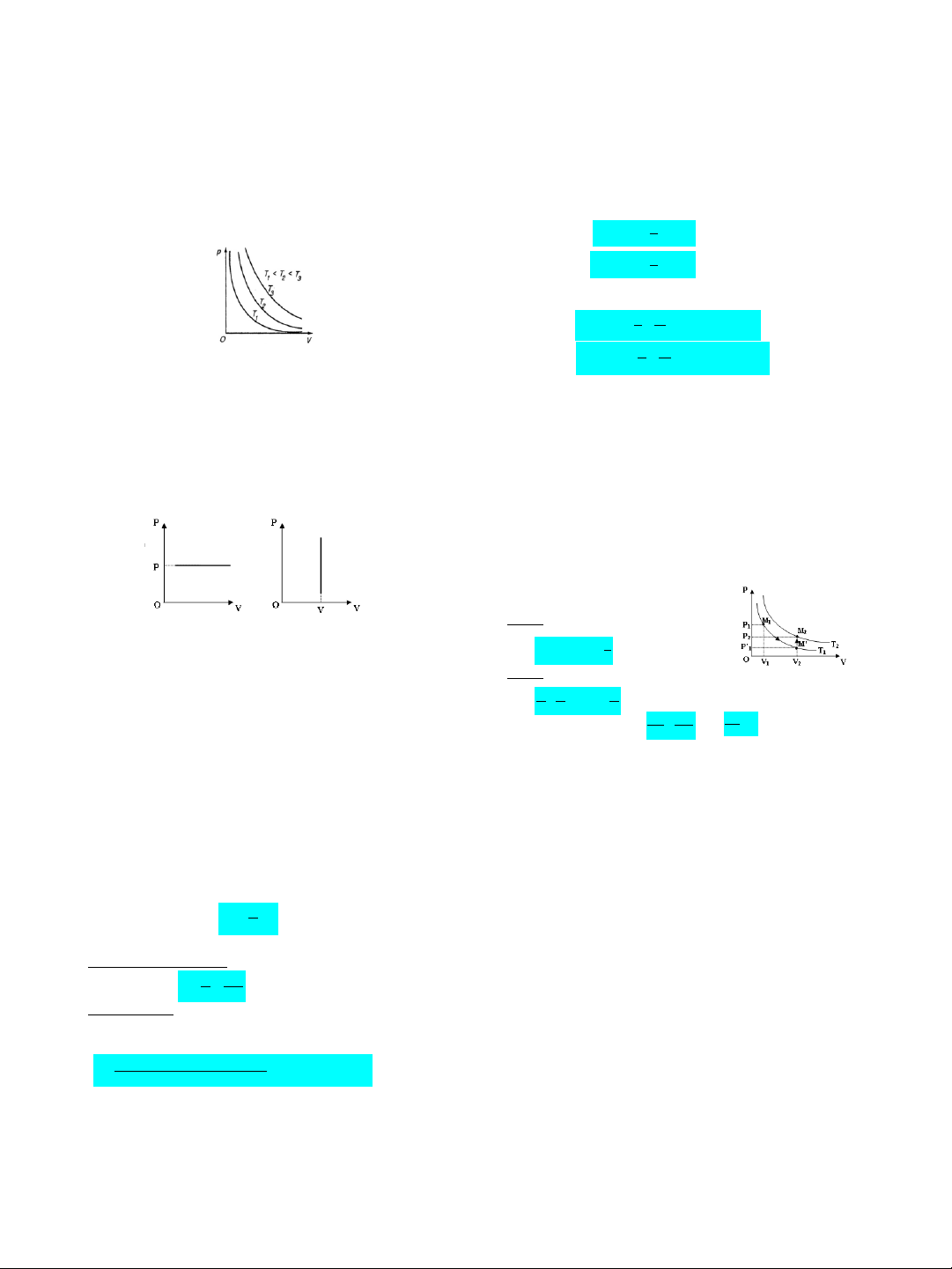
1. Định luật Bôilơ-Mariôt (BL).
7
+ Phƣơng trình: T = const PV =const hoặc P1V1= P2V2
+ Phát biểu:
Với khối khí xác định (m = hằng số) khi giữ nguyên nhiệt độ khối
khí không đổi thì tích số giữa P và V là một hằng số
+ Đồ thị:
Họ đƣờng đẳng nhiệt
2. Định luật Gay-Luytxắc (GL).
8
+Pb:
Với khối khí xác định, khi giữ nguyên thể tích khối khí thì áp suất tỉ lệ
bậc nhất với nhiệt độ tuyệt đối của khối khí ,khi giữ nguyên áp suất thì thể tích
tỉ lệ bậc nhất với nhiệt độ tuyệt đối.
+ Phƣơng trình:
;const
T
P
constV
const
T
V
constP
+Gọi P0, V0, T0là áp suất, thể tích, áp suất ở điều kiện tiêu chuẩn với T0=273 0Kvà
= 1/273 là hệ số dãn nở nhiệt các phƣơng trình đƣợc viết dƣới dạng:
TPPP
T
P
T
P
constV ... 00
0
0
TVVV
T
V
T
V
constP ... 00
0
0
9
+ Đồ thị:
Đồ thị biểu diễn quá trình đẳng áp và đẳng tích
3. Giới hạn ứng dụng của định luật thực nghiệm
Các định luật trên chỉ đúng trong điều kiện phòng thí nghiệm Nén mạnh hoặc hạ
T thấp thì các định luật trên không còn đúng nữa.
2. Thiết lập phương trình trạng thái của khí lí tưởng
10
*Biến đổi 1 kmol khí:TT1(P1,V1,T1)=> TT2(P2,V2, T2).
+Giả sử quá trình biến đổi thông qua 2 giai đoạn:
Giai đoạn 1
: Dãn đẳng nhiệt
từ TT1(P1,V1,T1)=> TT1’(P’1,V2,T1). Theo định luật BL:
2
1
1
'
12
'
111 ... V
V
PPVPVP
(*)
Giai đoạn 2
: Nung nóng đẳng tích từ TT1’(P’ ,V2,T1)=> TT2(P2,V2,T2). Theo định luật GL:
''
1 2 1
12
1 2 2
.
P P T
PP
T T T
(**)
+ Thay (**) vào phƣơng trình (*) đƣợc :
2
22
1
11 TVP
T
VP
R
T
PV
(Phƣơng trình trạng thái của 1 kmol khí lí tƣởng)
1. Khí lý tưởng.
+ Định nghĩa: “Khí lý tưởng là chất khí tuân theo hoàn toàn chính xác các định luật thực nghiệm”.
+ Đặc điểm: các phân tử khí coi là chất điểm và bỏ qua tương tác giữa chúng.
§3. PHƯƠNG TRÌNH TRẠNG THÁI CỦA KHÍ LÍ TƯỞNG.
11
*
Tính khối lƣợng riêng khối khí
:
*Đối với khối khí có khối lƣợng m bất kì ta có:
(PTTT tổng quát của một khối khí lí tƣởng)
RT
m
PV
.mP
V RT
* Tính hằng số khí R:
Ở điều kiện tiêu chuẩn (1kmol): T0=273,160K, P0=1,033 at = 1,013.105N/m2thì V0
=22,4 m3. Thay vào PTTT của 1kmol khí ta đƣợc hằng số R:
)./(10.31,8
16,273 )/(4,22)./(10.013,1 3
325 KkmolJ
KkmolmmN
Ro
12
Bài 1-1. Có40 gkhíôxy chiếm thể tích 3 lít, ápsuất 10 at.
a) Tính nhiệt độ của khối khí?
b) Cho khối khígiãn nở đẳng ápđến thể tích 4 lít. Hỏi nhiệt độ của khối khísau khi giãn
nở?
Bài 1-2. Có 10 g khí hyđrô ở áp suất 8,2 at đựng trong một bình có thể tích 20 lít.
a) Tính nhiệt độ của khối khí?
b) Hơ nóng đẳng tích khối khí này đến khi áp suất của nó bằng 9 at. Tính nhiệt độ của
khối khí sau khi hơ nóng?
Bài 1-3. Có 10 kg khí đựng trong một bình áp suất 107N/m2. Ngƣời ta lấy ở bình ra một lƣợng khí
cho tới khi áp suất của khí còn lại trong bình bằng 2,5.106 N/m2. Coi nhiệt độ của khối khí không
đổi. Tìm lƣợng khí đã lấy ra?
Bài 1-4. Có 10 g khí ôxy ở nhiệt độ 10ºC, áp suất 3 at. Sau khi hơ nóng đẳng áp, khối khí chiếm
thể tích 10 lít. Tìm:
a) Thể tích khối khí trƣớc khi giãn nở?
b) Nhiệt độ khối khí sau khi giãn nở?
c) Khối lƣợng riêng của khối khí trƣớc và sau khi giãn nở?
Bài 1-5. Có hai bình cầu đƣợc nối với nhau bằng một ống có khóa, đựng cùng một chất khí. Áp
suất ở bình thứ nhất là 2.105N/m2, ở bình thứ 2 là 106N/m2. Mở khóa nhẹ nhàng để hai bình
thông nhau sao cho nhiệt độ khí vẫn không đổi. Khi đã cân bằng, áp suất ở hai bình là 4.105N/m2.
Tìm thể tích của bình cầu thứ 2, nếu biết thể tích của bình cầu thứ nhất là 15 dm3?
BÀI TẬP

1/17/2018
3
CHƯƠNG II. THUYẾT ĐỘNG HỌC PHÂN TỬ (ĐHPT)
§1. NỘI DUNG THUYẾT ĐHPT-PHƯƠNG TRÌNH CƠ BẢN CỦA THUYẾT
ĐHPT.
§2. NỘI NĂNG KHÍ LÍ TƯỞNG.
§3. ĐỊNH LUẬT PHÂN BỐ BÔNZMAN.
13
§ 1. NỘI DUNG THUYẾT ĐỘNG HỌC PHÂN TỬ.
Dựa trên cơ sở cấu tạo phân tử và sự chuyển động hỗn loạn không ngừng của phân tử => thuyết động
học phân tử:
1. Các chất khí có cấu tạo gián đoạn gồm một số rất lớn các phân tử.
2. Các phân tử luôn chuyển động hỗn loạn không ngừng. Khi chuyển động chúng va chạm vào nhau và va
chạm vào thành bình.
3. Cường độ chuyển động của các phân tử biểu hiện ở nhiệt độ của khối khí. Chuyển động phân tử càng
mạnh thì nhiệt độ càng cao. Nhiệt độ tuyệt đối của khối khí tỉ lệ với động năng tịnh tiến trung bình của
phân tử.
4. Kích thước phân tử rất nhỏ so với khoảng cách giữa chúng, trong nhiều trường hợp tính toán ta bỏ qua
kích thước phân tử và coi như một chất điểm.
5. Các phân tử không tương tác trừ lúc va chạm.Sự va chạm giữa các phân tử với nhau và với thành bình
tuân theo quy luật của va chạm đàn hồi.
Các giả thiết 3,4,5 chỉ đúng với khí lí tưởng => thuyết động học phân tử của khí lí tưởng.
14
1. Giá trị trung bình.
+ Phân tử khí trong khối khí luôn chuyển động hỗn loạn không ngừng => v(Wđ, K…)của các
phân tử rất khác nhau => lấy giá trị trung bình của vận tốc để đặc trưng cho chuyển động
của phân tử.
+Giả sử có nphân tử trong bình: n1-----------------v1; n2-----------------v2;
………………………….. nn-----------------vn
+Định nghĩa vận tốc trung bình:
15
§2. PHƯƠNG TRÌNH CƠ BẢN CỦA THUYẾT ĐHPT
n
vn
nvnvn
nn vnvn
vii
...
... ... 2211
21
2211
(2-1)
+ Tƣơng tự ta có trung bình của bình phƣơng vận tốc là: (2-2)
+ Chia cả tử và mẫu của vế phải pt (2-2 ) cho V => viết giá trị trung bình bình của bình phƣơng
qua mật độ phân tử:
o
ioi
n
vn
v
2
2
(2-3)
(n0và n0i là mật độ phân tử của khối khí và mật độ phân tử khí có vận tốc vi).
n
vn
vii
2
2
16
+ Xét một khối khí đơn nguyên tử trong bình có mật độ phân tử khí là n0:
Theo phƣơng Ox vuông góc với thành bình:
ptử chuyển động với vận tốc v1x có mật độ: n01
ptử chuyển động với vận tốc v2x có mật độ: n02
………………………………..
ptử chuyển động với vận tốc vnx có mật độ: n0n
(n0= n01 + n02 +…+ n0n)
+ Xét một diện tích Δs nhỏ (coi là phẳng) => sau Δt số phân tử có vận tốc v1x có khả năng đến
đập vào Δs là:
01 1
1
2x
n n v s t
a. Lập phƣơng trình.
(Do các ptử chuyển động nhiệt hỗn loạn nên số phân tử đập vào diện tích Δs chỉ bằng ½ tổng số
các ptử có vận tốc v1x)
2. Phương trình cơ bản của thuyết động học phân tử
17
+ Độ biến thiên động lƣợng của các phân tử có v1x đến đập vào Δs là:
tsmvnmvtsvnktsvnK xxxx 2
1011101110112.
2
1
.
2
1
+ Độ biến thiên động lƣợng tổng cộng của các phân tử có vận tốc theo phƣơng Ox khi
đập vào Δs là:
(
m:
khối lƣợng của một phân tử khí)
iixi
iitsmvnKK 2
0
+ Theo định lý động lƣợng lực tác dụng lên Δs:
iixismvn
t
K
F2
0
iiximvn
s
F
P2
0
+ Ta có:
2 2 2
0 0 0i ix x x
in v n v P n mv
o
ioi
n
vn
v
2
2
18
2222 zyx vvvv
2222 zyx vvvv
+ Do tính chuyển động hỗn loạn không phƣơng ƣu tiên nên:
2
222
3
x y z v
vvv
+ Vậy áp suất tác dụng lên thành bình là:
2
0
2
02
1
3
2
3
1vmnvmnP
+ Do các phân tử chuyển động theo mọi phƣơng:
+ Gọi động năng trung bình của 1 phân tử khí là:
2
2
1vmWđ
đ
WnP 0
3
2
+ Ta có phƣơng trình cơ bản của thuyết động học phân tử là:

1/17/2018
4
b. Hệ quả.
*) Hệ quả 1:
+ Động năng tịnh tiến trung bình của phân tử tỉ lệ với nhiệt độ tuyệt
đối:
Từ hai phương trình
19
0
00
23 3 3
32 2 2
đ
đ
P n W P RT RT
Wn Vn N
PV RT
+ Đặt (k = 1,38.10-23J/độ) – hs Bônzman:
NRk /
kTWđ2
3
Biểu thức đn trên cho phân tử có cấu tạo đơn nguyên tử => coi pt nhƣ chất
điểm và nó chỉ chuyển động tịnh tiến .
20
*) Hệ quả 2:
(2-10)
+Nhận xét: nếu ở cùng T và P=> các chất khí có cùng n0.Ở đktc mọi chất
khí đều có mật độ pt khí (số Lôsmit) là:
+ Từ 2 phƣơng trình:
kT
P
W
P
n
kTW
WnP
đ
đ
đ
2
3
2
3
3
2
0
0
25
23
5
0
0
010.678,2
273.10.38,1 10.013,1
kT
P
n
(phân tử/m3)
21
+Vận tốc toàn phƣơng trung bình (còn gọi là vận tốc chuyển động nhiệt):
2
vvtp
(2-11)
+ Từ 2 phƣơng trình:
m
kT
m
W
v
kTW
vm
Wđ
đ
đ3
2
2
322
2
mà
mN
N
R
k
(2-12)
*)
Hệ quả 3:
RT
vv
RT
vtp 33 22
ta đƣợc:
1. Nội năng của một vật.
+ Nội năng là phần năng lượng tương ứng với chuyển động bên trong
vật gồm:
Động năng chuyển động nhiệt hỗn loạn của các pt
Thế năng tương tác các phân tử
Năng lượng dao đông các pt nhưng rất nhỏ ta có thể bỏ qua
+ Với khí lí tưởng các phân tử coi như không tương tác =>
22
đ
WU
+ Để tính U =>tính , nếu phân tử chỉ cđtt thì đntttb bằng .
Nhƣng thực tế phân tử còn có chuyển động quay do đó
=> Động năng trung bình lớn hơn động năng tịnh tiến trung bình.
đ
W
kTWđ2
3
§3. NỘI NĂNG KHÍ LÍ TƯỞNG.
2. Định luật phân bố đều năng lượng theo bậc tự do
a. Bậc tự do.
Bậc tự do là số tọa độ độc lập cần thiết để xác định vị trí của một vật
trong không gian.
•Với phân tử khí đơn nguyên tử => i=3
•Với phân tử cấu tạo 2 nguyên tử => i=5
•Với phân tử cấu tạo 3 nguyên tử => i=6
23
24
+
Nếu coi phân tử chỉ chuyển động tịnh tiến thì động năng trung bình cũng
chính là động năng tịnh tiến trung bình
.
222
22
1
2
1
2
1
2
1
2
3zyxđvmvmvmvmkTW
+ Do cđ hỗn loạn không phƣơng ƣu tiên nên động năng đƣợc phân bố đều
theo bậc tự do, mỗi bậc tự do ứng với năng lƣợng bằng . Măcxoen suy rộng
kết quả trên và đƣa ra đl sau:
Động năng trung bình của phân tử đƣợc phân
bố đều cho các bậc tự do và năng lƣợng ứng với mỗi bậc tự do là
:
kT
2
1
kT
2
1
+ Phân tử khí có i bậc tự đó thì:
kT
i
Wđ2
b. Đl phân bố đều năng lƣợng theo bậc tự do.

1/17/2018
5
3. Nội năng của khí lí tưởng.
+ Gọi U0là nội năng của 1kmol khí lí tưởng ta có:
25
RT
i
KT
i
NU 22
0
(3-13)
+ Với khối khí có khối lƣợng m thì nội năng U là:
RT
im
UU
m
U
m
U
U2
0
0
(3-14)
+ Vậy nội năng của khí lí tƣởng chỉ phụ thuộc vào nhiệt độ do
đó độ biến thiên nội năng của khí lí tƣởng là:
TR
im
U 2
1. Công thức khí áp.
26
+ Xét hai điểm có (z; p) và (z+dz;
p+dp) => (S = 1m2); theo
phƣơng trình trạng thái =>
gdzdp
RT
p
dz
RT
g
p
dp
gdz
RT
p
dp
+ Các phân tử khí chuyển động hỗn loạn => các phân tử khí có
xu hƣớng phân bố đồng đều.Do phân tử bị trọng trƣờng trái đất
hút => phân tử khí bị hút xuống => áp suất thay đổi theo chiều
cao.
§4. ĐỊNH LuẬT PHÂN BỐ BÔNZMAN
27
+ Lấy tích phân 2 vế ta đƣợc
z
RT
g
pzp
dz
RT
g
p
dp z
zp
p
)0( )(
ln
0
)(
)0(
+ Lấy e mũ hai vế đƣợc công thức khí áp:
RT
gz
epzp
)0()(
(3-15)
Trong đó p(z) và p(0) là áp suất ở độ cao z và ở mặt đất.Vậy áp
suất giảm theo chiều cao.
2. Định luật phân bố Bôzman.
28
+Vì áp suất tỉ lệ với mật độ phân tử khí nên nếu gọi n0(z) và n0(0) là mật độ
phân tử khí ởđộ cao z và ở mặt đất ta có
RT
gz
RT
gz enzne
nzn
pzp
).0()(
)0( )(
)0( )( 00
0
0
(3-16)
+ Thay µ= m.N (với mlà khối lƣợng của 1 phân tử khí )và R = k.N vào (3-16)
đƣợc :
kT
mgz
enzn
).0()( 00
(3-17)
+ Vì mgz là thế năng của phân tử khí trong trọng trƣờng trái đất ở độ cao z và:
n0(z)= n0(wt) là mật độ phân tử ở vị trí có thế năng wt
n0(0) là mật độ phân tử ở vị trí có thế năng wt= 0
29
kT
w
t
t
enwn
).0()( 00
(3-18)
+Nếu gọi n01, n02 là mật độ phân tử khí ởvị trí thế năng tƣơng ứng wt1 và wt2
từ (3-18)ta có thể viết
kTww tt
e
n
n12
02
01
(3-19)
Vậy khi chất khí đặt trong một trƣờng lực thế chỗ nào thế năng càng nhỏ thì
mật độ phân tử càng lớn và ngƣợc lại
Công thức (3-18)đƣợc gọi là định luật Bônzman.
30
Bài 2-1. Có một khối khí Heli đựng trong một bình kín giãn nở kém có thể tích V = 2 lít ở nhiệt độ
20ºC và áp suất 105N/m2. Tìm:
a) Vận tốc toàn phƣơng trung bình của các phân tử Heli ở trạng thái cuối?
b) Áp suất của khối khí sau khi cung cấp nhiệt?
c) Khối lƣợng riêng của khối khí?
d) Năng lƣợng chuyển động nhiệt của các phân tử sau khi cung cấp nhiệt cho khối khí?
Bài 2-2. Một khối khí Oxy chứa trong bình 10 lít, áp suất trong bình là 10-11 mmHg, nhiệt độ của
khối khí là 10ºC. Hãy xác định:
a) Động năng trung bình và động năng tịnh tiến trung bình của mỗi phân tử khí?
b) Tính mật độ các phân tử khí trong bình?
c) Nén đẳng áp để mật độ các phân tử khí tăng gấp đôi thì nhiệt độ của khối khí bằng
bao nhiêu?
d) Tính nội năng trƣớc và sau khi nén?
Bài 2-3. Trong một bình thể tích 2 lít, chứa 10g khí ôxy ởáp suất 860mmHg. Tìm:
a) Vận tốc toàn phƣơng trung bình của phân tử khí?
b) Số phân tử khí chứa trong bình?
c) Khối lƣợng riêng của khối khí?
Bài 2-4. Tổng động năng tịnh tiến trung bình của các phân tử khí Nitơ chứa trong một khí cầu thể
tích 0,02 m3bằng 5.103Jvà vận tốc toàn phƣơng trung bình của một phân tử khí đó là 2.103m/s.
a) Tìm khối lƣợng khí Nitơ chứa trong khí cầu?
b) Áp suất khí tác dụng lên thành khí cầu?
BÀI TẬP

















![Tài liệu ôn thi cuối kì môn Tính toán và mô phỏng vật liệu [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260416/hoabattu2026/135x160/28131776394772.jpg)








