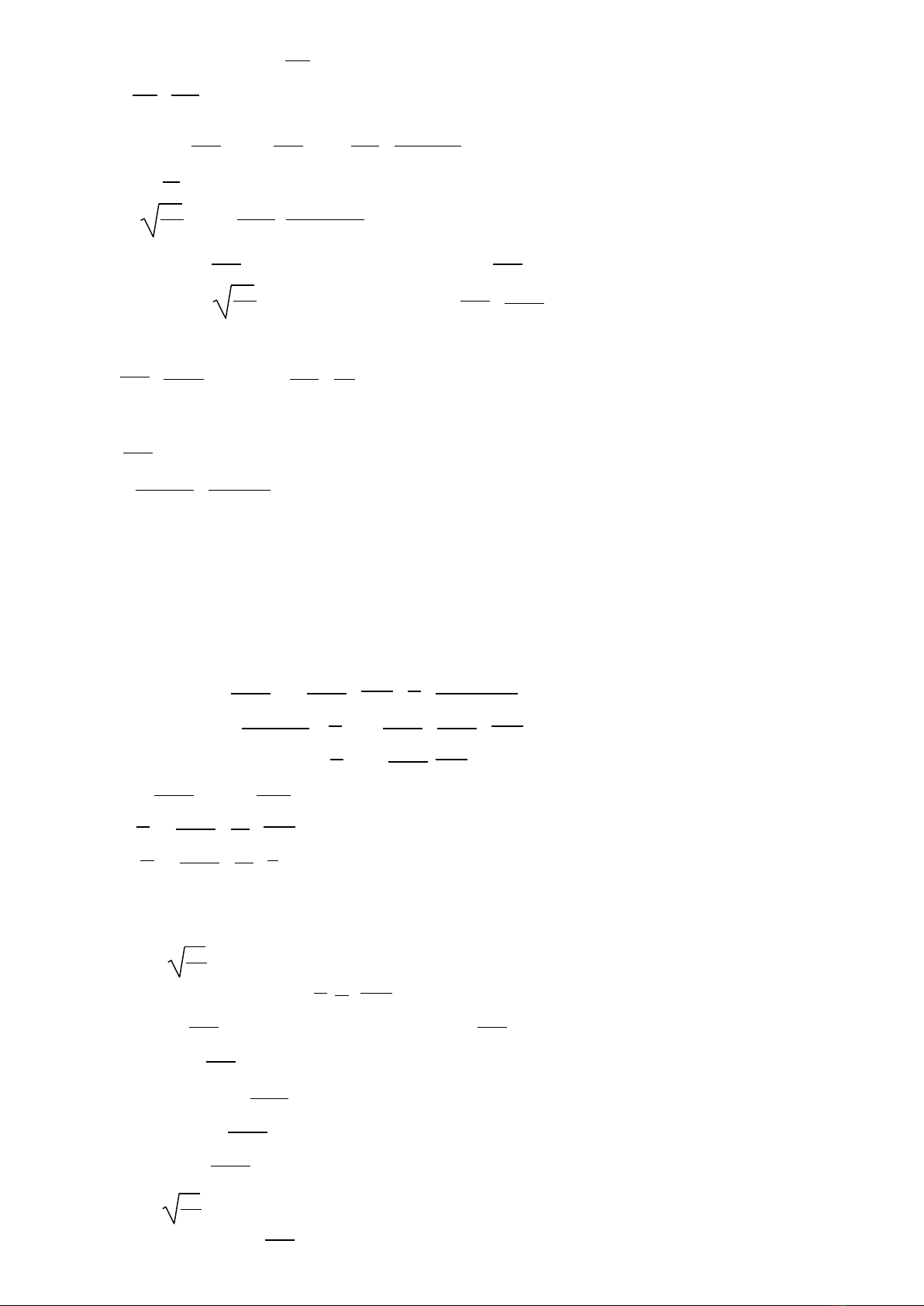
2.8. 1) Áp dụng qui tắc đương lượng: 125
M = 41,2 0,09 103 M = 337,1.
Co = 125
337 1000
50 = 0,0742M
2) Khi thêm 8,24 ml (chưa đến đTĐ)
Áp dụng: h = K1 P
P K = h P
1 P với P = CV
CoVo
= 009 824
00742 50 = 0,1998 0,2
K = 104,3 02
08 = 1,25 105.
2) h = WK
C' với C' = CCo
C + Co
=009 00742
009 + 00742 = 0,04067 pH = 8,75.
2.9. V = 10 ml h = K.1 P
P pH = 4,35. V = 12,45 ml h = K.1 P
P pH = 6,15.
V = 12,5 ml h2 = WK
C' pH = 8,14 V = 13 ml h = W
P 1 V + Vo
VoCo
pH = 11,12
2.10. TN1: Cho 20 ml dung dịch NaOH C (M) vào 30 ml CH3-COOH Co (M) đạt pH = 10,5 lớn hơn pHTĐ = 8,74, nghĩa là dung dịch tương ứng
với sau điểm tương đương, ta có:
h = W
P 1 V + Vo
VoCo
= 105 với P = CV
CoVo
= 2C
3Co
Sau khi thay số 2C 3Co = 1,58 103 ()
TN2: Thêm tiếp 0,05 mmol HCl, đạt pH = 6 < 8,74 trước điểm tương đương. Ta có:
h = K.1 P
P = 106 P = 0,94556
Với P = CV 005
CoVo
= 20C 005
30Co
= 0,094556 2C 2,837Co = 5 103 ()
Giải () và () C = 3,22 102M và Co = 2,098 102M.
2.11. 1) NH4
+
NH3 + H+ K = 109,26
0,2--------------------0,01
0,2x----------------0,01+x
Áp dụng ĐL tác dụng khối lượng với x 0,01 x = 107,96 0,01.
Vật h = [H+] = 0,01 pH = 2.
2) Gọi NaOH (C,V) và HCl (Co1,Vo) và
4
NH
(Co2,Vo)
Từ phương trình trung hoà điện: [Na+] + [H+] + [NH4] = [OH] + [Cl]
CV
V + Vo
+ h + Co2Vo
V + Vo
h
h + K = W
h + Co1Vo + Co2Vo
V + Vo
CV Co1Vo
V + Vo
= (W
h h) + Co2Vo
V + Vo
Co2Vo
V + Vo
h
h + K
= (W
h h) + Co2Vo
V + Vo
K
h + K
Nhân 2 vế cho V + Vo
CoVo
và đặt P = CV
Co1Vo
, ta được:
P 1 = (W
h h)V + Vo
CoVo
+ Co2
Co1
K
h + K
q = P 1 = (W
h h)V + Vo
CoVo
+ Co2
Co1
K
h với K h, thay số vào q = 1,74 102 hay 1,74%.
3) Áp dụng công thức q khi tính BNCĐ, chú ý môi trường (axit)
Đầu BNCĐ: 150h2 0,001h 1,099.108 = 0 h = 1,25 105 pH = 4,91.
Cuối BNCĐ: 150h2 + 0,001h 1,099.108 = 0 h = 5,85 106 pH = 5,23.
2.12. V = 0 ml h = WK
Co
= 1010,83 không hỏ hơn nhiều so K
Nếu giải phương trình bậc 2 suy ra từ : 1 = W
h1
Co
+ K
K + h pH = 10,82.
V = 10 ml h = K. P
1 P pH = 9,44 V = 20 ml h = K. P
1 P pH = 8,66.
V = 24,95 ml h = K. P
1 P pH = 6,56.
V = 25 ml h2 = KC' với C' = CCo
C + Co
= 0,0125M pH = 5,58.
V = 25,02 ml h = (P 1) CoVo
V + Vo
pH = 5
V = 30 ml h = (P 1) CoVo
V + Vo
pH = 2,64.
2.13. 1) P = 0 h = WK
Co
= 1011,22 với Co = 0,15M
Chuẩn độ 50% , P = 0,5 h = K. P
1 P pH = 9,26

Khi P = 1 h2 = KC' với C' = CCo
C + Co
= 0,09375M pH = 5,14.
2) Áp dụng công thức sai số q = (h W
h) C + Co
CCo
K
K + h với h W
h và K
q = 0,1% < 0,2% vậy MD dùng được.
2.14. 1) V = 10 ml đTĐ 1 h2 = K1K2C'
K1 + C' với C' = CCo
C + Co
= 2
3102M pH = 4,86.
V = 20 ml đTD 2 h2 = K2K3 + WK2
C'' với C'' = CCo
C + 2Co
= 5 103M pH = 9,41.
2) Khi dừng pH = 4,4 áp dụng qI sai số: 1,12%
3) Khi dừng pH = 9 áp dụng qII sai số: 0,7%.
2.15. Từ phương trình đường chuẩn độ của axit 2 nấc: P 1 = (W
h h)V + Vo
CoVo
+ K1K2 h2
h2 + hK1 + K1K2
Chú ý rằng VTĐ1 = 25 ml và VTĐ2 = 50 ml.
Nếu V = 20 ml trước đTĐ 1 P 1 = hV + Vo
CoVo
+ h
h + K1
Với P = 0,8
Thay số vào K1 = 5,06 103
Nếu V = 50 tại đTĐ 2 P 2 = W
h C + 2Co
CCo
h
K2
Với P = 2
K2 = 2 106.
2.16. 1) Điều kiện K1/K2 104 không thoả mãn không CĐ riêng được.
Do đó CĐ luôn đến nấc 2: h2 = WK2 C + 2Co
CCo
pH = 8,34.
2) h = K2 2 P
P 1 = 106 P = 1,9817 vậy CĐ được 98% kể từ nấc 1.
2.17. Chuẩn độ đến pH = 4,4: CĐ đến nấc thứ 1 của H3PO4
[H+] + [Na+] = [Ac] + [H2PO4
] + [OH]
với h và W
h không đáng kể và [HPO4
] và [PO4
3] không đáng kể
Gọi C1: nồng độ mol của ax. Axetic và C2: nồng độ ax. H3PO4.
20 01
20 + 25 = K
K + h 25C1
20 + 45 + 25C2
20 + 25 thay K = 104,76 và h = 104,4
2 = 7,59C1 + 25C2 ()
Chuẩn độ đến pH = 9 CĐ đến nấc thứ 2:
[H+] + [Na+] = [Ac] + 2[HPO4
2] + [OH] với h, W
h không đáng kể
01 45
25 + 45 = 25C1
25 + 45 + 2 25C2
70 4,5 = 25C1 + 50C2 ()
Giải hệ () và () C1 = 5,091 102M và C2 = 6,454 102M
2.18. 1) Tính được VTĐ1= 25 ml, VTĐ2 = 50 ml.
V = 20 ml h = K2 P
1 P với P = CV
CoVo
= 0,8 h = 109,73
V = 25 ml h2 = W + K2C'
1 + K1
1C' với C' = CCo
C + Co
h = 108,34.
V = 30 ml h = K1 P 1
2 P với P = 1,2 h = 106,95.
V = 50 ml C''= 5 103 < L = 3 102M
áp dụng: P 2 = h C + 2Co
CCo
K1
h + K1
với P = CV
CoVo
= 2 và h K1
h = 104,325.
2) q = (h W
h)C + Co
CCo
+ h2 K1K2
h2 + K1h + K1K2
= 1,76 102 hay 1,76%.
2.19. Lúc PP đổi màu: Sđlg NaOH + Sđlg Na2CO3 = Sđlg HCl
1,2( x
1001
40 + y
100 1
106) = 30 0,5 103 ()
Lúc MD đổi màu: Sđlg NaOH + Sđlg Na2CO3 = Sđlg HCl
1,2( x
1001
40 + y
100 1
53) = 35 0,5 103 ()
Giải hệ x = 41,67% và y = 22,08%.

2.20. Nồng độ dd B (NaOH): C' = 31 02
25 = 0,248M
1) Gọi x: số mol NaHCO3 và y số mol Na2CO3 (trong 25 mol dung dịch A)
Số mol HCl tác dụng với 25 ml dd A: x + 2y = 48 0,2 103 = 0,0096 ()
Sau khi thêm 50 ml dung dịch B vào 25 ml dung dịch A rồi trung hoà NaOH dư bằng HCl:
Số mol NaOH = x + số mol HCl
50 0,248 103 = x + (25 0,2 103) x = 7,4 103 mol NaHCO3 %NaHCO3 = 82,88%
Từ () y = 1,1 103 mol Na2CO3 %Na2CO3 = 15,54%.
2) Ta có thể xem Na2CO3 (8,5 mmol) đã bị chuẩn độ bằng axit đến dd A: gồm Na2CO3 (1,1 mmol và NaHCO3 7,4 mmol)
Lúc đó P = CV
CoVo
= số mmol NaHCO3
tổng số mmol Na2CO3 ban đầu = 74
85 = 0,87
Ap dụng h = K2 P
1 P = 109,5 pH = 9,5
3) Nếu CĐ 25 ml dung dịch A bằng HCl đến PP chuyển màu (đến NaHCO3):
Số đlg Na2CO3 = Sđlg HCl 1,1 = V 0,2 V = 5,5 ml.
2.21. Nhận xét: ở pH = 7,21 h = 107,21 = K2 2 P
P 1 P = 1,5
(nghĩa là CĐ đến ½ nấc 2 của H3PO4)
Khi pH = 9,78 pK1 + pK2
2 = 9,765 CĐ đến vừa hết nấc 2 của H3PO4.
Thể tích NaOH CĐ được 1 nấc H3PO4: 5 2 = 10 ml.
Suy ra thể tích NaOH CĐ vừa hết H2SO4: 15 5 10 = 10 ml.
C (H3PO4) = 10 01
5 = 0,2M và C (H2SO4) = 01 10
5 2 = 0,1M.
Trung hoà hoàn toàn 5 ml dung dịch hỗn hợp H3PO4 và H2SO4 (nghĩa là đến nấc 3 H3PO4)
Ta có: V 0,1 = (0,1 2 5) + (0,2 3 5) V = 40 ml.
2.22. Số mol H3PO4: 0,025 0,4 = 0,01 mol. Số mol Na3PO4: 0,03 0,5 = 0,015 mol.
Xét tỉ lệ f = số mol H3PO4
số mol Na3PO4
= 0,667 0,5 < f < 2 , ta có phản ứng:
H3PO4 + 2Na3PO4 3Na2HPO4 2H3PO4 + Na3PO4 3NaH2PO4
a-----------2a--------------------3a b-----------0,5b------------------1,5b
nH3PO4
= a + b = 0,02 và nNa3PO4
= 2a + 0,5b = 0,015 a = 002
3 và b = 001
3
nNa2HPO4
= 3a = 0,02 mol và nNaH2PO4
= 1,5b = 0,005 mol
Nếu CĐ đến MD chuyển màu cần V ml HCl: 0,02 = 0,1V V = 200 ml
Nếu CĐ đến PP chuyển màu cần V' ml NaOH: 0,005 = 0,1V' V' = 50 ml
3.1. 1) ETĐ = Eo
Fe + 5Eo
Mn
6 = 1,37V
2) Dừng CĐ ở E = 0,83 V < 1,37 V trước đTĐ, thiếu CĐ
Dùng E = Eo
Fe + 0,059lg P
1 P P = 0,99714 q = P 1 = 0,00286 hay 0,286%
3.2. 1) CĐ thiếu 0,2%: E = Eo
U + 0059
2lg P
1 P vơi P = 0,998 E = 0,414 V
CĐ đến đTĐ: E = 2Eo
U + Eo
Ce
3 = 0,703V
CĐ đến quá 0,2% : E = Eo
Ce + 0,059 lg(1 P) với P = 1,002 E = 1,280 V
2) Dừng ở thế 0,42 V < 0,703V trước đTĐ: E = Eo
U + 0059
2lg P
1 P P = 0,9988
P = NV
NoVo
= 0,9988 V = 39,95 ml.
Dừng ở thế 1,27V > 0,703 V sau đTĐ: E = Eo
Ce + 0,059 lg(1 P) P = 1,0013
P = NV
NoVo
= 1,0013 V = 40,052 ml
3.3. 1) Từ 2 bán phản ứng: Fe3+ + 1e Fe2+ K1 = 10 EFe/0,059
Ti3+ + H2O e TiO2+ + 2H+ K2 = 10ETi/0059
Phản ứng CĐ có K = K1K2 = 1011,36
2) Tính VTĐ = 50 ml và ETĐ = Eo
Fe + Eo
Ti
2 = 0,435V
Theo E = Eo
Fe + 0,059lg[Fe3+]
[Fe2+] vơi [Fe2+] = 005 20
20 + 50 = 1
70 thay vào biểu thức E [Fe3+] = 107,52
3) Dừng ở E = 0,330 V < ETĐ quá CĐ, ta dùng E = Eo
Ti + 0,059lg 1
P 1 P 1 và V 50 ml
3.4. ETĐ = 144 + 068
2 = 1,06V
* q = 0,001 P = 0,999

Áp dụng E =
o
Fe
E
+ 0,059log[Fe3+]
[Fe2+] =
o
Fe
E
+ 0,059log P
1 P
= 0,857 V
* q = +0,001 P = 1,001
Áp dụng E =
o
Ce
E
+ 0,059log(P 1) = 1,263v
BNCĐ: 0,857 1,263V: Chọn Feroin chuyển màu rõ ở thế 1,12V từ đỏ sang xanh nhạt.
3.5. Chuẩn độ được 50% (P = 0,5): E =
o
Sn
E
+ 0059
2log P
1 P
= 0,15V
Chuẩn độ được 90% (P = 0,9): E =
o
Sn
E
+ 0059
2log P
1 P
= 0,178V
CĐ được 100% (P = 1): ETĐ =
oo
Fe Sn
E 2E
3
= 0,3567V
CĐ đến 110% (P = 1,1): E =
o
Fe
E
+ 0,059log(P 1) = 0,711V.
3.6. Au3+ + 3I
AuI + I2
a----------------------------a mol
2Cu2+ + 4I
2CuI + I2
b------------------------------0,5b mol
I2 + 2S2O3
2
2I + S4O6
2
Số mol I2 = a + 0,5b = ½ Số mol S2O3
2 = 0,5(0,076132,7103) = 1,2442.103
Hay : 2a + b = 2,4884.103 ()
Ngoài ra khối lượng mẫu hợp kim: 197a + 64b = 0,1676 ()
a = 1,2090.104 mol và b = 2,2466.103 mol
%Au = 14,221%.
3.7. Gọi x: % khối lượng H2C2O4.2H2O (M = 126)
y: % khối lượng KHC2O4.H2O (M = 146)
Với phép chuẩn độ axit bazơ: Sđlg NaOH = Sđlg H2C2O4.2H2O + Sđlg KHC2O4.H2O
43,1 0,125.103 = ( x
10012
126
2
) + ( y
10012
146) ()
Với phép chuẩn độ oxi hóa khử:Sđlg KMnO4 = Sđlg H2C2O4.2H2O + Sđlg KHC2O4.H2O
43,1 0,125.103 = ( x
10012
126
2
) + ( y
10012
146
2
) ()
Giải hệ () và () x = 14,37 và y = 81,57.
3.8. Phản ứng oxi hóa Cr3+ thành
2
27
Cr O
:
2
28
SO
+ 2e
2
2
4
SO
2Cr3+
+ 7H2O 6e
2
27
Cr O
+14H+
3
2
28
SO
+ 2Cr3+ + 7H2O
6
2
4
SO
+
2
27
Cr O
+ 14H+
Sđlg Cr3+ = Sđlg
2
27
Cr O
= Sđlg Fe2+ (lấy dư) Số đlg KMnO4 (CĐ FeSO4 thừa)
(x
100 2
52
3
)20
100 = (35 15) 0,009 5 105.
x = 3,9%.
3.9. Gọi a: số mol BaCO3 = số mol Ba2+
2Ba2+
K2Cr2O7 2BaCrO4
H+
2Ba2+ +
2
27
Cr O
a--------------------------------------------------0,5a
2
27
Cr O
+ 6I + 14H+
2Cr3+ + 3I2 + 7H2O
0,5a-------------------------------------1,5a
I2 + 2
2
23
SO
2I +
2
46
SO
1,5a-----3a 3a = 0,1013 38,68 103
a = 1,306 103 %Ba = 1306 103 137 100%
0512
= 34,95%
3.10. Gọi x: số mol PbO và y: số mol PbO2
PbO + H2C2O4 PbC2O4 + H2O (1)
x----------x-----------------x
PbO2 + 2H2C2O4 PbC2O4 + 2CO2 + 2H2O (2)
y----------2y--------------- ----y
5H2C2O4 + 2KMnO4 + 3H2SO4 2MnSO4 + 10CO2 + K2SO4 + 8H2O (3)
Số mol H2C2O4 tham gia (1) và (2): x + 2y = 20.0,25.103 10.0,04.103.5
2
Hay x + 2y = 4.103 ()
Khi hòa tan kết tủa PbC2O4 ta thu được H2C2O4 số mol:
x + y = 5
2 30.0,04.103 = 3.103 ()
Giải hệ () và () x = 2.103 và y = 103 mol

%PbO = 2.103.223 100%
1234
= 36,14%
%PbO2 = 103.239 100%
1234
= 19,36%.
3.11. Pb2O3 + 6HCl 2PbCl2 + Cl2 + 3H2O
x-----------------------------------x
Pb3O4 + 8HCl 3PbCl2 + Cl2 + 4H2O
y-----------------------------------y
Pb2O3 2Pb2+ 2PbCrO4
2
27
Cr O
x---------------------------------------------------------x
Pb3O4 3Pb3+ 3PbCrO4 1,5
2
27
Cr O
y------------------------------------------------------------1,5y
2
27
Cr O
+ 6I + 14H+
2Cr3+ + 3I2 + 7H2O
(x + 1,5y)---------------------------(3x + 4,5y)
I2 + 2
2
23
SO
2I +
2
46
SO
Số mol
2
23
SO
= 2.Số mol I2 = 2(3x + 4,5y) = 35,04.103.0,2
Hay: 6x + 9y = 7,008.103 ()
Ngoài ra: Cl2 + 2I
I2 + 2Cl
(x + y)---------(x + y)
Số mol
2
23
SO
= 2(x + y) = 9,36.103.0,2
Hay: x + y = 9,36.104 ()
Giải hệ () và () x = 4,72.104 và y = 4,64.104
%Pb2O3 = 462x
06
100% = 36,33%
%Pb3O4 = 685y
06
100% = 52,96%.
3.12. Tính được VTĐ = 100 ml
Đầu BNCĐ: q = 0,001 và Vđ = 99,9 ml
E =
o
Fe
E
+ 0,059log[Fe3+]
[Fe2+] Với [Fe3+] = 001 999
1999 + 001 100
1999 = 1999
1999
Fe3+ sinh ra Fe3+ có sẵn
Và [Fe2+] = 001 01
1999 = 0001
1999
E = 0,68 + 0,059log1999
0001
= 0,875V
Cuối BNCĐ: Vc = 100,1 ml và P = 1,001
E =
o
Ce
E
+ 0,059log(P 1) = 1,263V.
3.13. Nếu cho qua cột khử Ag (trong dd HCl 1M), xảy ra:
Fe3+ + Ag + Cl
Fe2+ + AgCl
VO2
+ + Ag + 2H+ + Cl
VO2+ + H2O
Khi chuẩn độ dung dịch thu được bằng Ce4+ thì Fe2+ Fe3+ và VO2+ VO2
+
Số mol Ce4+ = Số mol Fe2+ + Số mol VO2+
8,86.103.0,2 = x + y
Hay x + y = 1.772.103 ()
Nếu cho qua cột khử Zn (H2SO4 1N) :
2Fe3+ + Zn
2Fe2+ + Zn2+
2VO2
+ + 3Zn + 8H+
2V2+ + 3Zn2+ + 4H2O
Chuẩn độ bằng Ce4+ thì Fe2+ Fe3+ và V2+ VO2
+
Số đlg Ce4+ = Số đlgFe2+ + Sđlg VO2
+
22.103.0,2 = x + 3y ()
Giải hệ () và () cho x = 4,58.104 và y = 1,314.103
%Fe = 200
50 458 104 56 100%
05 = 20,52%
%V = 200
50 1314 103 51 100%
05 = 53,6%.
3.14. Phản ứng: 6Fe2+ + Cr2O2
7 + 14H+
6Fe3+ + 2Cr3+ + 7H2O
Ta có: ETD = Eo
Fe + 6Eo
Cr
7 + 0059
7lg[Fe3+]
[Fe2+][Cr2O7
2-]
[Cr3+]2 (chấp nhận [H+] = 1)
Tại đTĐ: 6[Cr2O2
7] + 3[Cr3+] = [Fe3+] + [Fe2+] mà 3[Cr3+] = [Fe3+]
Nên suy ra: 6[Cr2O2
7] = [Fe2+], thay vào biểu thức sau log:
[Fe3+]
[Fe2+][Cr2O7
2-]
[Cr3+]2 = 3[Cr3+]
6[Cr2O2
7]
[Cr2O7
2-]
[Cr3+]2 = 1
2[Cr3+]
Vậy ETĐ = Eo
Fe + 6Eo
Cr
7 + 0059
7lg 1
2[Cr3+] = 1
7(Eo
Fe + 6Eo
Cr 0018lg[Cr3+])







![Đề cương ôn tập Hóa phân tích [năm] chi tiết, chuẩn nhất](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250629/sonvu86/135x160/6131751251868.jpg)












![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



