Đ
Đ
Đ
ĐẠ
Ạ
Ạ
ẠI H
I H
I H
I HỌ
Ọ
Ọ
ỌC N
C N
C N
C NÔ
Ô
Ô
ÔNG L
NG L
NG L
NG LÂ
Â
Â
ÂM TP HCM
M TP HCM
M TP HCM
M TP HCM
H
H
H
HÓ
Ó
Ó
ÓA H
A H
A H
A HỌ
Ọ
Ọ
ỌC
C
C
C
Đ
Đ
Đ
ĐẠ
Ạ
Ạ
ẠI C
I C
I C
I CƯƠ
ƯƠ
ƯƠ
ƯƠNG
NG
NG
NG
Th
Th
Th
Thạ
ạ
ạ
ạc
c
c
c
s
s
s
sỹ
ỹ
ỹ
ỹ
Nguyễn Vinh Lan
NỘI DUNG
M
M
M
Mô
ô
ô
ôn
n
n
n
H
H
H
Hó
ó
ó
óa
a
a
a
đ
đ
đ
đạ
ạ
ạ
ại
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng (
(
(
(
M
M
M
Mã
ã
ã
ã
m
m
m
mô
ô
ô
ôn
n
n
n
h
h
h
họ
ọ
ọ
ọc
c
c
c
202301
202301
202301
202301
)
)
)
)
l
l
l
là
à
à
à
m
m
m
mô
ô
ô
ôn
n
n
n
h
h
h
họ
ọ
ọ
ọc
c
c
c
3
3
3
3 t
t
t
tí
í
í
ín
n
n
n
ch
ch
ch
chỉ
ỉ
ỉ
ỉ
( 45
( 45
( 45
( 45 ti
ti
ti
tiế
ế
ế
ết
t
t
t )
)
)
)
g
g
g
gồ
ồ
ồ
ồm
m
m
m 2
2
2
2 ph
ph
ph
phầ
ầ
ầ
ần
n
n
n:
:
:
:
�Ph
Ph
Ph
Phầ
ầ
ầ
ần
n
n
n 1:
1:
1:
1: H
H
H
Hó
ó
ó
óa
a
a
a
Đ
Đ
Đ
Đạ
ạ
ạ
ại
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng ( 22,5
( 22,5
( 22,5
( 22,5 ti
ti
ti
tiế
ế
ế
ết
t
t
t )
)
)
)
�Ph
Ph
Ph
Phầ
ầ
ầ
ần
n
n
n 2:
2:
2:
2: H
H
H
Hó
ó
ó
óa
a
a
a
H
H
H
Hữ
ữ
ữ
ữu
u
u
u
c
c
c
cơ
ơ
ơ
ơ ( 22,5
( 22,5
( 22,5
( 22,5 ti
ti
ti
tiế
ế
ế
ết
t
t
t )
)
)
)
T
T
T
TÀ
À
À
ÀI LI
I LI
I LI
I LIỆ
Ệ
Ệ
ỆU THAM KH
U THAM KH
U THAM KH
U THAM KHẢ
Ả
Ả
ẢO
O
O
O
1-
1-
1-
1-
H
H
H
Hó
ó
ó
óa
a
a
a
Đ
Đ
Đ
Đạ
ạ
ạ
ạ
i
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng
,
,
,
,
T
T
T
Tà
à
à
à
i
i
i
i
li
li
li
li
ệ
ệ
ệ
ệu
u
u
u
n
n
n
nộ
ộ
ộ
ộ
i
i
i
i
b
b
b
bộ
ộ
ộ
ộ, 2010
, 2010
, 2010
, 2010*
*
*
*
T
T
T
Tậ
ậ
ậ
ập
p
p
p 1-
1-
1-
1- Ph
Ph
Ph
Phầ
ầ
ầ
ần
n
n
n
Đ
Đ
Đ
Đạ
ạ
ạ
ạ
i
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng
,
,
,
,
Nguy
Nguy
Nguy
Nguyễ
ễ
ễ
ễn
n
n
n
V
V
V
Vă
ă
ă
ăn
n
n
n
Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
,
,
,
,
L
L
L
Lâ
â
â
âm
m
m
m
Ng
Ng
Ng
Ngọ
ọ
ọ
ọc
c
c
c
Á
Á
Á
Ánh
nh
nh
nh
,
,
,
,
…
…
…
…
T
T
T
Tậ
ậ
ậ
ập
p
p
p 2-
2-
2-
2- Ph
Ph
Ph
Phầ
ầ
ầ
ần
n
n
n
H
H
H
Hữ
ữ
ữ
ữu
u
u
u
c
c
c
cơ
ơ
ơ
ơ
,
,
,
,
Nguy
Nguy
Nguy
Nguyễ
ễ
ễ
ễn
n
n
n
Vinh
Vinh
Vinh
Vinh
Lan
Lan
Lan
Lan
,
,
,
,
Đ
Đ
Đ
Đinh
inh
inh
inh
Thanh
Thanh
Thanh
Thanh
T
T
T
Tù
ù
ù
ùng
ng
ng
ng
,
,
,
,
…
…
…
…
2-
2-
2-
2-
H
H
H
Hó
ó
ó
óa
a
a
a
Đ
Đ
Đ
Đạ
ạ
ạ
ạ
i
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng
,
,
,
,
Nguy
Nguy
Nguy
Nguyễ
ễ
ễ
ễn
n
n
n
Đ
Đ
Đ
Đ
ì
ì
ì
ì
nh
nh
nh
nh Chi, NXB
Chi, NXB
Chi, NXB
Chi, NXB Gi
Gi
Gi
Giá
á
á
áo
o
o
o
d
d
d
dụ
ụ
ụ
ục
c
c
c, 1997
, 1997
, 1997
, 1997
3-
3-
3-
3-
H
H
H
Hó
ó
ó
óa
a
a
a
H
H
H
Họ
ọ
ọ
ọc
c
c
c
H
H
H
Hữ
ữ
ữ
ữu
u
u
u
c
c
c
cơ
ơ
ơ
ơ
,
,
,
,
Đ
Đ
Đ
Đặ
ặ
ặ
ặng
ng
ng
ng
Nh
Nh
Nh
Như
ư
ư
ư
T
T
T
Tạ
ạ
ạ
ạ
i
i
i
i,
,
,
,
Ng
Ng
Ng
Ngô
ô
ô
ô
Th
Th
Th
Th
ị
ị
ị
ị
Thu
Thu
Thu
Thuậ
ậ
ậ
ận
n
n
n
,
,
,
,
NXB
NXB
NXB
NXB Gi
Gi
Gi
Giá
á
á
áo
o
o
o
d
d
d
dụ
ụ
ụ
ục
c
c
c, 2010
, 2010
, 2010
, 2010
.
.
.
.
ĐÁ
ĐÁ
ĐÁ
ĐÁNH GI
NH GI
NH GI
NH GIÁ
Á
Á
Á M
M
M
MÔ
Ô
Ô
ÔN H
N H
N H
N HỌ
Ọ
Ọ
ỌC
C
C
C
� Kiểm tra giữa kỳ: 30% ( Điểm D1 )
� Thi học kỳ: 70% ( Điểm D2 )
Điểm môn học D = 0,3D1 + 0,7D2

H
H
H
HÓ
Ó
Ó
ÓA
A
A
A Đ
Đ
Đ
ĐẠ
Ạ
Ạ
ẠI C
I C
I C
I CƯƠ
ƯƠ
ƯƠ
ƯƠNG
NG
NG
NG
Ph
Ph
Ph
Phầ
ầ
ầ
ần
n
n
n 2
2
2
2
– H
H
H
HÓ
Ó
Ó
ÓA H
A H
A H
A HỮ
Ữ
Ữ
ỮU C
U C
U C
U CƠ
Ơ
Ơ
Ơ
N
N
N
Nộ
ộ
ộ
ộ
i
i
i
i
dung:
dung:
dung:
dung:
Gồm 7 chương
Chương I-
Đ
Đ
Đ
Đạ
ạ
ạ
ạ
i
i
i
i
c
c
c
cư
ư
ư
ươ
ơ
ơ
ơng
ng
ng
ng
v
v
v
về
ề
ề
ề
H
H
H
Hó
ó
ó
óa
a
a
a
h
h
h
hữ
ữ
ữ
ữu
u
u
u
c
c
c
cơ
ơ
ơ
ơ
Chương II-
Hidrocarbon
Hidrocarbon
Hidrocarbon
Hidrocarbon
Chương III-
D
D
D
Dẫ
ẫ
ẫ
ẫn
n
n
n
xu
xu
xu
xuấ
ấ
ấ
ất
t
t
t
hidroxi
hidroxi
hidroxi
hidroxi
c
c
c
củ
ủ
ủ
ủa
a
a
a
hidrocarbon
hidrocarbon
hidrocarbon
hidrocarbon
Chương IV-
H
H
H
Hợ
ợ
ợ
ợp
p
p
p
ch
ch
ch
chấ
ấ
ấ
ất
t
t
t carbonyl
carbonyl
carbonyl
carbonyl
Chương V-
Axit
Axit
Axit
Axit carboxylic
carboxylic
carboxylic
carboxylic v
v
v
và
à
à
à
d
d
d
dẫ
ẫ
ẫ
ẫn
n
n
n
xu
xu
xu
xuấ
ấ
ấ
ất
t
t
t
Chương VI-
H
H
H
Hợ
ợ
ợ
ợp
p
p
p
ch
ch
ch
chấ
ấ
ấ
ất
t
t
t
ch
ch
ch
chứ
ứ
ứ
ứa
a
a
a
nit
nit
nit
nitơ
ơ
ơ
ơ
Chương VII-
Gluxit
Gluxit
Gluxit
Gluxit
CH
CH
CH
CHƯƠ
ƯƠ
ƯƠ
ƯƠNG I
NG I
NG I
NG I
Đ
Đ
Đ
ĐẠ
Ạ
Ạ
ẠI C
I C
I C
I CƯƠ
ƯƠ
ƯƠ
ƯƠNG V
NG V
NG V
NG VỀ
Ề
Ề
Ề H
H
H
HÓ
Ó
Ó
ÓA H
A H
A H
A HỮ
Ữ
Ữ
ỮU C
U C
U C
U CƠ
Ơ
Ơ
Ơ
Đ
Đ
Đ
ĐỒ
Ồ
Ồ
ỒNG PH
NG PH
NG PH
NG PHÂ
Â
Â
ÂN
N
N
N
�
Đ
Đ
Đ
Đị
ị
ị
ịnh
nh
nh
nh
ngh
ngh
ngh
nghĩ
ĩ
ĩ
ĩa
a
a
a :
:
:
:
là hiện tượng cùng một công thức có nhiều chất khác
nhau
�Đồng phân cấu tạo (phẳng) : cùng công thức phân
t
ử
nhưng
khác
công
thức
cấu
t
ạo
.
�Đồng phân lập thể (không gian) : cùng công thức
cấu tạo nhưng khác nhau về cách thức sắp xếp các
nguyên
t
ử
trong
không
gian (khác
nhau
về
cấu
h
ì
nh)
�
Ph
Ph
Ph
Phâ
â
â
ân
n
n
n
lo
lo
lo
loạ
ạ
ạ
ạ
i
i
i
i
:
:
:
:
Tùy
thuộc
vào việc các chấ
t
đồng phân phân
biệ
t
nhau về
cấu tạo
hay phân biệ
t
nhau về
cấu hình
mà
có 2
l
ọai
đồng
phân
I-
I-
I-
I- Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
c
c
c
cấ
ấ
ấ
ấu
u
u
u
t
t
t
tạ
ạ
ạ
ạo
o
o
o:
:
:
: phân biệt nhau về CTHH
Đồng phân cấu tạo
Đồng phân
mạch carbon
Đồng phân
vị trí
Đồng phân
nhóm chức
�Đồng phân mạch carbon, đồng phân vị trí : tính chấ
t
vậ
t
lý khác nhau (không nhiều), tính chấ
t
hóa học tương
đồng
.
�Đồng phân nhóm chức : tính chấ
t
vậ
t
lý hóa học hoàn
toàn
khác
nhau
.
CH3CH2CH2CH2CH
3CH3CH
OH
CH3
CH3CH2CH2OH
CH3CH2OH
CH3O CH3
CH3CH2CH CH3
CH3
�
Phân biệt giữa hỗ biến và đồng phân
�Trong một số trường hợp, chất hữu cơ có thể tồn tại dưới 2 dạng
cấu tạo khác nhau. Giữa 2 dạng này tồn tại một cân bằng liên tục
chuyển hóa lẫn nhau khiến cho chúng chỉ xử sự như một chất duy
nhất. Hiện tượng này được gọi là
sự hỗ biến
.
C
O
C
H
3
C
O
H
C
H
2
C
O
N
H
C
N
E
no
l
A
m
i
d
I
m
i
d
RR
X
e
t
on
RR'
O
H
RR'
� Hai dạng hỗ biến không thể tách riêng được do chúng chuyển
hóa (biến đổi) liên tục qua lại � như vậy hỗ biến không phải hiện
tượng đồng phân.
V
V
V
VÍ
Í
Í
Í D
D
D
DỤ
Ụ
Ụ
Ụ:
:
:
: CH OH
OCH
CH3CH2
C
2
H
4
O
II-
II-
II-
II- Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
l
l
l
lậ
ậ
ậ
ập
p
p
p
th
th
th
thể
ể
ể
ể:
:
:
:
Đ
Đồ
ồng
ng
ph
phâ
ân
n
l
l
ậ
ập
p
th
thể
ể
Đồng phân
hình học
Đồng phân
quang học
Các
đồng
phân
l
ập
thể
phân
biệ
t
nhau
về
cấu
h
ì
nh
ngh
ĩ
a
l
à
phân
biệ
t
nhau
về
sự
phân
bố
của
các
nhóm
thế
trong
không
gian
�
Đ
Đ
Đ
Đị
ị
ị
ịnh
nh
nh
nh
ngh
ngh
ngh
nghĩ
ĩ
ĩ
ĩa
a
a
a :
:
:
:
là những hợp chấ
t
có cùng CTPT, cùng
công thức khai triển phẳng ( cùng CTCT ) nhưng cách
sắp xếp của những nguyên tử hay nhóm nguyên tử khác
nhau
đố
i
vớ
i
mộ
t
mặ
t
phẳng
quy
chiếu
.
�Tùy vào mặ
t
phẳng qui chiếu đó là mặ
t
phẳng π (mặ
t
phẳng chứa nố
i
σ và π) hay mặ
t
phẳng vòng carbon mà
ta
đồng
phân
h
ì
nh
học
t
ương
ứng
.
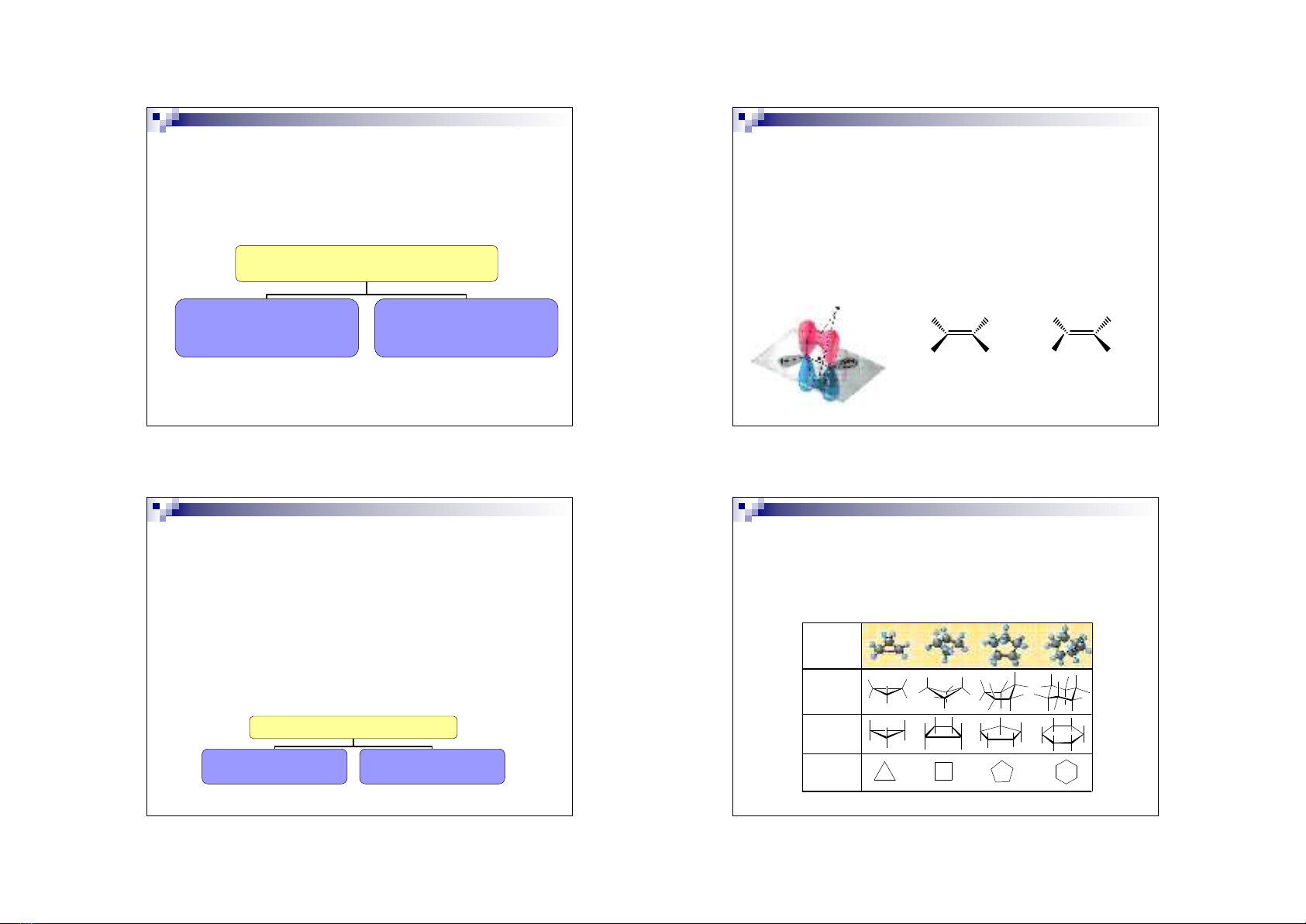
Đ
Đồ
ồng
ng
ph
phâ
ân
n
h
hì
ình
nh
h
họ
ọc
c
Đồng phân
của nối đôi
Đồng phân
xiclan
1-
1-
1-
1- Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
h
h
h
hì
ì
ì
ình
nh
nh
nh
h
h
h
họ
ọ
ọ
ọc
c
c
c:
:
:
:
�
Hiện
t
ượng
đồng
phân
có
được là do cơ cấu cứng nhắc
của nố
i
đô
i
khác vớ
i
nố
i
đơn không thể xoay được (nếu
không
sẽ
mấ
t
đ
i
sự
xen
phủ
bên
của 2 vân
đạo
π).
�
Như vậy nếu trên 2 carbon nố
i
đô
i
có 2 nhóm thế khác
nhau thì ta sẽ có 2 cách sắp xếp các nhóm thế trong
không gian (đố
i
vớ
i
mặ
t
phẳng π - mặ
t
phẳng chứa nố
i
σ
và
π) � 2 đồng
phân
h
ì
nh
học
.
H
HOOC
H
COOH
H
HOOC
COOH
H
Axit maleic Axit fumaric
Axit
cis
-2-butenoic Axit
trans
-2-butenoic
Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
h
h
h
hì
ì
ì
ình
nh
nh
nh
h
h
h
họ
ọ
ọ
ọc
c
c
c
c
c
c
củ
ủ
ủ
ủa
a
a
a
n
n
n
nố
ố
ố
ối
i
i
i
đ
đ
đ
đô
ô
ô
ôi
i
i
i
Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
h
h
h
hì
ì
ì
ình
nh
nh
nh
h
h
h
họ
ọ
ọ
ọc
c
c
c
ở
ở
ở
ở
h
h
h
hợ
ợ
ợ
ợp
p
p
p
ch
ch
ch
chấ
ấ
ấ
ấ
t
t
t
t
v
v
v
vò
ò
ò
òng
ng
ng
ng no
no
no
no
(
(
(
( Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
xiclan
xiclan
xiclan
xiclan )
)
)
)
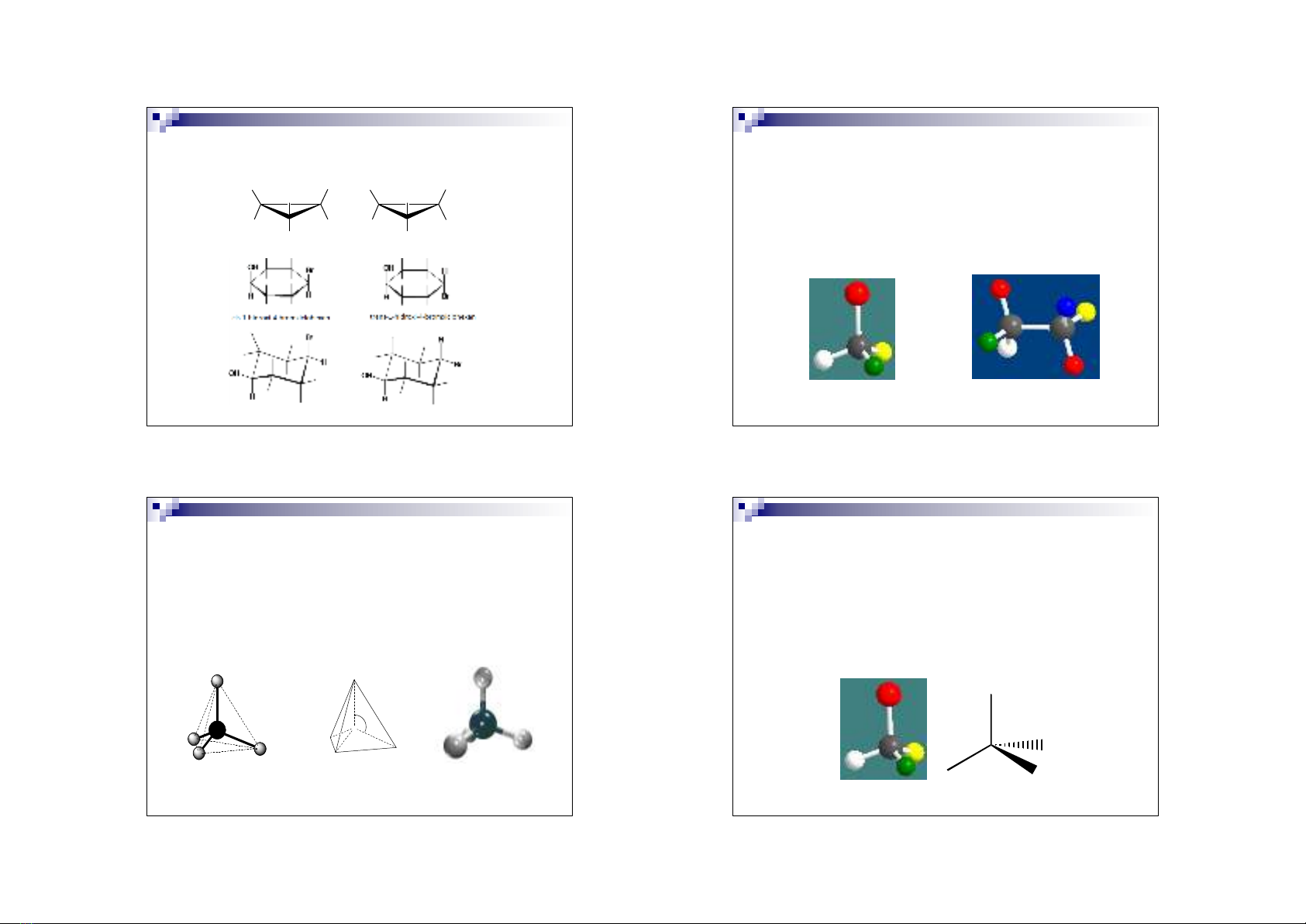
-Các hợp chất vòng no có thể có 3, 4, 5, 6, 7, 8, … carbon
-Nhưng vòng 3,4
r
ất kém bền (quá căng), trên thực tế các chất vòng
chủ yếu là vòng 5,6 (bền nhất). Vòng 7 trở lên
r
ất ít gặp.
Daïng ñôn giaûn
Caáu traïng öu ñaõi
thöïc teá
Coâng thöùc
khai trieån phaúng
Moâ hình phaân töû
H
3C
H
H
H
C
H
3
H
H
3C
H
H
C
H
3
H
H
Cis- và trans-1,2-dimetilxiclopropan
V
V
V
V
Í
Í
Í
Í
D
D
D
DỤ
Ụ
Ụ
Ụ:
:
:
:
Tùy vào sự phân bố của các nhóm thế so với mặt phẳng vòng
carbon mà ta có đồng phân cis- hay trans-
2-
2-
2-
2- Đ
Đ
Đ
Đồ
ồ
ồ
ồng
ng
ng
ng
ph
ph
ph
phâ
â
â
ân
n
n
n
quang
quang
quang
quang
h
h
h
họ
ọ
ọ
ọc
c
c
c:
:
:
:
2.1-
2.1-
2.1-
2.1- Thuy
Thuy
Thuy
Thuyế
ế
ế
ết
t
t
t carbon
carbon
carbon
carbon t
t
t
tứ
ứ
ứ
ứ
di
di
di
diệ
ệ
ệ
ện
n
n
n
v
v
v
và
à
à
à qui
qui
qui
qui ư
ư
ư
ướ
ớ
ớ
ớc
c
c
c
bi
bi
bi
biể
ể
ể
ểu
u
u
u
di
di
di
diễ
ễ
ễ
ễn
n
n
n
c
c
c
cơ
ơ
ơ
ơ
c
c
c
cấ
ấ
ấ
ấu
u
u
u
ph
ph
ph
phâ
â
â
ân
n
n
n
t
t
t
tử
ử
ử
ử
trong
trong
trong
trong
kh
kh
kh
khô
ô
ô
ông
ng
ng
ng
gian
gian
gian
gian:
:
:
:
a-
Thuyế
t
carbon
t
ứ
diện
(
Lebel & Van
’
Hoff, 1874
):
4 nguyên tử, nhóm nguyên tử nố
i
vớ
i
carbon được
phân bố trong không gian tạ
i
4 đỉnh của tứ diện đều có
t
âm
l
à
nguyên
t
ử carbon đó
:
H
H
H
H
C
H
H
H
H
109o28'
Nếu 4 nguyên tử hoặc nhóm nguyên tử
li
ên kết vớ
i
nguyên tử carbon hoàn toàn khác nhau thì nguyên tử
carbon trung tâm được gọ
i
l
à
carbon phi đố
i
xứng
hay
carbon bất đố
i
xứng
và được kí hiệu
l
à C
*.
Axit lactic 3-brombutan-2-ol
CH
3
–CHOH–COOH CH
3
–CHBr–CHOH–CH
3
V
V
V
V
í
í
í
í
d
d
d
dụ
ụ
ụ
ụ:
:
:
:
b- Qui
Qui
Qui
Qui ư
ư
ư
ướ
ớ
ớ
ớc
c
c
c
bi
bi
bi
biể
ể
ể
ểu
u
u
u
di
di
di
diễ
ễ
ễ
ễn
n
n
n
c
c
c
cơ
ơ
ơ
ơ
c
c
c
cấ
ấ
ấ
ấu
u
u
u
ph
ph
ph
phâ
â
â
ân
n
n
n
t
t
t
tử
ử
ử
ử
trong
trong
trong
trong
kh
kh
kh
khô
ô
ô
ông
ng
ng
ng
gian
gian
gian
gian:
:
:
:
�
C
C
C
Cô
ô
ô
ông
ng
ng
ng
th
th
th
thứ
ứ
ứ
ức
c
c
c
ph
ph
ph
phố
ố
ố
ố
i
i
i
i
c
c
c
cả
ả
ả
ảnh
nh
nh
nh:
:
:
:
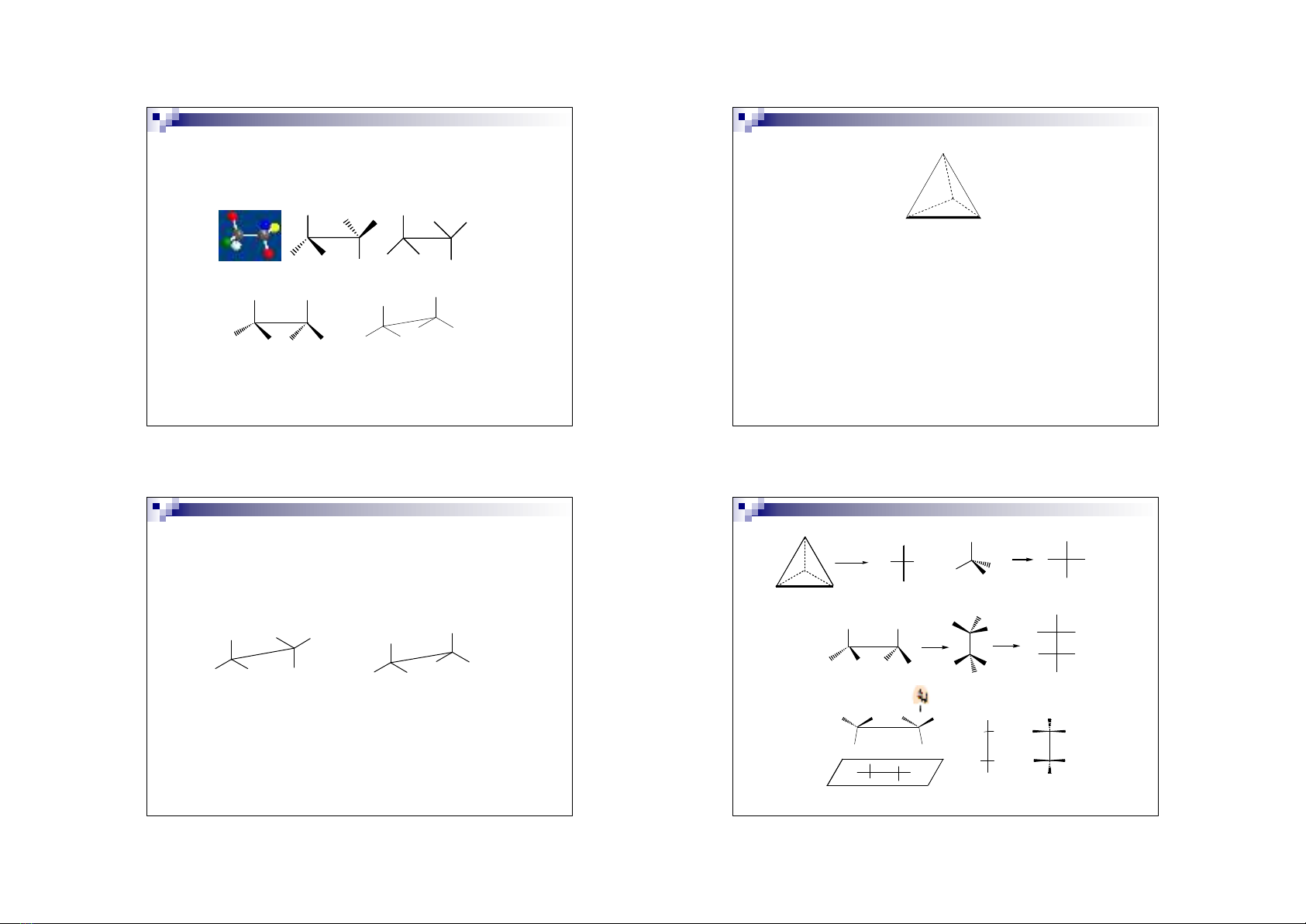
�
Các liên kế
t
nằm trong mặ
t
phẳng được biểu diễn bằng
né
t li
ền
mảnh
.
�
Liên kế
t
hướng ra phía trước mặ
t
phẳng được biểu diễn
bằng
né
t
đậm
.
�
Liên kế
t
hướng ra phía sau mặ
t
phẳng được biểu diễn
bằng
né
t
đứ
t.
=
�
Công
thức
phố
i
cảnh
cho
hợp
chấ
t
có
nhiều carbon:
�Nố
i
sang phả
i
hướng
ra
bên
ngoà
i
mặ
t
phẳng
�Nố
i
sang trá
i
hướng
ra
ph
í
a
sau
mặ
t
phẳng
==
CT phố
i
cảnh dạng đố
i
=
CT phố
i
cảnh dạng che khuất
Ví dụ:
Công thức phối cảnh dạng đối và công thức phối cảnh
dạng che khuất của axit 2-brom-3-clobutanoic
CH
3
-CHCl-CHBr-COOH
H
Cl
C
H
3
H
Br
COO
H
C
H
3
Br
COO
H
H
C
l
H
�
M
M
M
Mô
ô
ô
ô
h
h
h
h
ì
ì
ì
ì
nh
nh
nh
nh
t
t
t
tứ
ứ
ứ
ứ
di
di
di
diệ
ệ
ệ
ện
n
n
n
:
�
C
C
C
Cô
ô
ô
ông
ng
ng
ng
th
th
th
thứ
ứ
ứ
ức
c
c
c
chi
chi
chi
chiế
ế
ế
ếu
u
u
u Fischer
Fischer
Fischer
Fischer
:
Đặ
t t
ứ
diện
hoặc
công
thức
phố
i
cảnh
sao
cho 1 cạnh
nằm
ngang
hướng
về
ph
í
a
ngườ
i
quan
sá
t
rồ
i
chiếu
xuống
mặ
t
phẳng
giấy
.
Trục
thẳng
đứng
l
à
mạch carbon đồng
thờ
i
biểu
diễn
các
li
ên
kế
t
hướng
ra
ph
í
a
sau
mặ
t
phẳng
.
Trục
nằm
ngang
biểu
diễn
các
li
ên
kế
t
hướng
ra
ph
í
a
trước
mặ
t
phẳng
.
b
a
cd
H
COO
H
O
H
C
H
3
H
COO
H
O
H
C
H
3
B
rH
COO
H
H
C
l
C
H
3
B
r
COO
H
H
C
H
3
H
C
l
COO
H
B
rH
C
H
3
C
l
H
COO
H
C
H
3
O
H
H
COO
H
O
HH
C
H
3
CH3COOH
H Cl Br H
CH3
H
Cl
Br
H
COOH
COOH
H
Br
ClH
CH3
HBr
COOH
CH3
H Cl
=
Hoặc








![Tập bài giảng Hoá học đại cương 1 - Đăng Thị Thu Huyền [Full, Chi Tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260312/hoabattu2026/135x160/11351773633935.jpg)











![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



