
CHƯƠNG 9
VẬT LÍ NGUYÊN TỬ
2
Chương 9-Vật lí nguyên tử
1. Nguyên tử Hydro
•Phương trình Schrodinger và nghiệm cho electron trong nguyên tử
Hydro
•Các kết luận về nguyên tử H ( năng lượng, trạng thái, xác suất tìm
thấy electron)
2. Nguyên tử kim loại kiềm ( biểu thức năng lượng, dãy vạch quang
phổ)
3. Mômen động lượng quỹ đạo và mômen từ quĩ đạo của electron
4. Spin của electron

3
1. NGUYÊN TỬ HIĐRÔ
•Chúng ta nghiên cứu chuyển động của electrôn trong nguyên tử
hiđrô trên cơ sở phương trình Schrodinger, phương trình cơ bản của
cơ học lượng tử:
trong đó U là thế năng tương tác giữa hạt nhân và electrôn.
Bài toán đặt ra là tìm năng lượng của electrôn và hàm sóng của
nó.
Giải phương trình Schrodinger trong hệ tọa độ cầu, ta thu được một số
kết luận.
4
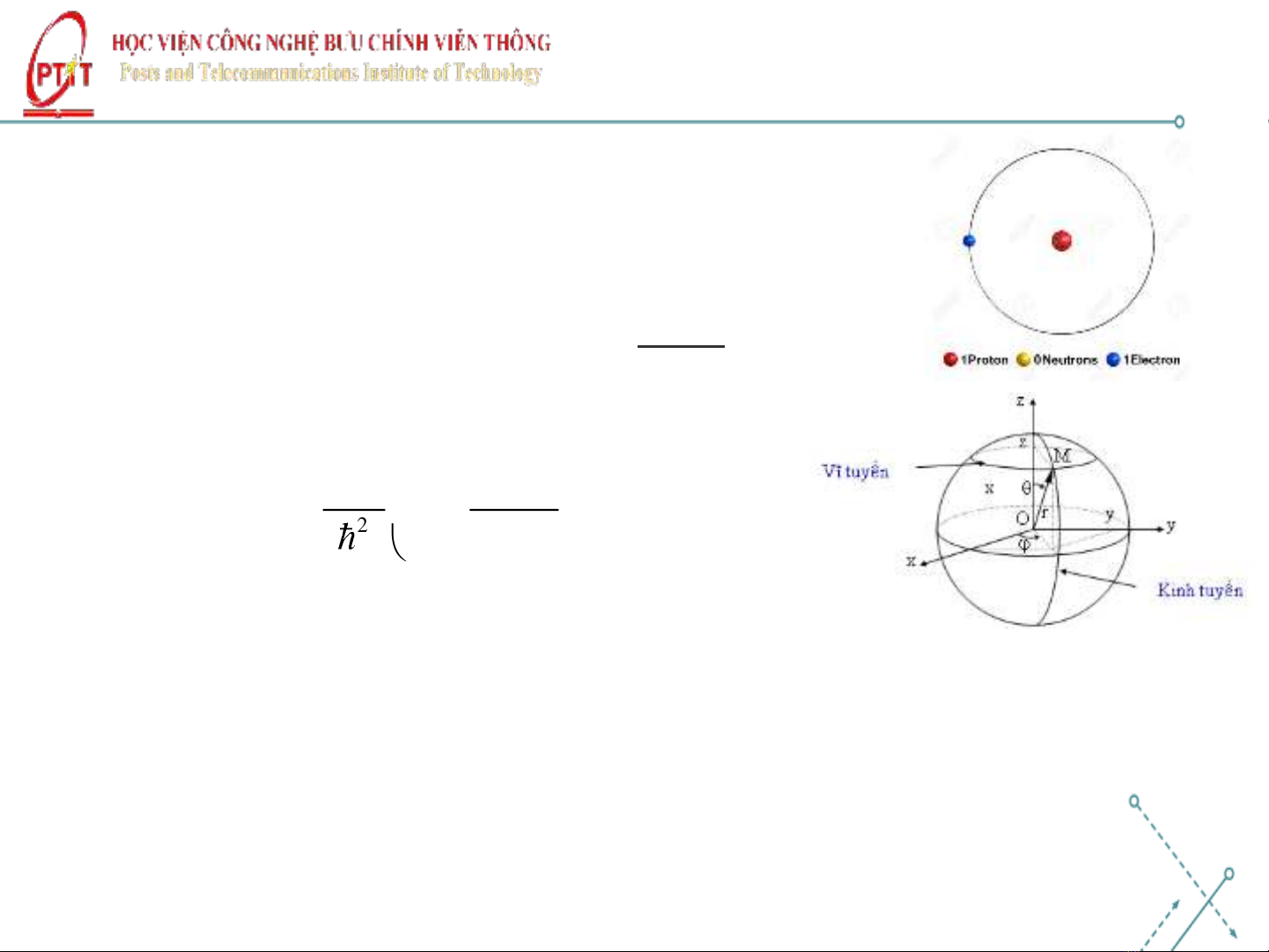
•Cấu tạo nguyên tử H:
•Thế năng tương tác giữa hạt nhân và electron:
U = − Ze2
4𝜋𝜀0r
•Phương trình Schrodinger:
•Do U phụ thuộc r nên bài toán có tính
đối xứng cầu chuyển Descartes sang tọa độ cầu:
2
2
2
( , , ) ( , , ) 0
4
e
o
me
x y z E x y z
r
sin cos
sin sin
cos
xr
yr
zr
0 180o,
0 360o
5
•Toán tử Laplace trong hệ toạ độ cầu:
Phương trình này được giải bằng phương pháp phân li biến số, nghiệm của
phương trình có dạng như sau:
Hàm sóng:
(hàm xuyên tâm,
hàm cầu)
•Năng lượng:
R là hằng số Rydberg (Rittbe), R = 3,27.1015 s-1
0
r4
e
E
m2
sinr
1
sin
sinr
1
r
r
r
r
1
o
2
2
e
2
2
222
2
2
( , , ) ( ) ( , )
()
( , )
nl lm
nl
lm
r R r Y
Rr
Y
222
o
4
e
2
nn
Rh
)4(2
em
n
1
E
Với:
n=1,2,3... : số lượng tử chính
l=0,1,2...(n-1) : số lượng tử quĩ đạo
( orbital)
m=0,±1,±2...±l : số lượng tử từ


![Bài giảng Cấu tạo vật thể ThS. Nguyễn Hoàng Thông [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250707/nguyenhoangthong.hui@gmail.com/135x160/197_bai-giang-cau-tao-vat-the-ths-nguyen-hoang-thong.jpg)
















![Đề thi học kì 2 môn Vật lí 1 năm 2023-2024 có đáp án [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/64291778553454.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2023-2024 có đáp án [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/1381778553461.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2022-2023 có đáp án [kèm PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/21778553462.jpg)




