
Đ C NG ÔN T P H C K II – NĂM H C 2021-2021Ề ƯƠ Ậ Ọ Ỳ Ọ
MÔN: HÓA H C 10Ọ
A. LÝ THUY TẾ
CH NG V: HALOGENƯƠ
1. Trình bày c u t o nguyên t c a các halogen, s oxi hoá c a halogen trong các h p ch t.ấ ạ ử ủ ố ủ ợ ấ
2. Nêu tính ch t hoá h c, tính ch t v t lí c b n c a các halogen và h p ch t c a chúng.ấ ọ ấ ậ ơ ả ủ ợ ấ ủ
3. Nêu ph ng pháp đi u ch halogen và m t s h p ch t c a halogen.ươ ề ế ộ ố ợ ấ ủ
CH NG VI: OXI-OZONƯƠ
1. C u t o nguyên t c a các nguyên t nhóm oxi. ấ ạ ử ủ ố S oxi hoá c a O trong các h p ch t.ố ủ ợ ấ
2. C u t o phân t , tính ch t hoá h c, tính ch t v t lí c b n c a Oấ ạ ử ấ ọ ấ ậ ơ ả ủ 2,O3
3. Ph ng pháp đi u ch Oươ ề ế 2 trong công nghi p và trong phòng thí nghi m.ệ ệ
4. Cách nh n bi t Oậ ế 2, O3.
B. BÀI T PẬ
CH NG V:HALOGENƯƠ
D NG 1: Hoàn thành chu i ph n ng:Ạ ỗ ả ứ
a. MnO2 Cl2 FeCl3Fe(OH)3 FeCl3 AgCl Cl2.
b. KMnO4 Cl2 HCl CuCl2 BaCl2 BaSO4.
c. NaCl HCl Cl2 FeCl3 NaCl NaOH NaClCl2CaCl2AgClAg.
d. NaClHCl KCl Cl2NaClH2HCl Cl2CuCl2Cu(OH)2
D NG 2: NH N BI T :Ạ Ậ Ế
Nh n bi t các dung d ch m t nhãn b ng ph ng pháp hóa h c.ậ ế ị ấ ằ ươ ọ
a. NaOH, HCl, NaCl, NaNO3. b. KCl, KNO3, HCl, HNO3.
c. KCl, K2SO4, KNO3. d. HCl, H2SO4, HNO3.
e. Ba(OH)2, H2SO4, Na2SO4 , KCl, HNO3. f. CaCl2, Ca(OH)2, NaOH, Ca(NO3)2.
D NG 3: BÀI T P ĐNH TÍNHẠ Ậ Ị
(Kim lo i hoăc oxit kim lo i vào dd HCl)ạ ạ
1. Cho 26,1g MnO2 tác d ng h t v i 400ml dung d ch axit clohidric đm đc.ụ ế ớ ị ậ ặ
a. Tính th tích khí thoát ra đktc.ể
b. Tính n ng đ mol HCl.ồ ộ
c. L ng khí clo thu đc có đ đ tác d ng h t v i 1,12g s t không?ượ ượ ủ ể ụ ế ớ ắ
2. Cho 30g h n h p g m Cu và Zn tác d ng h t v i 200g dung d ch HCl thu đc 5600ml khí (đktc).ỗ ợ ồ ụ ế ớ ị ượ
a. Tính kh i l ng m i kim lo i.ố ượ ỗ ạ
b. Tính thành ph n % kh i l ng m i kim lo i theo kh i l ng.ầ ố ượ ỗ ạ ố ượ
c. Tính n ng đ % HCl.ồ ộ
3. Cho 15g h n h p g m Fe,Ag tác d ng h t v i dung d ch HCl 15,6% thu đc 3360ml khí thu đc ỗ ợ ồ ụ ế ớ ị ượ ượ
(đktc).
a. Tính kh i l ng m i kim lo i trong h n h p.ố ượ ỗ ạ ỗ ợ
b. Tính thành ph n % kh i l ng m i kim lo i.ầ ố ượ ỗ ạ
c. Tính kh i l ng dung d ch HCl ph n ng.ố ượ ị ả ứ
4. Cho 1,4g s t tác d ng v i 840ml khí clo (đktc).ắ ụ ớ
a. Tính kh i l ng các ch t thu đc sau ph n ng.ố ượ ấ ượ ả ứ
b. Tính th tích dung d ch HCl 0,5M đ đ tác d ng h t v i các ch t thu đc trong ph n ng ể ị ủ ể ụ ế ớ ấ ượ ả ứ
trên.
5. Cho 29,8g h n h p g m Fe,Zn tác d ng h t v i 600ml dung d ch HCl thu d c 11,2 lít khí (đktc).ỗ ợ ồ ụ ế ớ ị ượ
a. Tính thành ph n % theo kh i l ng m i kim lo i.ầ ố ượ ỗ ạ
b. Tính n ng đ mol HCl.ồ ộ
6. Cho clo tác d ng v i v a đ v i Fe r i hòa tan l ng mu i sinh ra vào n c đc 100g dung d ch ụ ớ ừ ủ ớ ồ ượ ố ướ ượ ị
mu i có n ng đ 16,25%.ố ồ ộ
1

a. Tình kh i l ng mu i trong dung d ch.ố ượ ố ị
b. Tính kh i l ng s t và clo (đktc) đã dung.ố ượ ắ
7. Hòa tan 10,55g h n h p g m Zn và ZnO vào m t l ng v a đ dung d ch HCl 10% thì thu đc 2,24 ỗ ợ ồ ộ ượ ừ ủ ị ượ
lít khí (đktc).a. Tính kh i l ng m i ch t trong h n h p đu.ố ượ ỗ ấ ỗ ợ ầ
b. Tính kh i l ng dung d ch HCl đã dùng.ố ượ ị
CH NG VI: OXI-OZONƯƠ
D NG 1: OXI TÁC D NG KIM LO IẠ Ụ Ạ
Bài 1: Khi đt 18,4 (g) h n h p Zn, Al thì c n 5,6 (l) khí Oố ỗ ợ ầ 2 (đkc).
a) Tính % theo kh i l ng c a h n h p ban đu?ố ượ ủ ỗ ợ ầ
b) N u cho 9,2(g) h n h p kim lo i vào dd Hế ỗ ợ ạ 2SeO4 thì thu đc bao nhiêu lít khí Hượ 2?
Bài 2: Cho 3,36 (l) khí O2 (đkc) ph n ng hoàn toàn v i kim lo i M có hóa tr 3, thu đc 10,2 (g) oxit.ả ứ ớ ạ ị ượ
Xác đnh M?ị
Bài 3:Cho 1,35 gam m t kim lo i R tác d ng h t v i oxi d thu đc 2,55 gam oxit kim lo i. Xác đnhộ ạ ụ ế ớ ư ượ ạ ị
kim lo i R ?ạ
D NG 2: BÀI TOÁN T KH I H N H P OẠ Ỉ Ố Ỗ Ợ 2 – O3
Bài 1: M t h n h p khí X g m Oộ ỗ ợ ồ 2 và O3. T kh i h i c a X đi v i khí hidro b ng 18. Xác đnh thànhỉ ố ơ ủ ố ớ ằ ị
ph n % theo th tích c a h n h p khí?ầ ể ủ ỗ ợ
Bài 2: D n 2,688 lít h n h p khí g m oxi và ôzn (đktc) vào dung d ch KI d thì thu đc 20,32g Iôt k tẫ ỗ ợ ồ ị ư ượ ế
t a màu đen tím. Tính thành ph n ph n tram theo th tích c a m i khí trong h n h p?ủ ầ ầ ể ủ ỗ ỗ ợ
CÂU H I TR C NGHI MỎ Ắ Ệ
I. BI TẾ
Câu 1: S p x p theo chi u tăng tính oxi hóa c a các nguyên t là ắ ế ề ủ ử
A. I, Cl, Br, F B. Cl,I,F,Br. C. I,Br,Cl,F D. I,Cl,F,Br
Câu 2: C u hình electron l p ngoài cùng c a các nguyên t Halogen làấ ớ ủ ử
A. ns2 np4. B. ns2 np5 C. ns2 np6D. (n – 1)d10 ns2 np5.
Câu 3: Trong n c clo có ch a các ch tướ ứ ấ
A. HCl, HClO B. HCl, HClO, Cl2 C. HCl, Cl2D. Cl2
Câu 4: Hoá ch t dùng đ nh n bi t 4 dd : NaF, NaCl, NaBr, NaI là ấ ể ậ ế
A. NaOH B. H2SO4C. AgNO3D. Ag
Câu 5: Trong phòng thí nghi m ng i ta th ng đi u ch clo b ng cáchệ ườ ườ ề ế ằ
A. đi n phân nóng ch y NaCl.ệ ả B. đi n phân dung d ch NaCl có màng ngăn.ệ ị
C. phân hu khí HCl.ỷD. cho HCl đc tác d ng v i MnOặ ụ ớ 2; KMnO4…
Câu 6. Clorua vôi là
A. Mu i t o b i kim lo i liên k t v i m t g c axit.ố ạ ở ạ ế ớ ộ ố
B. Mu i t o b i kim lo i liên k t v i hai g c axit.ố ạ ở ạ ế ớ ố
C. Mu i t o b i hai kim lo i liên k t v i m t g c axit. ố ạ ở ạ ế ớ ộ ố
D. Clorua vôi không ph i là mu i.ả ố
Câu 7. Thu c th đ nh n ra iot làố ử ể ậ
A. h tinh b t.ồ ộ B. n c brom.ướ C. phenolphthalein. D. Quì tím.
Câu 8. Clo không ph n ng v i ch t nào sau đây?ả ứ ớ ấ
A. NaOH B. NaCl C. Ca(OH)2 D. NaBr
2
Câu 9. Ph n ng gi a Clả ứ ữ 2 và H2 có th x y ra đi u ki nể ả ở ề ệ
A. nhi t đ th ng và bóng t i.ệ ộ ườ ố B. ánh sáng m t tr i.ặ ờ
C. ánh sang c a magie cháy.ủ D. C A, B và C.ả
Câu 10: Cho hai khí v i th tích là 1:1 ra ngoài ánh sáng m t tr i thì có hi n t ng n , hai khí đó là ớ ể ặ ờ ệ ượ ổ
A. N2 và H2. B. H2 và O2. C. Cl2 và H2. D. H2S và Cl2.
Câu 11: đi u ki n th ng, clo là ch t khí, màu vàng l c, có mùi x c và n ng h n không khíở ề ệ ườ ấ ụ ố ặ ơ
A. 1,25 l n. ầ B. 2,45 l n. ầ C. 1,26 l n. ầ D. 2,25 l n.ầ
Câu 12: Trong các Halogen sau: F2, Cl2, Br2, I2, halogen ph n ng v i n c m nh nh t là:ả ứ ớ ướ ạ ấ
A. Cl2B. Br2C. F2D. I2
Câu 13: Trong dãy dung d ch axit : HF, HCl, HBr, HI ị
A.Tính axit tang d n t trái qua ph iầ ừ ả
B.Tính axit gi m d n t trái qua ph iả ầ ừ ả
C.Tính axit tang d n đn HCl và sau đó gi m đn HIầ ế ả ế
D.Tính axit b bi n đi ko theo quy lu t.ị ế ổ ậ
Câu 14:Cho các axit : HCl(1);HI(2);HBr(3).S p x p theo chi u tính kh gi m d n:ắ ế ề ử ả ầ
A.(1)>(2)>(3) B.(3)>(2)>(1)
C.(1)>(3)>(2) D.(2)>(3)>(1)
Câu 15: Tính oxy hoá c a các halogen gi m d n theo th t sau:ủ ả ầ ứ ự
A.Cl2> Br2>I2>F2B. F2> Cl2>Br2>I2
C. Br2> F2>I2>Cl2D. I2> Br2>Cl2>F2
Câu 16: S oxy hoá c a clo trong các ch t: HCl, KClOố ủ ấ 3, HClO, HClO2, HClO4 l n l t là:ầ ượ
A. +1, +5, -1, +3, +7 B. -1, +5, +1, -3, -7
C. -1, -5, -1, -3, -7 D. -1, +5, +1, +3, +7
Câu 17: Trong 4 h n h p sau đây, h n h p nào là n c Javenỗ ợ ỗ ợ ướ
A. NaCl + NaClO + H2O B. NaCl + NaClO2 + H2O
C. NaCl + NaClO3 + H2O D. NaCl +HClO+ H2O
Câu 18: Thêm d n d n n c Clo vào dung d ch KI có ch a s n m t ít h tinh b t . Hi n t ng quan sátầ ầ ướ ị ứ ẵ ộ ồ ộ ệ ượ
đc : A.dd hi n màu xanh . ượ ệ B. dd hi n màu vàng l c ệ ụ
C. Có k t t a màu tr ng ế ủ ắ D. Có k t t a màu vàng nh t .ế ủ ạ
Câu 19: Ch t tác d ng v i Hấ ụ ớ 2O t o ra khí oxi là:ạ
A. Flo B. Clo C. Brom D. Iot
Câu 20: Ph n ng nào sau đây dung đ đi u ch khí Clo trong công nghi pả ứ ể ề ế ệ
A. MnO2 + 4 HCl MnCl2 + Cl2 + H2O
B. 2KMnO4 + 16 HCl 2 KCl + 2 MnCl2 + 5 Cl2 + 8 H2O
C. 2 NaCl + 2 H2O 2NaOH + H2 + Cl2
D. a,b,c đu đúng ề
Câu 21: Ph n ng gi a hydro và ch t nào sau đây thu n ngh ch? ả ứ ữ ấ ậ ị
A. Iot. B. Brom C. Clo. D. Flo.
Câu 22: Cho khí Clo tác d ng v i s t, s n ph m sinh ra là:ụ ớ ắ ả ẩ
A. FeCl2 B. FeCl C.FeCl3 D. Fe2Cl3
Câu 23: N c clo có tính oxy hóa m nh là do trong đó cóướ ạ
A. Cl2. B. HCl. C. HClO. D. O.
Câu 24: Cho Flo, Clo, Brom, Iot l n l t tác d ng v i Hầ ượ ụ ớ 2. Ph n ng gi a halogen nào x y ra mãnh li t ả ứ ữ ả ệ
nh t. A. Fấ2. B. Cl2. C. Br2. D. I2.
Câu 25: Ph n ng nào sau đây không th x y ra ?ả ứ ể ả
A. H2Oh ơnóng + F2B. KBrdd + Cl2
C. NaIdd+ Br2D. KBrdd + I2
3
Câu 26: Hãy l a ch n ph ng pháp đi u ch khí hidroclorua trong phòng thí nghi m:ự ọ ươ ề ế ệ
A. Th y phân AlClủ3. B. T ng h p t Hổ ợ ừ 2 và Cl2.
C. clo tác d ng v i Hụ ớ 2O. D. NaCl tinh th và Hể2SO4đc.ặ
Câu 27: Thu c th dùng đ nh n ra ion clorua trong dung d ch là :ố ử ể ậ ị
A. Cu(NO3)2B.Ba(NO3)2C. AgNO3D. Na2SO4
Câu 28: Ch t tác d ng v i Hấ ụ ớ 2O t o ra khí oxi là:ạ
A. Flo B. Clo C. Brom D. Iot
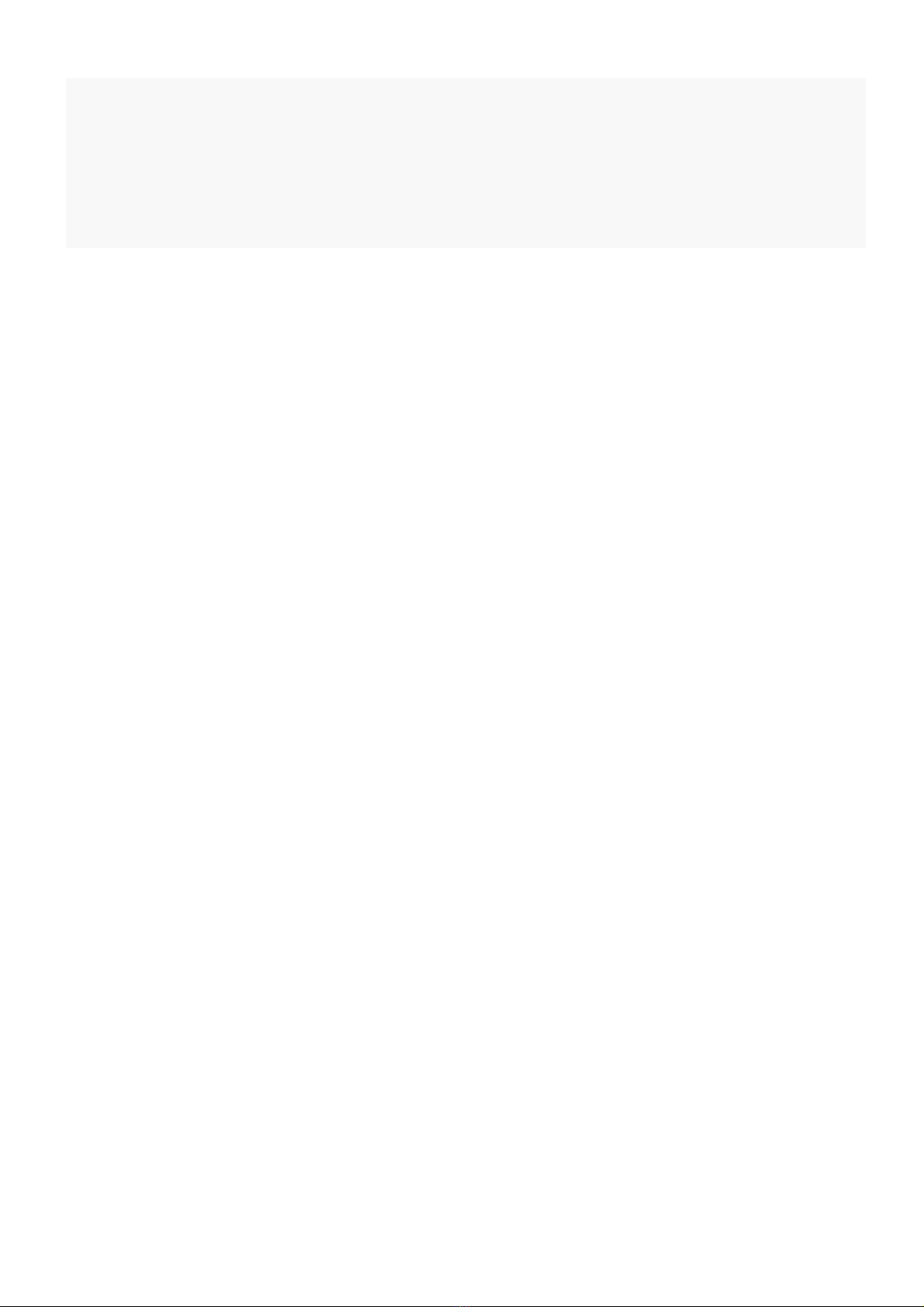
Câu 29: Cho hình v mô t thí nghi m đi u ch Clẽ ả ệ ề ế 2 t MnOừ2 và dung d ch HCl.ị
Khí Cl2 sinh ra th ng có l n h i n c và hidrocloruaườ ẫ ơ ướ . Đ thu đc khí Clể ượ 2 khô thì bình (1) và bình (2)
l n l t đngầ ượ ự
A. dung d ch NaOH và dung d ch Hị ị 2SO4 đặc. B. dung d ch Hị2SO4 đc và dung d ch NaCl.ặ ị
C. dung d ch Hị2SO4 đc và dung d ch AgNOặ ị 3.D. dung d ch NaCl và dung d ch Hị ị 2SO4 đặc.
Câu 30: Ch t nào d i đây có s thăng hoa khi đun nóng (tr ng thái r n chuy n sang tr ng thái h i) ấ ướ ự ạ ắ ể ạ ơ
A. Cl2B. I2C. Br2D. F2
II. THÔNG HI U:Ể
Câu 31: Hòa tan khí Cl2 vào dung d ch KOH đc, nóng, d thu đc dung d ch ch a các ch t thu c dãyị ặ ư ượ ị ứ ấ ộ
nào sau đây?
A. KCl, KClO3, Cl2B. KCl, KClO, KOH
C. KCl, KClO3, KOH. D. KCl, KClO3
Câu 32: Hòa tan khí Cl2 vào dung d ch NaOH loãng, d nhi t đ phòng thu đc dung d ch ch a cácị ư ở ệ ộ ượ ị ứ
ch tấ
A. NaCl, NaClO3, Cl2B. NaCl, NaClO, NaOH
C. NaCl, NaClO3, NaOH D. NaCl, NaClO3
Câu 33: Dãy g m các ch t đu ph n ng v i dung d ch HCl làồ ấ ề ả ứ ớ ị
A. NaOH, Al, CuSO4, CuO. B. Cu(OH)2, Cu, CuO, Fe.
C. CaO, Al2O3, Na2SO4, H2SO4. D. NaOH, Al, CaCO3,Cu(OH)2, Fe, CaO, Al2O3.
Câu 34: Kim lo i tác d ng đc v i axit HCl loãng và khí clo cho cùng m t lo i mu i clorua kim lo iạ ụ ượ ớ ộ ạ ố ạ
là
A. Fe. B. Zn. C. Cu. D. Ag.
Câu 35: Hoá ch t dùng đ nh n bi t 4 dd : NaF, NaCl, NaBr, NaI là ấ ể ậ ế
A. NaOH B. H2SO4C. AgNO3D. Ag
Câu 36. Tính t y màu c a dung d ch n c clo là doẩ ủ ị ướ
A. Cl2 có tính oxi hóa m nh.ạ B. HClO có tính oxi hóa m nh.ạ
C. HCl là axit m nh.ạ D. nguyên nhân khác.
Câu 37: Phát bi u nào sau đây ểsai?
A. Halogen là nh ng phi kim đi n hình, chúng là nh ng ch t oxi hóa.ữ ể ữ ấ
B. Trong h p ch t các halogen đu có th có s oxi hóa: -1, +1, +3, +5, +7.ợ ấ ề ể ố
C. Kh năng oxi hóa c a halogen gi m d n t flo đn iotả ủ ả ầ ừ ế
D. Các halogen khá gi ng nhau v tính ch t hóa h c.ố ề ấ ọ
4
Câu 38: Cho dãy dung d ch axit sau HF, HCl, HBr, HI. Dung d ch có tính axit m nh nh t và tính khị ị ạ ấ ử
m nh nh t là:ạ ấ
A. HF B. HCl C. HBr D. HI
Câu 39: Đ dd ch a 1 g HBr vào dd ch a 1 g NaOH. Nhúng gi y quì tím vào dung d ch thu đc thìổ ứ ứ ấ ị ượ
gi y quì tím chuy n sang màu ấ ể
A. đ.ỏB. xanh. C. Không màu. D.tím.
Câu 40: Đ phân bi t 5 dd riêng bi t sau: NaCl, NaBr, NaI, NaOH, HCl. Ta có th dùng nhóm thu c th ể ệ ệ ể ố ử
nào sau đây?
A. khí Clo, dd AgNO3 B. quì tím, khí Clo C. quì tím, dd AgNO3D. c B,C đúngả
Câu 41: Nh n đnh nào sau đâyậ ị sai khi nói v flo?ề
A. Là phi kim lo i ho t đng m nh nh tạ ạ ộ ạ ấ B. Có nhi u đng v b nề ồ ị ề trong t nhiênự
C. Là ch t oxi hoá r t m nhấ ấ ạ D. Có đ âm đi n l n nh tộ ệ ớ ấ
Câu 42. Đc đi m nào không ph i là đc đi m chung c a các halogen?ặ ể ả ặ ể ủ
A. Đu là ch t khí đi u ki n th ng.ề ấ ở ề ệ ườ B. Đu có tính oxi hóa m nh.ề ạ
C. Tác d ng v i h u h t các kim lo i và phi kim.ụ ớ ầ ế ạ D. Kh năng tác d ng v i n c gi m d n tử ụ ớ ướ ả ầ ử
F2 đn Iế2.
Câu 43:Dùng bình th y tinh có th ch a đc t t c các dung d ch axit trong dãy nào d i đây ?ủ ể ứ ượ ấ ả ị ướ
A. HCl, H2SO4, HF, HNO3. B. HCl, H2SO4, HF.
C. H2SO4, HF, HNO3. D. HCl, H2SO4, HNO3.
Câu 44: Ph n ng nào ch ng t HCl là ch t kh ?ả ứ ứ ỏ ấ ử
A. HCl + NaOH NaCl + H→2O. B. 2HCl + Mg MgCl→2+ H2 .
C. MnO2+ 4 HCl → MnCl2+ Cl2 + 2H2O. D. NH3+ HCl → NH4Cl.
Câu 45: Dung d ch HCl ph n ng đc v i t t c các ch t trong nhóm nào sau đây:ị ả ứ ượ ớ ấ ả ấ
A. NaCl, H2O, Ca(OH)2, KOH B. CaO, Na2CO3, Al(OH)3, S
C. Al(OH)3, Cu, S, Na2CO3 D. Zn, CaO, Al(OH)3, Na2CO3
Câu 46: Trong các oxit sau:CuO, SO2, CaO, P2O5, FeO, Na2O, Oxit ph n ng đc ả ứ ượ v i axit HCl là:ớ
A. CuO, P2O5, Na2O B. CuO, CaO,SO2
C. SO2, FeO, Na2O, CuO D. FeO, CuO, CaO, Na2O
Câu 47: S oxi hóa c a Clo trong phân t CaOClố ủ ử 2 là:
A. 0 B. –1 C. +1 D. –1 và +1.
Câu 48: Ph n ng nào ch ng t HCl là ch t kh ?ả ứ ứ ỏ ấ ử
A. HCl + NaOH NaCl + H2O. B. 2HCl + Mg MgCl2+ H2 .
C. MnO2+ 4 HCl MnCl2+ Cl2 + 2H2O. D. NH3+ HCl NH4Cl.
Câu 49: H p ch t mà trong đó oxi có s oxi hoá +2 là :ợ ấ ố
A. H2O B. H2O2
C. OF2D. Cl2O7
Câu 50: H p ch t nào sau đây đc dung đ đi u ch khí Clo khi cho tác d ng v i axit HCl:ợ ấ ượ ể ề ế ụ ớ
A. MnO2, NaCl B. KMnO4, NaCl
C. KMnO4, MnO2 D. NaOH, MnO2
Câu 51: Cho ph n ng: HCl + Fe ả ứ H2 + X. Công th c hóa h c c a X là:ứ ọ ủ
A. FeCl2B. FeCl
C. FeCl3 D.Fe2Cl3
III. V N D NG:Ậ Ụ
Câu 52: Đt 11,2 g b t s t trong khí Clo. Kh i l ng s n ph m sinh ra là:ố ộ ắ ố ượ ả ẩ
A. 32,5 g B. 24,5 g C. 162,5 g D. 25.4 g
Caâu 53: Cho 11,2 gam s t tác d ng v i dd HCl d . Kh i l ng mu i sinh ra là: ắ ụ ớ ư ố ượ ố
A. 32,5 g B.162,5 g C. 24,5 g D. 25,4 g
5



![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)










![Phiếu bài tập cuối tuần Tiếng Việt 1 tuần 2 đề 2: [Hướng dẫn chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250728/thanhha01/135x160/42951755577464.jpg)

