
TRUNG TÂM TIẾP BƯỚC LỚP HÓA 12 NĂM HỌC 2022 - 2023
1
ĐỀ DỰ ĐOÁN THI THPT QUỐC GIA 2023 – ĐỀ 2
Câu 1: Kim loại sau đây không tác dụng với dung dịch H2SO4 loãng là
A. Al. B. Ag. C. Mg. D. Fe.
Câu 2: Ở điều kiện thường, chất nào sau đây là chất khí?
A. Anilin. B. Etanamin. C. Glyxin. D. Metanol.
Câu 3: Chất nào sau đây không phải là chất điện li?
A. CH3COOH. B. CH3COOC2H5. C. NaOH. D. MgCl2.
Câu 4: Al2O3 không tan được trong dung dịch chứa chất tan nào sau đây?
A. KOH. B. NaOH. C. HCl. D. CaCl2.
Câu 5: Vật làm bằng hợp kim Zn-Fe trong môi trường không khí ẩm (hơi nước có hòa tan oxi) đã xảy ra quá trình ăn
mòn điện hóa. Tại anot xảy ra quá trình:
A. Oxi hóa Fe. B. Khử O2. C. Khử Zn. D. Oxi hóa Zn.
Câu 6: Nước cứng có chứa các ion Mg2+, Cl,
3
HCO-
thuộc loại nước cứng
A. Toàn phần. B. Tạm thời. C. Vĩnh cửu. D. Một phần.
Câu 7: Cho từ từ đến dư kim loại X vào dung dịch FeCl3, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp kim loại
Fe và X dư. X là kim loại nào sau đây?
A. Fe. B. Cu. C. Mg. D. Na.
Câu 8: Kim loại M phản ứng được với dung dịch HCl, dung dịch Zn(NO3)2. Kim loại M là
A. Cu. B. Mg. C. Ag. D. Zn.
Câu 9: Este nào sau đây có mùi dứa chín?
A. etyl isovalerat. B. etyl propionat. C. benzyl axetat. D. metyl axetat.
Câu 10: Khi điều chế kim loại, các ion kim loại đóng vai trò là chất
A. khử. B. bị oxi hoá. C. môi trường. D. bị khử.
Câu 11: Chất không bị nhiệt phân hủy là
A. CaCO3. B. KHCO3. C. KNO3. D. NaCl.
Câu 12: Polime nào sau đây được tổng hợp bằng phản ứng trùng ngưng?
A. Poli(vinyl clorua). B. Polibutađien.
C. Poli(hexametylen-ađipamit). D. Polietilen.
Câu 13: Kali cromat (K2CrO4) là chất rắn có màu
A. đỏ thẫm. B. lục thẫm. C. da cam. D. vàng.
Câu 14: Nhóm những chất khí (hoặc hơi) nào dưới đây đều gây hiệu ứng nhà kính khi nồng độ của chúng trong khí
quyển vượt quá tiêu chuẩn cho phép?
A. CH4 và H2O. B. CO2 và CH4. C. N2 và CO. D. CO2 và O2.
Câu 15: Axit oleic là axit béo có nhiều trong dầu ô liu, dầu macca. Công thức của axit oleic là
A. C3H5(OH)3. B. CH3COOH. C. C17H33COOH. D. C15H31COOH.
Câu 16: Kim loại X có nhiệt độ nóng chảy cao nhất, có thể dùng để sản xuất dây tóc bóng đèn. Kim loại X là
A. Cr. B. Ag. C. Cu. D. W.
Câu 17: Chất nào sau đây chứa liên kết ba trong phân tử?
A. Etan. B. Axetilen. C. Etilen. D. Buta – 1,3 – đien.
Câu 18: Đimetylamin có công thức cấu tạo là
A. (CH3)2NH. B. CH3NHC2H5. C. CH3NH2. D. (C2H5)2NH.
Câu 19: Oxit kim loại nào sau đây tan hoàn toàn trong nước dư tạo thành dung dịch kiềm?
A. BaO. B. Al2O3. C. MgO. D. CuO.
Câu 20: Chất nào sau đây oxi hóa được H2 (Ni, t°) tạo ra sobitol?
A. Tinh bột. B. Glucozơ. C. Xenlulozơ. D. Saccarozơ.
Câu 21: Thí nghiệm nào sau đây không xảy ra phản ứng?
A. Cho thanh kim loại Ag vào dung dịch Fe2(SO4)3.
B. Cho dung dịch Ca(OH)2 vào dung dịch NaHCO3.
C. Cho dung dịch KHSO4 vào dung dịch BaCl2.
D. Cho thanh kim loại Fe vào dung dịch H2SO4 loãng, nguội.
Câu 22: Phát biểu nào sau đây sai?

TRUNG TÂM TIẾP BƯỚC LỚP HÓA 12 NĂM HỌC 2022 - 2023
2
A. Nhỏ dung dịch I2 vào dung dịch hồ tinh bột thì xuất hiện màu xanh tím.
B. Phân tử xenlulozơ gồm nhiều mắt xích α–glucozơ liên kết với nhau.
C. Thủy phân hoàn toàn saccarozơ thì thu được glucozơ và fructozơ.
D. Dung dịch glucozơ có khả năng hòa tan được đồng(II) hiđroxit.
Câu 23: Trong công nghiệp, saccarozơ là nguyên liệu để thủy phân thành glucozơ và fructozơ dùng trong kĩ thuật tráng
gương, ruột phích. Để thu được 20,25 kg glucozơ cần thủy phân m kg saccarozơ với hiệu suất phản ứng là 75%. Giá trị
của m là
A. 45,60. B. 85,50. C. 42,75. D. 51,30.
Câu 24: Cho 5,15 gam amino axit X tác dụng vừa hết với dung dịch NaOH, thu được 6,25 gam muối. Công thức của X là
A. H2NCH2CH2COOH. B. H2NCH2COOH.
C. H2NCH(CH3)COOH. D. H2NCH2CH2CH2COOH.
Câu 25: Cho X và Y là hai cacbohiđrat. Biết X là chất rắn, ở dạng bột vô định hình, màu trắng, không tan trong nước
lạnh. Còn Y là loại đường phổ biến nhất, có trong nhiều loài thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa
thốt nốt. Tên gọi của X, Y lần lượt là
A. tinh bột và glucozơ. B. tinh bột và saccarozơ. C. saccarozơ và fructozơ. D. xenlulozơ và saccarozơ.
Câu 26: Chất X có công thức phân tử C4H6O2. Khi X tác dụng với dung dịch NaOH sinh ra chất Y có công thức phân tử
C3H3O2Na. Chất X có tên gọi là
A. metyl axetat. B. metyl acrylat. C. etyl acrylat. D. metyl metacrylat.
Câu 27: Cho 4 dung dịch riêng biệt: Na2SO4, NaHSO4, AgNO3 và NaOH. Số dung dịch có khả năng phản ứng với
Fe(NO3)2 là
A. 1. B. 4. C. 2. D. 3.
Câu 28: Khi xà phòng hóa 2,52 gam hỗn hợp E gồm chất béo X (tạo từ axit béo Y và glixerol) và axit béo Y thì thu được
0,184 gam glixerol. Biết 1 gam E thì phản ứng vừa đủ với 200 mg KOH. Khối lượng KOH phản ứng với lượng axit có
trong 2,52 gam hỗn hợp E là
A. 0,056 gam. B. 0,112 gam. C. 0,168 gam. D. 0,224 gam.
Câu 29: Cho hỗn hợp X gồm Fe2O3, Al2O3, Cu tác dụng với dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu
được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng, dư) trong điều kiện không có oxi
thu được kết tủa gồm
A. Fe(OH)2, Cu(OH)2 và Al(OH)3. B. Fe(OH)2 và Cu(OH)2
C. Fe(OH)3 và Al(OH)3. D. Fe(OH)3.
Câu 30: Cho các phát biểu sau:
(1) Đipeptit Gly-Ala có phản ứng màu biure.
(2) PVC được điều chế bằng phản ứng trùng ngưng vinyl clorua.
(3) Metyl fomat và glucozơ có cùng công thức đơn giản nhất.
(4) Metylamin có lực bazơ mạnh hơn phenylamin.
(5) Thủy phân saccarozơ chỉ thu được glucozơ.
(6) Metyl metacrylat làm mất màu dung dịch brom.
Số phát biểu đúng là
A. 5. B. 4. C. 6. D. 3.
Câu 31: Cho các phát biểu sau:
(1) Phân đạm amoni không nên bón cho loại đất chua.
(2) Dung dịch hỗn hợp FeSO4 và H2SO4 làm mất màu dung dịch KMnO4.
(3) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa ba muối.
(4) Hỗn hợp Al và BaO (tỉ lệ mol tương ứng là 1: 1) tan hoàn toàn trong nước dư.
(5) Điện phân dung dịch NaCl, thu được khí hiđro tại catot.
(6) Dùng Ba(OH)2 có thể phân biệt hai dung dịch NaHCO3 và Na2SO4
Số phát biểu đúng là
A. 4. B. 5. C. 3. D. 6.
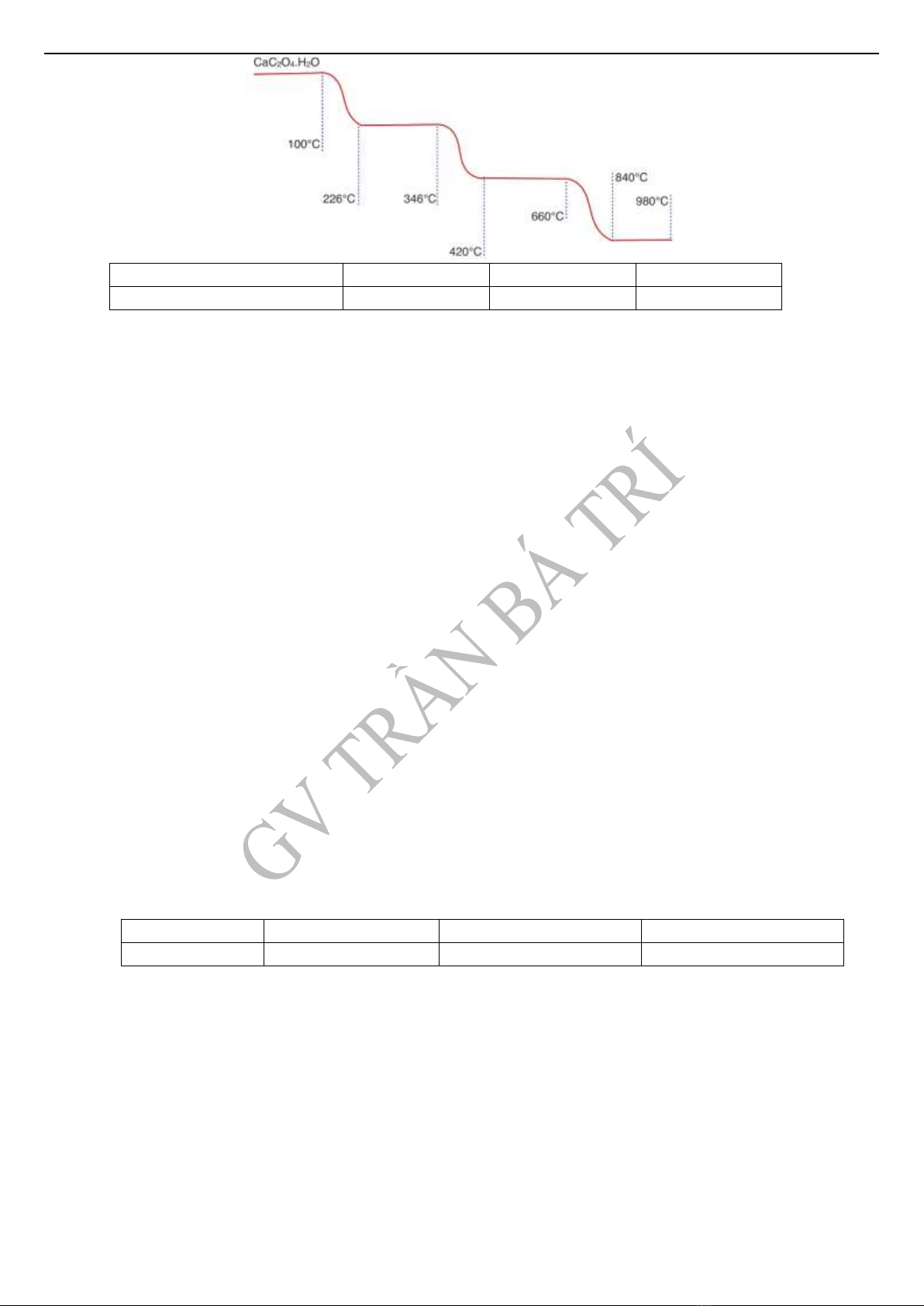
Câu 32: Trong phương pháp phân tích nhiệt, một chất rắn khối lượng m1 được gia nhiệt, thu được chất rắn mới khối
lượng m2 và chất khí hoặc hơi. Giản đồ phân tích nhiệt hình dưới cho biết sự biến đổi khối lượng của canxi oxalat ngậm
nước CaC2O4.H2O trong môi trường khí trơ theo nhiệt độ:
TRUNG TÂM TIẾP BƯỚC LỚP HÓA 12 NĂM HỌC 2022 - 2023
3
Nhiệt độ
2260C
4200C
8400C
Lượng m2 còn lại so với m1
87,7%
68,5%
38,4%
Cho các phương trình hóa học (theo đúng tỉ lệ mol) ứng với ba giai đoạn phân ứng có kèm theo thay đổi khối lượng của
các chất rắn như sau:
2 4 2 1 1
(1) CaC O .H O R + K
0
t
1 2 2
(2) R R + K
0
t
2 3 3
(3) R R + K
Kí hiệu R cho các chất rắn, K cho các chất khí hoặc hơi. Trong các phát biểu sau, phát biểu nào đúng?
A. K2 là oxit axit. B. R2 không tan trong axit.
C. R3 tan trong nước tạo mỗi trường trung tính. D. K3 là chất khí nặng hơn không khí.
Câu 33: Trong một vụ mùa để canh tác 1 sào bắc bộ (500m2) ruộng lúa thì thông thường người nông dân cần bón phân
hoá học 4 lần
– Bón lót trước khi gieo cấy thường bón đậm, bón khoảng 10 kg NPK loại 16 – 16 – 8 kết hợp 2kg ure, bón xong nhất
thiết phải dùng cây chuối hoặc thanh gỗ kéo để vùi phân vào đất nhằm hạn chế mất phân.
– Bón thúc lần 1 bón sau khi cấy 10 – 12 ngày, bón từ 8 kg NPK 16 – 16 – 8.
– Bón thúc lần 2 sau lần 1 khoảng 7 – 8 ngày, lần này bón từ 7 kg NPK 16 – 16 – 8 kết hợp 4 kg Ure.
– Bón đón đòng khi lúa 38 – 42 ngày. Bón 4 kg kali (KCl) kết hợp với 2 kg Ure.
Biết độ dinh dưỡng phân Kali là 47%, độ dinh dưỡng phân Ure là 46%.
Tổng khối lượng (N + P + K) cần bón cho 1 sào bắc bộ ở trên là
A. 10,00 kg. B. 12,65 kg. C. 37,00 kg. D. 15,56 kg.
Câu 34: Hỗn hợp E gồm hai axit oleic, axit panmitic và chất béo Y (có tỉ lệ mol
Axit Y
n : n 5 : 4=
). Cho E vào dung dịch
NaOH dư (đun nóng), sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch Z. Cô cạn dung dịch Z thu được chất rắn T
có khối lượng 53,06 gam chứa 3 chất rắn khan. Đốt cháy hoàn toàn T thu được Na2CO3; 2,795 mol CO2 và 2,775 mol
H2O. Phần trăm khối lượng của Y trong E có giá trị gần nhất với giá trị nào sau đây?
A. 71. B. 72. C. 73. D. 70.
Câu 35: Cho m gam hỗn hợp X gồm Na, Na2O, Ba, BaO (O chiếm 8,5% về khối lượng) vào lượng dư nước thu được
dung dịch Y và 2,52 lít khí. Sục từ từ khí CO2 vào dung dịch Y, kết quả thí nghiệm được ghi lại theo bảng sau:
Số mol CO2
0,1
0,1+ x
0,38
Số mol kết tủa
a
1,1a
a
Giá trị của m là
A. 28. B. 20. C. 32. D. 24.
Câu 78: Cho các chất hữu cơ X, Y, Z, T, E thoả mãn các phương trình hoá học sau:
(1) C6H10O4 + 2NaOH
o
t
X + Y + Z
(2) X + NaOH
o
CaO, t
CH4 + Na2CO3
(3) Y + CuO
o
t
T + Cu + H2O
(4) T + 2AgNO3 + 3NH3 + H2O
o
t
CH3COONH4 + 2Ag + 2NH4NO3
(5) Z + HCl → M + NaCl
Cho các phát biểu sau:
(a) 1 mol M có khả năng phản ứng tối đa với 2 mol kim loại Na.
(b) Dung dịch M làm quỳ tím hóa đỏ.
TRUNG TÂM TIẾP BƯỚC LỚP HÓA 12 NĂM HỌC 2022 - 2023
4
(c) Khối lượng phân tử của Y là 60.
(d) Z là hợp chất hữu cơ đa chức.
Số nhận định đúng là
A. 2. B. 3. C. 4. D. 1.
Câu 37: Xăng sinh học E5 (chứa 5% etanol về thể tích; còn lại là xăng, giả thiết chỉ là octan). Khi được đốt cháy hoàn
toàn, 1 mol etanol tỏa ra nhiệt lượng là 1365,0 kJ và 1 mol octan tỏa ra lượng nhiệt là 5928,7 kJ. Trung bình, một chiếc xe
máy di chuyển được 1km thì cần một nhiệt lượng chuyển thành công cơ học độ lớn là 211,8 kJ. Nếu xe máy đó đã sử
dụng 4,5 lít xăng E5 ở trên thì quãng đường di chuyển được là bao nhiêu km, biết hiệu suất sử dụng nhiên liệu của động
cơ là 25%; khối lượng riêng của etanol là 0,8 g/ml; của octan là 0,7g/ml.
A. 250 km. B. 180 km. C. 200 km. D. 190 km.
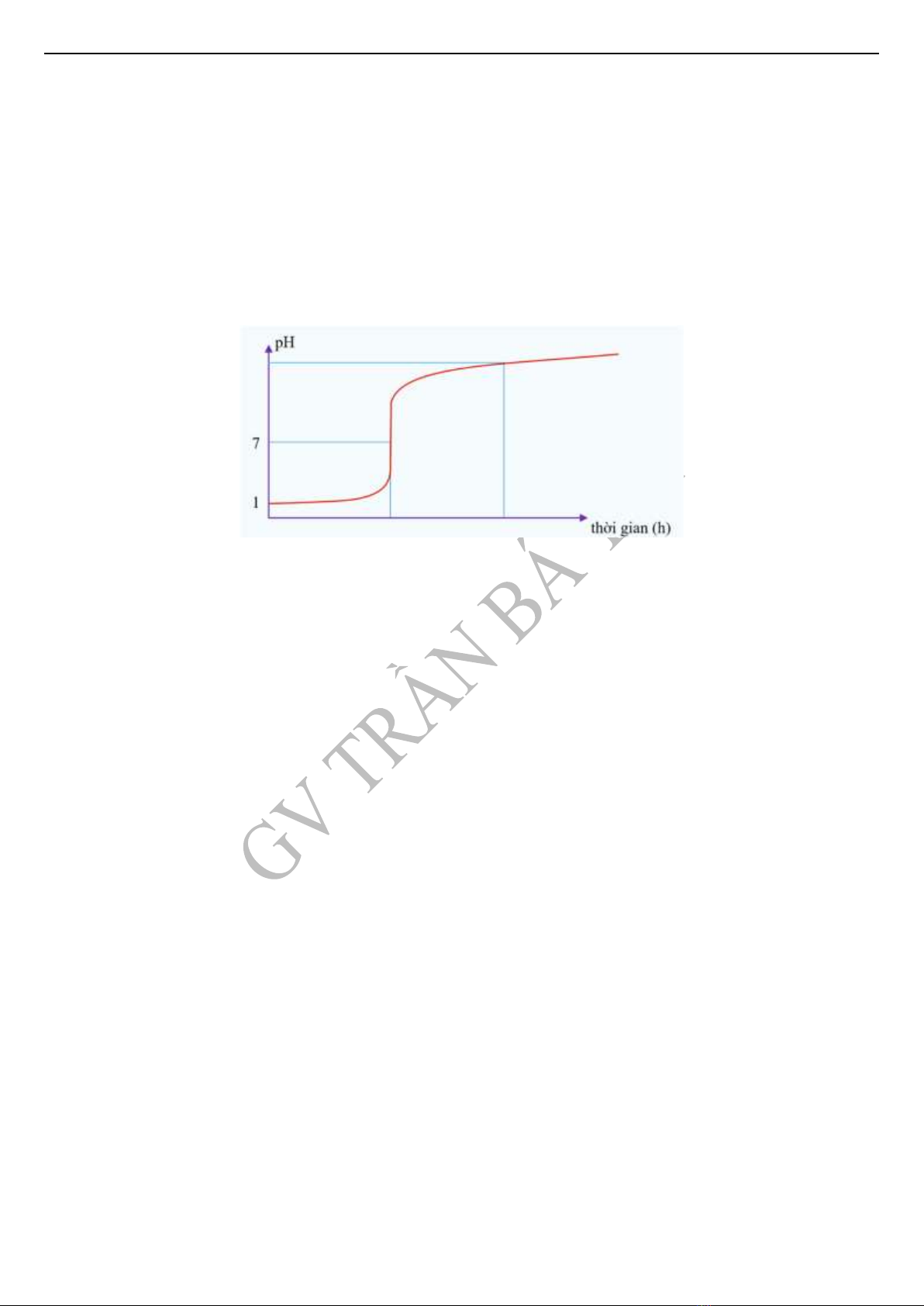
Câu 38: Điện phân (với điện cực trơ, màng ngăn và có dòng điện ổn định) 3 lít dung dịch chứa H2SO4 và NaCl (tỉ lệ mol
3:8). Sự biến đổi pH của dung dịch theo thời gian điện phân như sau:
0 3 6
Sau 6h điện phân, tổng số mol khí thoát ra tại hai điện cực là a mol. Biết rằng các khí sinh ra đều thoát ra hoàn toàn khỏi
dung dịch và lượng nước bay hơi không đáng kể. Giá trị của a là
A. 0,60. B. 0,55. C. 0,65. D. 0,70.
Câu 39: Hỗn hợp X gồm Cu, CuO, Fe, Fe2O3. Hòa tan hết m gam X trong dung dịch chứa 1,05 mol HCl (dư 25% so với
lượng phản ứng), thu được 0,07 mol H2 và 250 gam dung dịch Y. Mặt khác, hòa tan hết m gam X trong dung dịch H2SO4
đặc nóng, thu được dung dịch Z (chứa 3 chất tan) và 0,1 mol SO2 (sản phẩm khử duy nhất của H2SO4). Cho Z tác dụng
với dung dịch Ba(OH)2 dư, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 136,85 gam
chất rắn. Nồng độ phần trăm FeCl3 trong Y là
A. 3,25%. B. 5,20%. C. 3,90%. D. 2,60%.
Câu 40: Hỗn hợp T gồm ba este mạch hở gồm X (đơn chức), Y (hai chức), Z (ba chức), đều được tạo thành từ ancol và
axit cacboxylic. Xà phòng hóa hoàn toàn m gam T bằng dung dịch NaOH vừa đủ, thu được hỗn hợp E gồm 2 ancol no (có
số nguyên tử cacbon liên tiếp) và hỗn hợp muối F gồm 2 muối có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn hỗn hợp
E thu được 1 mol CO2 và 1,8 mol H2O. Đốt cháy toàn bộ F, thu được H2O, Na2CO3 và 0,8 mol CO2. Phần trăm khối
lượng của Y trong T có giá trị là
A. 28,05%. B. 11,72%. C. 60,22%. D. 24,50%.





![Bài tập so sánh hơn và so sánh nhất của tính từ [kèm đáp án/mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250808/nhatlinhluong27@gmail.com/135x160/77671754900604.jpg)
![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)




![Tài liệu Lý thuyết và Bài tập Tiếng Anh lớp 6 [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250802/hoihoangdang@gmail.com/135x160/18041754292798.jpg)




