Trang 1/3 - Mã đề thi 303
ĐỀ CHÍNH THỨC
TRƯỜNG THPT QUẾ SƠN
TỔ: HOÁ – SINH – CNNN
(Đề gồm có 03 trang)
KIỂM TRA CUỐI KỲ I- NĂM HỌC 2023-2024
Môn: HOÁ HỌC – Lớp 10
Thời gian làm bài: 45 phút
(Không kể thời gian giao đề)
MÃ ĐỀ 303
I. PHẦN TRẮC NGHIỆM ( 21 câu; 7 điểm)
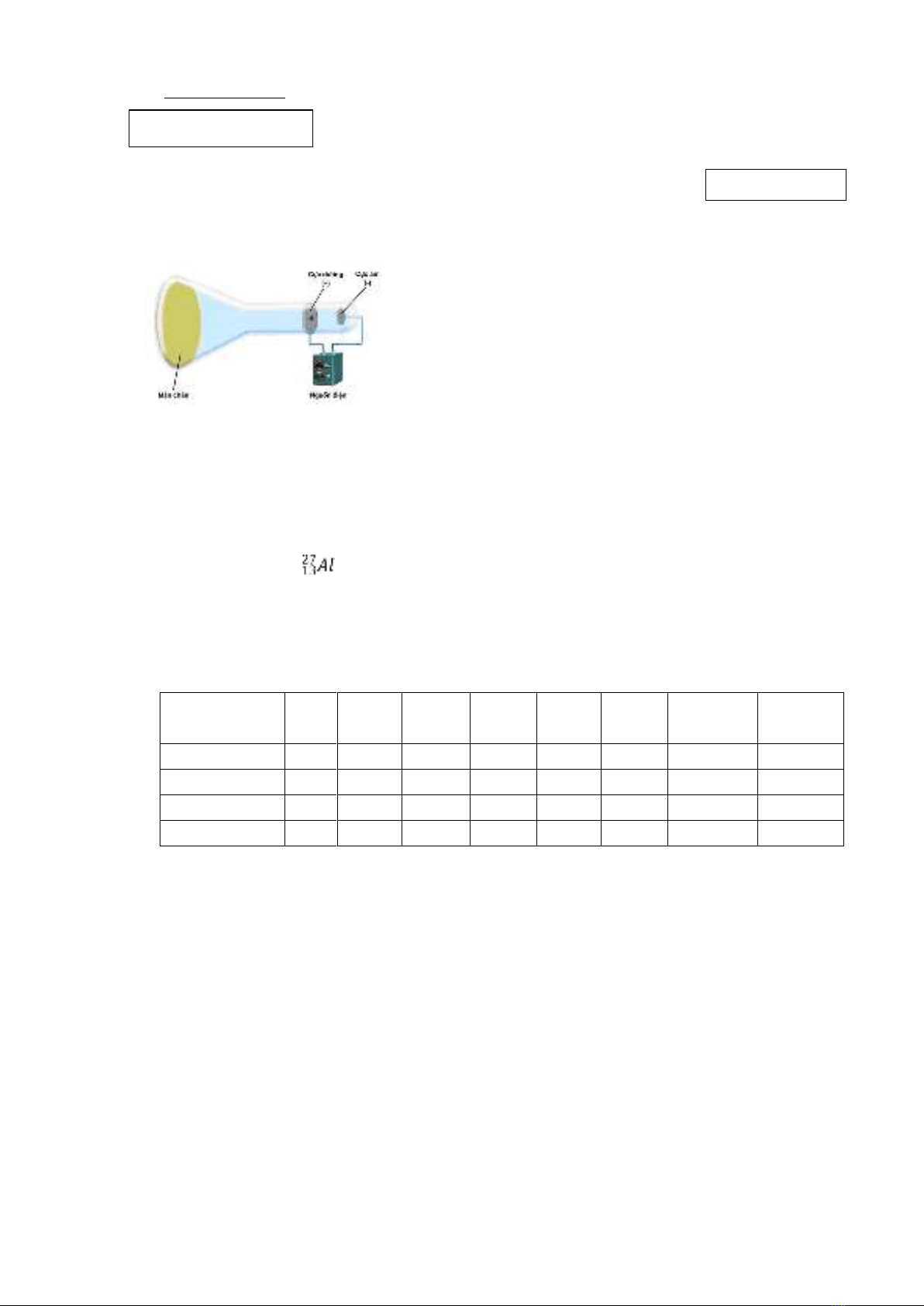
Câu 1: Hình vẽ trên mô tả thí nghiệm tìm ra
A. hạt electron. B. hạt proton.
C. hạt neutron. D. hạt nhân nguyên t.
Câu 2: Trong bảng tuần hoàn, nhóm là dãy các nguyên tố mà nguyên t có
A. cùng số electron lớp ngoài cùng. B. cấu hình electron tương tự nhau.
C. cùng số lớp electron. D. cùng số electron.
Câu 3: Trong nguyên t tổng số hạt mang điện nhiều hơn số hạt không mang điện là
A. 12 hạt. B. 1 hạt. C. 14 hạt. D. 13 hạt.
Câu 4: Một phần của Bảng tuần hoàn với ký hiệu hóa học của các nguyên tố được thay
bằng các chữ cái X, Y, Z, T, Q, G được trình bày trong bảng sau:
Nhóm
Chu kì
IA
IIA
IIIA
IVA
VA
VIA
VIIA
VIIIA
1
X
2
Z
3
Q
G
T
4
Y
Phát biểu nào sau đây sai?
A. Z, T là nguyên tố phi kim. B. Q và Y có cùng số electron hóa trị.
C. Tính phi kim của T > G > Q. D. X là nguyên tố kim loại.
Câu 5: Nguyên tố hóa học là tp hợp những nguyên t có cùng
A. số khối. B. số neutron.
C. nguyên t khối. D. điện tích hạt nhân.
Câu 6: Nguyên t X có phân lớp electron ngoài cùng là 3p5. Nhn xét nào sau đây sai khi
nói về nguyên t X?
A. Hạt nhân nguyên t X có 17 electron. B. X có 3 lớp electron, 7 electron hoá trị.
C. Lớp ngoài cùng của X có 7 electron. D. X nằm ở ô 17, nhóm VIIA, chu kì 3.
Câu 7: Trong số các hydroxide: H2SiO3, H3PO4, H2SO4, HClO4, hydroxide nào có tính acid
mạnh nhất?
A. H2SiO3. B. H3PO4. C. HClO4. D. H2SO4.






































