Họ và tên:………………………………….Số báo danh………………… Lớp…………….
PHẦN I. CÂU TRẮC NGHIỆM NHIỀU PHƯƠNG ÁN LỰA CHỌN. Thí sinh trả lời từ câu 1 đến câu
12. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Chất nào sau đây là dẫn xuất của hydrocarbon ?
A. CH≡CH. B. CH3COOC2H5.C. CH3-CH2-CH3.D. CH2=CH2.
Câu 2: Cho các phát biểu sau:
(a) Sulfur là chất rắn, màu trắng, không tan trong nước.
(b) Sulfur và sulfur dioxide vừa có tính oxi hóa, vừa có tính khử.
(c) Khi phản ứng với hydrogen, sulfur thể hiện tính oxi hóa
(d) Nước thải sinh hoạt là một trong các nguồn phát thải khí SO2.
Số phát biểu đúng là
A. 2. B. 1. C. 4. D. 3.
Câu 3: Các oxide của nitrogen không được tạo thành trong trường hợp nào sau đây?
A. Mưa dông, sấm sét.
B. Đốt cháy các nhiên liệu hóa thạch.
C. Núi lửa phun trào.
D. Xả thải nước thải công nghiệp chưa qua xử lí.
Câu 4: Cặp chất nào dưới đây là đồng đẳng của nhau?
A.
3
CH COOH
và
3 3
CH COOCH
.B.
3 2
CH CH CHO
và
3 2 3
CH COCH CH
.
C.
3 2
CH CH OH
và
2 2
HOCH CH OH
.D.
3
CH OH
và
3 2 2 2
CH CH CH CH OH
.
Câu 5: Hợp chất hữu cơ nào sau đây thể hiện tính chất hóa học đặc trưng của nhóm chức của carboxylic
acid?
A. CH2=CH-CHO. B. HCOOCH3.C. CH3COONa. D. C17H33COOH.
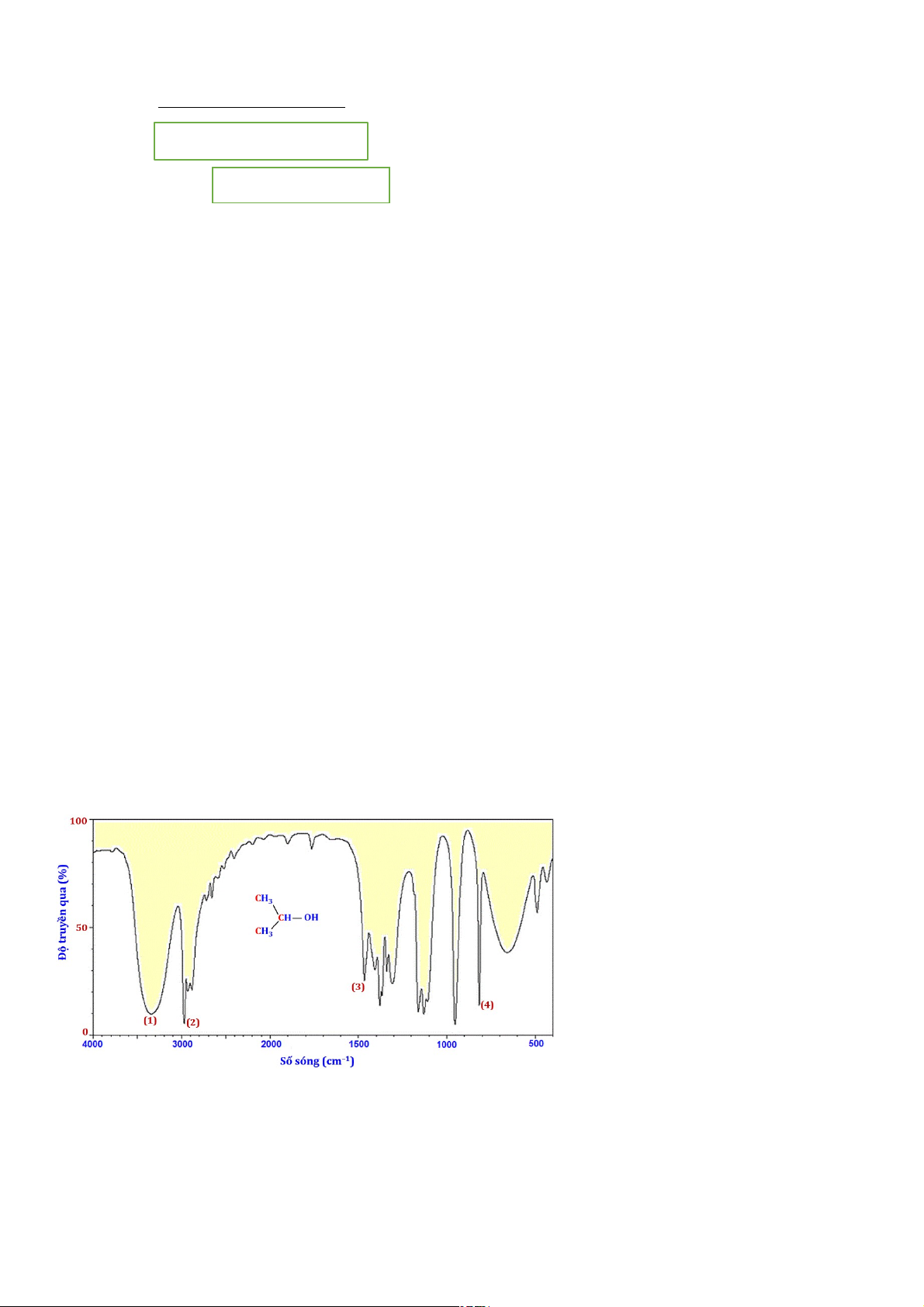
Câu 6: Dựa vào phổ hồng ngoại (IR) của hợp chất X có công thức CH3CH(OH)CH3 dưới đây, hãy chỉ ra
peak nào giúp dự đoán X có nhóm -OH?
A. (2). B. (3). C. (4). D. (1).
Câu 7: Phát biểu nào sau đây không đúng?
A. Dưới tác dụng của nhiệt, muối ammonium đều bị phân hủy thành ammonia và acid.
B. Các muối ammonium đều dễ tan trong nước.
C. Có thể dùng muối ammonium để đều chế NH3 trong phòng thí nghiệm.
D. Các muối ammonium khi tan trong nước đều phân li hoàn toàn thành ion.
Câu 8: Cặp chất nào sau đây là đồng phân của nhau?
Trang 1/4 - Mã đề 304
SỞ GD&ĐT QUẢNG NAM KIỂM TRA CUỐI KỲ 1
TRƯỜNG THPT TRẦN HƯNG ĐẠO NĂM HỌC 2024 - 2025
ĐỀ CHÍNH THỨC Môn thi: HÓA 11
Thời gian làm bài: 45 phút (Không kể thời gian phát đề)
(Đề thi có 04 trang)
Mã đề: 304







































