MA TRẬN, BẢN ĐẶC TẢ VÀ ĐỀ KIỂM TRA ĐỊNH KÌ
MÔN: HÓA HỌC 8 ( Cuối học kì 2)
1. Khung ma trận và đặc tả đề kiểm tra cuối kì II môn Hóa học, lớp 8
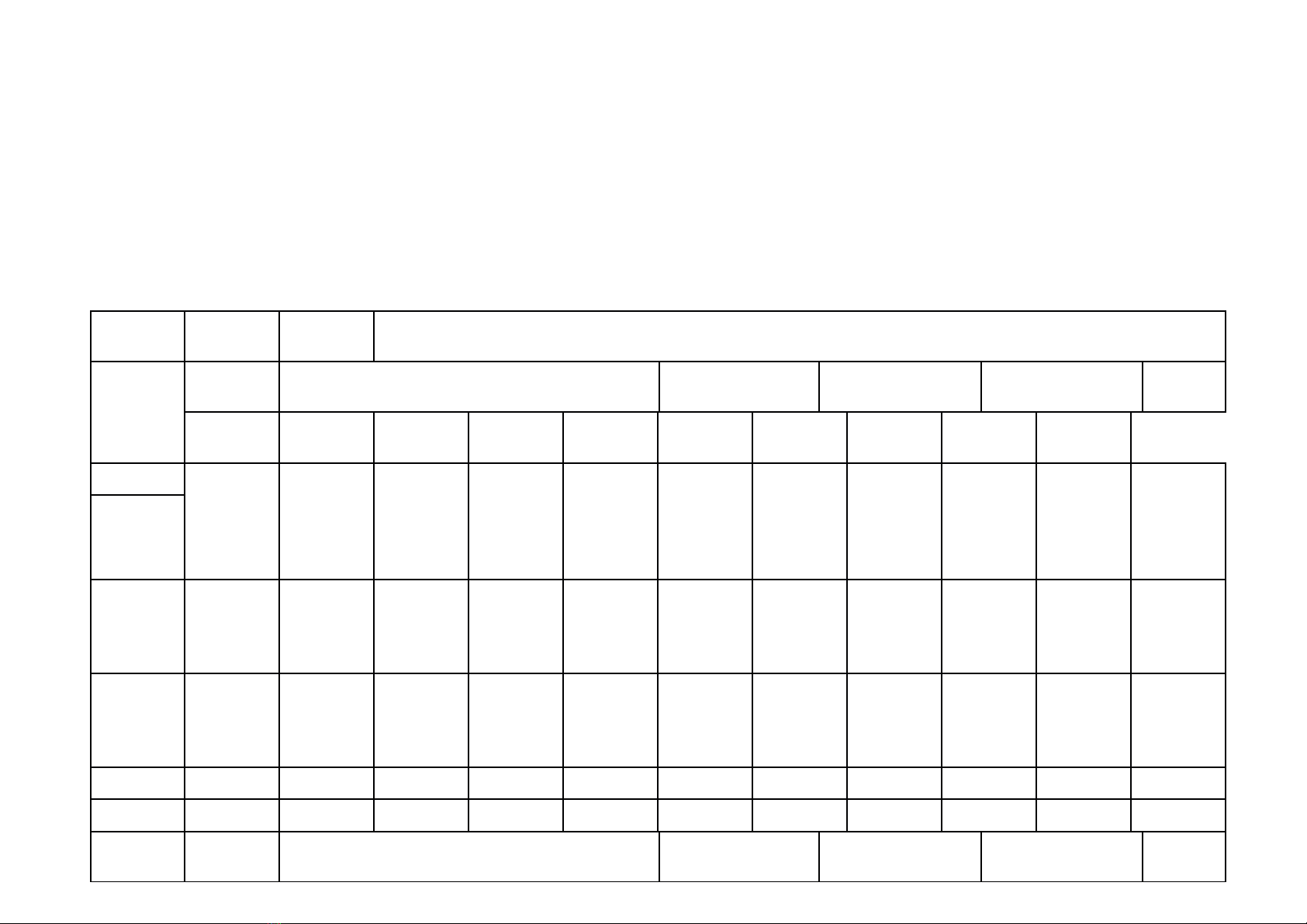
a) Khung ma trận
- Thời điểm kiểm tra: Kiểm tra giữa học kì II (Từ tuần 19 đến tuần 33, từ bài 24 đến bài 44)
- Thời gian làm bài: 45 phút.
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 50% trắc nghiệm, 50% tự luận).
- Cấu trúc: - Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao.
- Phần trắc nghiệm: 5,0 điểm, (gồm 15 câu hỏi: nhận biết: 9 câu, thông hiểu:3 câu, Vận dụng thấp: 3 câu), mỗi câu 0,33
điểm.
- Phần tự luận: 5,0 điểm (nhận biết: 1 điểm, thông hiểu: 2 điểm; Vận dụng thấp: 1 điểm; Vận dụng cao: 1 điểm).
Chủ đề MỨC
ĐỘ
Tổng số
câu Điểm số
Nhận
biết Thông hiểu Vận dụng Vận dụng cao
Tự luận Trắc
nghiệm Tự luận Trắc
nghiệm Tự luận Trắc
nghiệm Tự luận Trắc
nghiệm Tự luận Trắc
nghiệm
Chương
4: oxi –
không
khí (8
tiết)
5(1,66đ) 1(0,33) 6 2đ
Chương
5: hiđro
– nước
(11 tiết)
3(1đ) 2 (2đ) 2(0,66) 0,5 (2 ý)
(1đ) 1(0,33) 0,5 (2 ý)
(1đ 3 6 6đ
Chương
6: dung
dịch (6
tiết)
1(đ) 1(0,33) 1(0,33) 1(0,33) 1 3 2đ
Số câu 1 9 2 3 0,5 3 0,5 4 15 19
Điểm số 1 3 2 1 1 1 1 5 5 10
Tổng số
điểm 4 3 2 1 10 10

b) Bản đặc tả
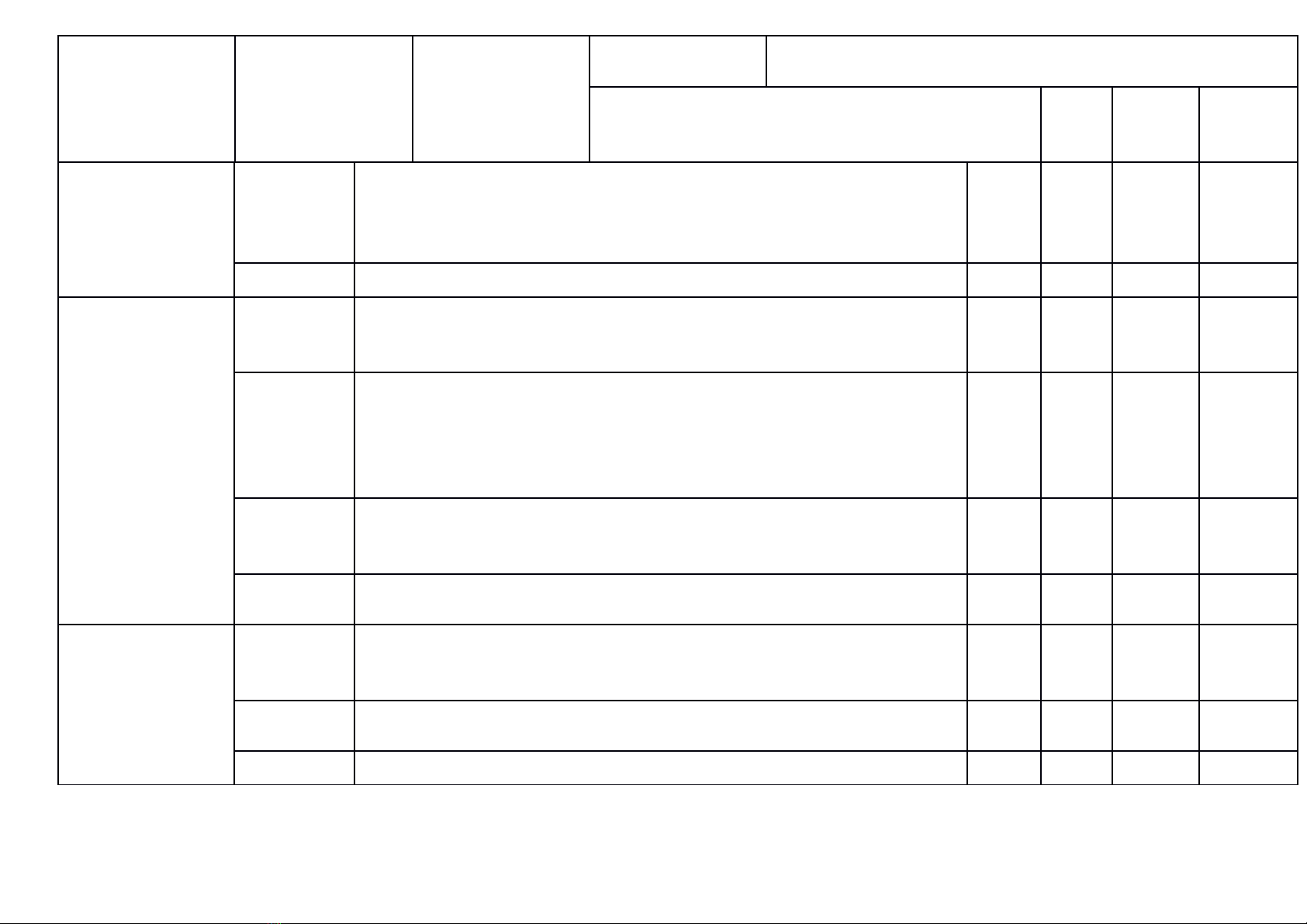
Nội dung Mức độ Yêu cầu cần đạt
Số ý TL/số câu
hỏi TN Câu hỏi
TL
(Số ý)
TN
(Số
câu)
TL
(Số ý)
TN
(Số câu)
Chương 4: oxi –
không khí (8 tiết)
Nhận biết Nhận biết CTHH của chất thuộc loại oxit, oxit bazơ
Nhận biết phản ứng hóa học nào thuộc loại phản ứng hóa hợp
Biết cách thu khi oxi dựa vào TCVL
Biết tính chất vật lý của oxi
2
1
1
1
C1,C5
C2
C3
C6
Vận dụng Tính % về khối lượng của oxi trong hợp chất 1 C4
Chương 5: hiđro –
nước (11 tiết)
Nhận biết Biết trạng thái tồn tại của nước
Biết hóa chất dùng để điều chế khí hiđro trong phòng thí nghiệm
Nhận biết CTHH của chất thuộc loại Oxit, Axit, Bazơ, Muối
1
1
1
C7
C8
C12
Thông
hiểu
Hiểu TCHH của hidro
Hiểu TCHH của nước, TCVL của hidro
Phân loại và gọi tên các hợp chất oxit, axit, bazơ, muối
Hoàn thành các sơ đồ phản ứng và chỉ rõ mỗi phản ứng thuộc loại
phản ứng hóa học nào
1
1
1
1
C17
C18
C9
C11
Vận dụng
Tính được nồng độ phần trăm của dung dịch
Viết PTHH và nhận xét sự đổi màu của chỉ thị 0,5(2
ý)
1
C19a,b
C10
Vận dụng
cao
Tính nồng độ, số mol theo PTHH 0,5(2
ý)
C19c,d
Chương 6: dung
dịch (6 tiết)
Nhận biết
Nhận biết chất cụ thể hòa tan với nhau tạo thành dung dịch
Lấy ví dụ về dung dịch và xác định chất tan, dung môi trong mỗi
dung dịch đó.
1
1
C16
C14
Thông
hiểu
Phân biệt chất nào đóng vai trò chất tan, dung môi trong dung dịch 1 C13
Vận dụng Tính được độ tan của một chất ở một nhiệt độ xác định 1 C15
c/ Đề

Trường THCS Thạnh Mỹ KIỂM TRA CUỐI HỌC KÌ II
Họ và tên:............................................... Năm học: 2022-2023
SBD:................... Phòng thi:................. Môn: Hóa học 8
Lớp:........................................................ Thời gian: 45 phút (Không kể thời gian giao đề)
I. TRẮC NGHIỆM: (5.0 điểm) Chọn đáp án đúng nhất cho các câu sau:
Câu 1. Dãy chất nào sau đây chỉ gồm oxit?
A. CaO, HCl, CuO, ZnO. B. K2O, NaCl, MgO,SO3.
C. MgO, SO2, NaOH, Fe(OH)3. D. BaO, CO2, MgO,Fe2O3.
Câu 2. Phản ứng nào sau đây thuộc loại phản ứng hóa hợp?
A. 3Fe + 2O2 Fe3O4 B. 2KClO3 2KCl + 3O2
C. HCl + NaOH NaCl + H2O D. Mg + 2HCl MgCl2 + H2
Câu 3. Để thu khí oxi bằng cách đẩy không khí, ta đặt ống nghiệm thu khí như thế nào?
A. Ngửa lên. B. Úp xuống. C. Nằm ngang. D. Đặt sao cũng được.
Câu 4. Oxit nào dưới đây có % về khối lượng oxi thấp nhất ?
A. N2O B. NO C. N2O5 D. NO2
Câu 5. Dãy chất nào sau đây là oxit bazơ ?
A. CaO, ZnO, CO2, MgO, CuO B. CaO, CuO, Na2O, BaO, Fe2O3
C. N2O, P2O5, SO2, CuO, SO3 D. MgO, NO2, Na2O, Al2O3, Fe2O3
Câu 6. Điều nào sau đây nói sai về khí oxi ?
A. Oxi là chất khí không màu, không mùi. B. Oxi là chất khí năpng hơn không khí.
C. Khí oxi tan vô hạn trong nước. D. Khí oxi còn gọi là dưỡng khí.
Câu 7. Ở nhiệt độ thường, nước ở trạng thái
A. rắn. B. lỏng. C. khí. D. hơi nước.
Câu 8. Hóa chất dùng để điều chế khí hiđro trong phòng thí nghiệm là
A. Zn và HCl. B. Cu và H2SO4. C. Al và H2O. D. FeO và HCl.
Câu 9. Khí hiđro tác dụng được với tất cả các chất nào trong dãy các chất sau?
A. CuO, HgO, H2O. B. CuO, HgO, O2. C. CuO, HgO, H2SO4. D. CuO, HgO, NaOH.
Câu 10. Hòa tan 34,2 gam bari hiđroxit vào 165,8 gam nước. Nồng độ phần trăm của dung dịch bari hiđroxit thu được là
A. 0,206%. B. 20,6%. C. 17,1%. D. 0,171%.
Câu 11. Khi cho mẫu natri vào nước, có chất khí thoát ra, khí đó không có tính chất nào sau đây?
A. Nhẹ nhất trong tất cả các chất khí. B. Làm đục nước vôi trong.

C. Cháy trong không khí với ngọn lửa màu xanh. D. Tan rất ít trong nước.
Câu 12. Dãy hợp chất nào sau đây lần lượt là oxit, axit, bazơ, muối ?
A. BaO, MgO, NaOH, KOH. B. NaOH, HCl, NaCl, H2SO4
C. CuO, NaOH, H2SO4, NaCl. D. CaO, H2SO4, NaOH, NaCl
Câu 13. Pha trộn 25 ml rượu etylic nguyên chất vào 75 ml nước ta được dung dịch rượu, vậy khẳng định nào sau đây là đúng ?
A. Nước là chất tan, rượu là dung môi. B. Nước là dung môi, rượu là chất tan
C. Nước và rượu đều là chất tan D. Nước và rượu đều là dung môi
Câu 14. Hai chất không thể hòa tan với nhau tạo thành dung dịch là
A. nước và đường. B. dầu ăn và xăng. C. rượu và nước. D. dầu ăn và cát.
Câu 15. Ở 200C hoà tan 40g KNO3 vào trong 95g nước thì được dung dịch bão hoà. Độ tan của KNO3 ở nhiệt độ 200C là
A. 29,6g B. 21,1g C. 42,1g D. 63,2g
II. TỰ LUẬN (5.0 điểm)
Câu 16. (1đ) Hãy kể 2 dung dịch và xác định chất tan, dung môi trong mỗi dung dịch đó.
Câu 17. (1đ) Phân loại và gọi tên các hợp chất sau: FeSO4, H2SO3, MgO, NaOH.
Câu 18. (1đ) Hoàn thành các sơ đồ phản ứng sau và chỉ rõ mỗi phản ứng thuộc loại phản ứng hóa học nào?
a. Al + O2 ?
b. KMnO4 ? + ? + ?
c. CuO + ? Cu + ?
d. ? + H2O ? + H2
Câu 19. (2đ) Cho 10 gam lưu huỳnh trioxit (SO3) tác dụng hết với nước thu được dung dịch axit sunfuric (H2SO4)
a. Hãy viết phương trình hóa học của phản ứng xảy ra.
b. Cho quỳ tím vào sản phẩm của phản ứng trên thì có hiện tượng như thế nào? Vì sao?
c. Tính nồng độ mol của 500ml dung dịch axit sunfuric ở trên?
d. Nếu lấy cùng một khối lượng nhôm, sắt tác dụng hết với lượng axit sunfuric đã pha loãng thì kim loại nào cho nhiều khí hiđro hơn?
(Cho nguyên tử khối của các nguyên tố: S=32, O=16; H=1, Al=27, Fe=56,
K=39, N=14, Ba=137)
Bài làm:
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………












![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



