Höôùng daãn giaûi ñeà soá 5
Câu 1: Dùng công thức: =
CO2
H2
O
Ö ĐS:A
Câu 2: Cần nhớ:
3
12 2
4
;HNO
SS SO
+
−−
⎯⎯⎯→ −
Ta có sơ đồ nhẩm: FeS2 Fe3+ + 2SO4
2- (1)
0,05mol 0,05mol 0,1mol
Cu
2S Cu2+ + SO4
2- (2)
0,1mol 0,1mol 0,1mol
BaSO
4: 0,2mol
(1), (2), đề => Kết tủa gồm: Fe(OH)3: 0,05mol
Cu(OH)
2: 0,1mol
Ö mkết tủa = 233.0,2 + 107.0,05 + 98. 0,1= 61,75
Ö ĐS: D
Câu 3: Mọi hợp chất hữu cơ có 1 liên kết π đốt đều có nCO2 = nH2O
Ö ĐS: B
Câu 4: 2 – metyl butadien – 1,3
CH2 = C – HC – CH2 tạo được 3 sản phẩm cộng với Br2 theo tỉ lệ 1:1
CH3
Ö ĐS: C
Câu 5: Ta nhẩm được nCO2 = nBaCO3↓ = = 0,03mol
Ö nH2O = = 0,03mol
Ö
CO2 =
H2O
Ö ĐS:A
Câu 6: Với Z ≤ 20 nguyên tố có 2 electron độc thân có cấu hình e phân lớp ngoài cùng là:
2p2 ; 2p4; 3p2 ; ;3p4
Ö Nguyên tố: C, Si, O, S
Ö ĐS: D
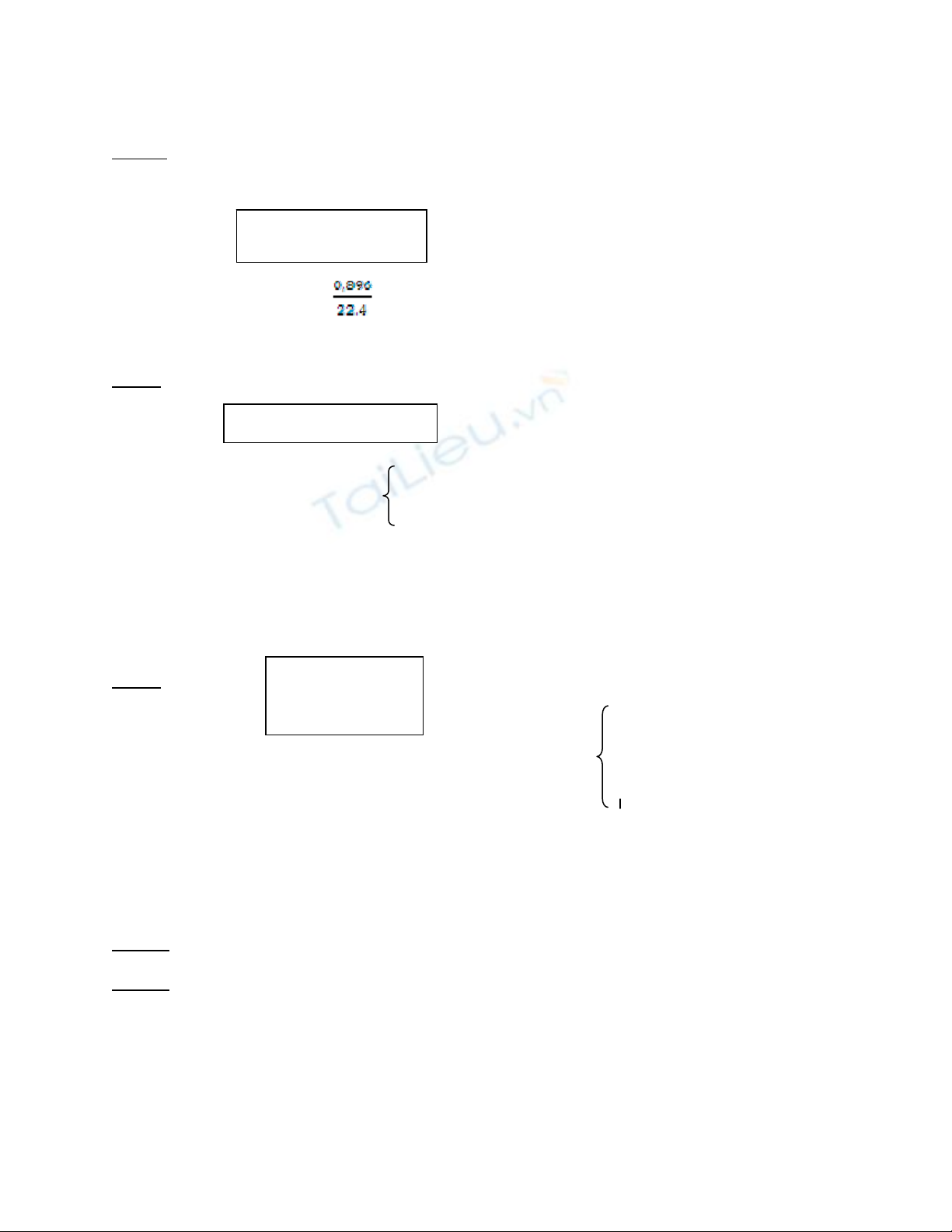
Câu 7:
Cần nhớ: Kim loại phản ứng với HCl có
mMuối = mKL pư + 71.n
H2
Ö mKL pư = 5,865 – 71. = 3,016
Ö ĐS: B
Câu 8:
CTTQ: (*)
CnH2n + 2 - 2a – m(CHO)m
a = 0
Anđehit no 2 chức có:
m = 2
(*) => CTTQ: CnH2n(CHO)2 => ĐS:C
Câu 9: Ta nên nhớ:
CH
3COOH
X(C, H, O)
%O=53,33
=> CTN: (CH2O)n
Theo đề =>X: C2H4O2 với C2H4O2 có 3 công thức phân tử: HCOO – CH3
CH
2 – CHO
OH
Chỉ có C2H6O là thoả điều kiện đề bài (C2H5OH → CH3COOH)
Đaùp aùn : C
Câu 10: Dể thấy C3H6O2 có 1 liên kết π nên chỉ có đáp aùn a là thoả mãn
Câu 11:
• Ở nhiệt độ thường
Cl2 + 2KOH → KClO + KCl + H2O
• Ở nhiệt độ cao
3Cl2 + 6KOH → KClO3 + 5KCl + 3H2O

Theo đề => ĐS: B
Câu 12:
Pư: CO2 + NaOH = NaHCO3 (1)
x x x
CO
2 + 2NaOH = Na2CO3 + H2O (2)
y 2y y
CO2 = x + y = 0,1 x = 0,1
Có =>
NaOH = x + 2y = 0,15 y = 0,05
Ö mMuối = 84x + 106y = 13,7g
Ö ĐS: D
Câu 13: Với CxHyOzNtClu
0 < y ≤ 2x + 2 + t - u
Điều kiện tồn tại:
y + t + u = số chẳn
Ö C3H6O2N sai
Ö ĐS:A
Câu 14: B
Từ phản ứng đốt amin có:
Số C: Số H: Số N = nCO2 : 2nH2O : 2nN2
= 0,2:0,8:0,2
= 1:4:1
Câu 15: B: CH3 – CH – COOH: Alanin
NH2
Câu 16: Tổng Quát
M – ne → Mn+
X +me → Xm-
Số proton trong nguyên tử và ion: không đổi
Ö P X2- = P X = 10 + 2 = 12
P Y- = P Y = 10 -1 = 9
Ö ĐS: B

Câu 17: A tạo CH2 = CH và còn CH3OH
B, D: sinh nhiều hơn 1 olefin
Ö ĐS: B
Câu 18: Dùng sơ đồ nhẩm tỉ lệ mol:
amol C3H8 44 7
51
bmol C4H10 58 7
Ö = = 1 => ĐS: A
Câu 19: n = n = 0,2mol
Al2(SO4)3 SO42-
Ö ĐS: A
Câu 20: Alanin:không đổi màu quì tím
Ö ĐS: D
Câu 21:
Al phản ứng với HCl; ddNaOH → H2
FeS phản ứng với HCl → H2S
(NH4)2CO3 → NH3; CO2
Ö ĐS: C
Câu 22:
n H2= = 0,3
Ö ĐS: C
C âu 23: Dễ thấy hết , CH3C OOH c òn nguyên
Ö dd sau gồm: CH3COOH: 0,1mol
HBr: 0,3mol
Ö VddNaOH = 2000ml
Ö ĐS:A
Câu 24: nHClbđ = = 0,2mol
Ta có nHClpư =2.nH2 = 0,2mol

Ö HCl: hết
Ö n Mgpư = nH2 = 0,1mol
Ö mCu ≤ 8 – 0,1.24 = 5,6
Ö ĐS:A
Câu 25:
nH2 = ½ nB => B: đơn chức
Ö A: Anđêhyt đơn
Ö A: C3H5CHO có CTCT: CH2 = C – CHO
CH3
Sơ đồ điều chế:
An đehyt → Axit → Este → Thuỷ tinh
Ö ĐS: B
Câu 26: nCO2 = nH2O
Ö Anđehyt có 1 liên kết π
Ö Anđêhyt là đơn, no
Ö ĐS: A
Câu 27: Theo đề X pải đứng sau Fe
Ö X: Ag
Câu 28: Chỉ có A có tỉ lệ số C:số H: số O = 6:8:7
Ö ĐS: A
Câu 29: A
Câu 30: Choïn A do 2 kim loại: Cu, Zn
Câu 31: Do dB/A = 0,7 <1
Ö B: olefin vì A đơn
Ö ĐS: B
Câu 32:
=
CO2 = =
H2O
C2H5NO4 không đảm bảo hoá trị
Ö ĐS:A
Câu 33: Theo đề Y là rượu => ĐS: C
Câu 34: A



![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)










![Phiếu bài tập cuối tuần Tiếng Việt 1 tuần 2 đề 2: [Hướng dẫn chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250728/thanhha01/135x160/42951755577464.jpg)

