
Bài 6
KH O SÁT V N T C PH N NG TH Y PHÂN ESTERẢ Ậ Ố Ả Ứ Ủ
XÁC Đ NH NĂNG L NG HO T HÓA C A PH N NGỊ ƯỢ Ạ Ủ Ả Ứ
------------------------------
I. M C ĐÍCHỤ
Kh o sát v n t c ph n ng th y phân ester acetat etyl, có acid vô c làm xúc tác haiả ậ ố ả ứ ủ ơ ở
nhi t đ khác nhau, t đó xác đ nh năng ho t hóa Eệ ộ ừ ị ạ a c a ph n ng.ủ ả ứ
II. C S LÝ THUY TƠ Ở Ế
Vi c xác đ nh năng l ng ho t hóa Eệ ị ượ ạ a c a ph n ng d a vào ph ng trình Arrhenius:ủ ả ứ ự ươ
H th c (1) giúp xác đ nh năng l ng ho t hóa Eệ ứ ị ượ ạ a và tr s kị ố * khi đo m t chu i giá tr kộ ỗ ị
ng v i các nhi t đ T khác nhau và bi u di n theo v i h s góc là và tung đ góc là . ứ ớ ệ ộ ể ế ớ ệ ố ộ
Thông th ng nh ng ph n ng có c ch gi ng nhau, th c hi n trong đi u ki n thìươ ữ ả ứ ơ ế ố ự ệ ề ệ
nghi m nh nhau, có tr s Eệ ư ị ố a g n b ng nhauầ ằ
Khi xác đ nh đ c năng l ng ho t hóa Eị ượ ượ ạ a, ta có th xác đ nh kể ị 2 nhi t đ Tở ệ ộ 2 n u bi tế ế
k1 nhi t đ Tở ệ ộ 1. T h th c (1) suy ra:ừ ệ ứ
Ph n ng th y phân ester acetat etyl: CHả ứ ủ 3COOC2H5 hay công th c t ng quát: RCOORứ ổ /
RCOOR/ + H2O RCOOH + R/OH
Ester N c Acid h u c Ancolướ ữ ơ
Đ i v i dung d ch loãng và l ng n c d nên ph n ng th y phân x y ra r t ch mố ớ ị ượ ướ ư ả ứ ủ ả ấ ậ
nh ng cũng hoàn toàn. N u th c hi n trong môi tr ng Hư ế ự ệ ườ + thì ph n ng x y ra r t nhanh.ả ứ ả ấ
Vì s n ph m có acid nên t xúc tác ph n ng và làm ph c t p thêm quá trình. Tuyả ẩ ự ả ứ ứ ạ
nhiên, n u n ng đ c a acid vô c xúc tác ban đ u cao thì s tăng n ng đ Hế ồ ộ ủ ơ ầ ự ồ ộ + do acid h u cữ ơ
t o ra không đáng k .ạ ể
Trong giai đo n đ u c a ph n ng, n ng đ c a CHạ ầ ủ ả ứ ồ ộ ủ 3COOH và C2H5OH hi n di n r tệ ệ ấ
ít nên ph n ng ngh ch không đáng k . Ph ng trình đ ng h c có d ng sau (ph n ng b c 1ả ứ ị ể ươ ộ ọ ạ ả ứ ậ
theo ester và b c 0 theo n c):ậ ướ

V i (a – x) là n ng đ c a ester acetat etyl t i th i đi m tớ ồ ộ ủ ạ ờ ể
a là n ng đ ban đ u c a ester acetat etylồ ộ ầ ủ
Thay vì theo dõi n ng đ c a ester acetat etyl trong ph n ng thì ng i ta theo dõiồ ộ ủ ả ứ ườ
l ng acid h u c CHượ ữ ơ 3COOH sinh ra t i t ng th i đi m cách nhau 10 phút.ạ ừ ờ ể
V i là th tích dung d ch NaOH dùng đ chu n đ 10 mL m u khi ph n ng k t thúcớ ể ị ể ẩ ộ ẫ ả ứ ế
là th tích dung d ch NaOH dùng đ chu n đ 10 mL m u t i th i đi m tể ị ể ẩ ộ ẫ ạ ờ ể
là th tích dung d ch NaOH dùng đ chu n đ 10 mL m u khi ph n ng b t đ uể ị ể ẩ ộ ẫ ả ứ ắ ầ
V đ ng bi u di n theo t có d ng đ ng th ng v i h s góc là và tung đ góc là .ẽ ườ ể ễ ạ ườ ẳ ớ ệ ố ộ
T đó, suy ra h ng s v n t c ph n ng kừ ằ ố ậ ố ả ứ 1 nhi t đ Tở ệ ộ 1.
III.THÍ NGHI MỆ(có th làm đ ng th i nhi t đ 30 ể ồ ờ ở ệ ộ oC và 40 oC):
1. Th c hi n thí nghi m 30 ự ệ ệ ở o
C :
B t máy đi u nhi t và ch n (set) nhi t đ 30 ậ ề ệ ọ ệ ộ oC.
L y pipet 5 mL hút 5 mL ester acetate ethyl cho vào bình đ ng m c 100 mL và dùngấ ị ứ
ng đong 100 mL l y 100 mL dung d ch HCl 0.2 N cho vào becher 250 mL r i đ t bình đ nhố ấ ị ồ ặ ị
m c và becher vào b đi u nhi t.ứ ể ề ệ
Đ kho ng 20 phút (cho dung d ch trong bình đ nh m c và c becher đ u có nhi tể ả ị ị ứ ả ề ệ
là 30 oC) l y becher ch a dung d ch HCl 0.2 N cho t t vào bình đ nh m c ch a ethyl acetateấ ứ ị ừ ừ ị ứ ứ
sao cho đ n v ch đ nh m c và l c đ u h n h p dung d ch. Ghi nh n nh n th i đi m b t đ uế ạ ị ứ ắ ề ỗ ợ ị ậ ậ ờ ể ắ ầ
đ vào – th i đi m b t đ u ester b th y phân là tổ ờ ể ắ ầ ị ủ o.
Sau đó 5 phút, dùng pipet 10 mL hút 10 mL dung d ch trong bình đ nh m c cho vàoị ị ứ
erlen ch a s n 50 mL n c c t đã ngâm l nh (đ m b o s th y phân c a ester ng ng l i).ứ ẵ ướ ấ ạ ả ả ự ủ ủ ừ ạ
Dung d ch trong erlen không màu. Ghi nh n th i đi m phút.ị ậ ờ ể
Ti n hành đ nh phân HCl b ng NaOH 0.1 N v i ch t ch th phenolphthalein đ nế ị ằ ớ ấ ỉ ị ế
khi dung d ch trong erlen chuy n sang ị ể màu h ng nh t ồ ạ b n trong 30 giây thì k t quá trìnhề ế
chu n đ . Ghi nh n giá tr th tích dung d ch NaOH 0.1 N đã dùng là Vẩ ộ ậ ị ể ị 1 ng v i th i đi m tứ ớ ờ ể 1.
C 10 phút l p l i s đ nh phân trên và ghi nh n giá tr th tích dung d ch NaOHứ ặ ạ ự ị ậ ị ể ị
0.1 N đã dùng là V2 →
6 ng v i các th i đi m tứ ớ ờ ể 2 →
6.
Ta có:
là th tích dung d ch NaOH 0.1 N c n đ nh phân HCl trong 10 mL h n h p th i đi m t,ể ị ầ ị ỗ ợ ở ờ ể
không đ i.ổ
• là th tích dung d ch NaOH 0.1 N c n đ nh phân CHể ị ầ ị 3COOH trong 10 mL m uẫ
h n h p th i đi m ph n ng hoàn toàn.ỗ ợ ở ờ ể ả ứ
•Suy ra:
B ng s li u c a quá trình đ nh phân HCl b ng dung d ch NaON 0.1 N:ả ố ệ ủ ị ằ ị
Vt (mL) V (mL) V – Vt (mL)
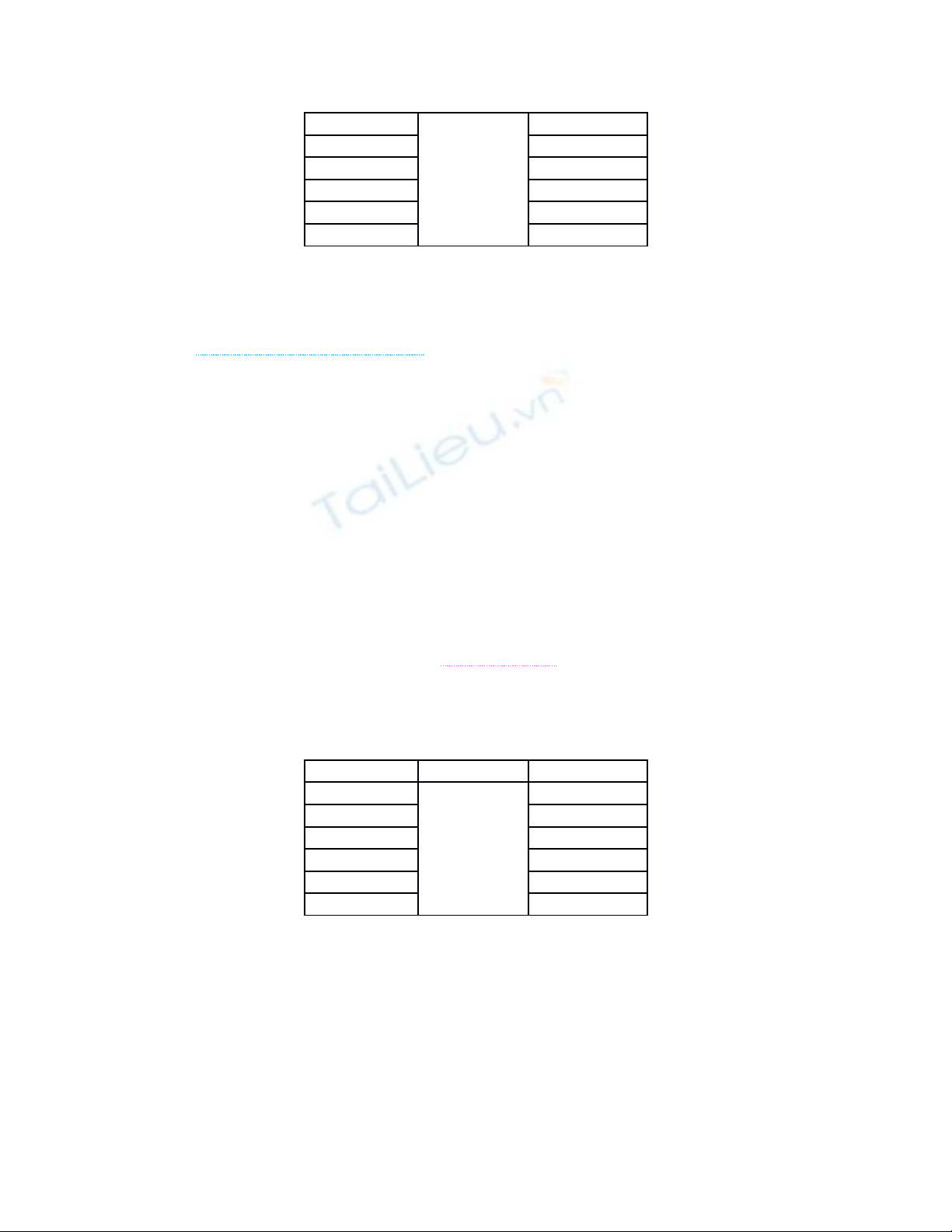
V1 = 17.9
69.966
52.066
V2 = 18.9 51.066
V3 = 19.4 50.566
V4 = 19.9 50.066
V5 = 21.2 48.766
V6 = 22 47.966
T b ng s li u, ta v đ c đ th bi u di n ừ ả ố ệ ẽ ượ ồ ị ể ễ ln(V
∝
– Vt) theo th i gian ờt (phút):
T đ th , ta ngo i suy tìm đ c: ừ ồ ị ạ ượ
2. Th c hi n thí nghi m 40 ự ệ ệ ở o
C :
Làm đ ng th i v i thí nghi m 30 ồ ờ ớ ệ ở oC:
B t máy đi u nhi t và ch n (set) nhi t đ 40 ậ ề ệ ọ ệ ộ oC.
L y pipet 5 mL hút 5 mL ester acetate ethyl cho vào bình đ ng m c 100 mL vàấ ị ứ
dùng ng đong 100 mL l y 100 mL dung d ch HCl 0.2 N cho vào becher 250 mL r i đ t bìnhố ấ ị ồ ặ
đ nh m c và becher vào b đi u nhi t.ị ứ ể ề ệ
Đ kho ng 25 phút (cho dung d ch trong bình đ nh m c và c becher đ u cóể ả ị ị ứ ả ề
nhi t là 40 ệoC) l y becher ch a dung d ch HCl 0.2 N cho t t vào bình đ nh m c ch a ethylấ ứ ị ừ ừ ị ứ ứ
acetate sao cho đ n v ch đ nh m c và l c đ u h n h p dung d ch. Ghi nh n nh n th i đi mế ạ ị ứ ắ ề ỗ ợ ị ậ ậ ờ ể
b t đ u đ vào – th i đi m b t đ u ester b th y phân là tắ ầ ổ ờ ể ắ ầ ị ủ o.
Sau đó 5 phút, dùng pipet 10 mL hút 10 mL dung d ch trong bình đ nh m c choị ị ứ
vào erlen ch a s n 50 mL n c c t đã ngâm l nh (đ m b o s th y phân c a ester ng ngứ ẵ ướ ấ ạ ả ả ự ủ ủ ừ
l i). Dung d ch trong erlen không màu. Ghi nh n th i đi m phút.ạ ị ậ ờ ể
Ti n hành đ nh phân HCl b ng NaOH 0.1 N v i ch t ch th phenolphthaleinế ị ằ ớ ấ ỉ ị
đ n khi dung d ch trong erlen chuy n sang ế ị ể màu h ng nh tồ ạ b n trong 30 giây thì k t quá trìnhề ế
chu n đ . Ghi nh n giá tr th tích dung d ch NaOH 0.1 N đã dùng là Vẩ ộ ậ ị ể ị 1 ng v i th i đi m tứ ớ ờ ể 1.
C 10 phút l p l i s đ nh phân trên và ghi nh n giá tr th tích dung d chứ ặ ạ ự ị ậ ị ể ị
NaOH 0.1 N đã dùng là V2 →
6 ng v i các th i đi m tứ ớ ờ ể 2 →
6.
B ng s li u c a quá trình đ nh phân HCl b ng dung d ch NaON 0.1 N:ả ố ệ ủ ị ằ ị
Vt (mL) V (mL) V – Vt (mL)
V1 =17.8
69.966
52.166
V2 =19.4 50.566
V3 =21.1 48.866
V4 =22.2 47.766
V5 =24.7 45.266
V6 =25.5 44.466
T b ng s li u, ta v đ c đ th bi u di n ừ ả ố ệ ẽ ượ ồ ị ể ễ ln(V
∝
– Vt) theo th i gian ờt (phút):

T đ th , ta ngo i suy tìm đ c: ừ ồ ị ạ ượ
T hai giá tr c a h ng s v n t c 30 ừ ị ủ ằ ố ậ ố ở oC và 40 oC, ta xác đ nh đ c năngị ượ
l ng ho t hóa Eượ ạ a theo công th c:ứ



![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)










![Phiếu bài tập cuối tuần Tiếng Việt 1 tuần 2 đề 2: [Hướng dẫn chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250728/thanhha01/135x160/42951755577464.jpg)

