Chương 5
Lý thuyết lượng tử của nguyên tử Hydro
PGS.TS. Lê Công Hảo
BT: 5.2, 5.3, 5.5, 5.6, 5.7, 5.11, 5.12, 5.13, 5.16, 5.17, 5.20,
5.21, 5.30, 5.31, 5.40
5.1 Phương trình Schrӧdinger
𝜕2𝜓
𝑑𝑥2+𝜕2𝜓
𝑑𝑦2+𝜕2𝜓
𝑑𝑧2+2𝑚
ℏ2𝐸 −𝑈 𝜓 = 0
Phương trình Schrödinger đối với electron
năng lượng Echuyển động trong nguyên tử
hydro theo không gian 3 chiều là
Thế tương tác Coulomb
r
e
U
0
2
4
−=
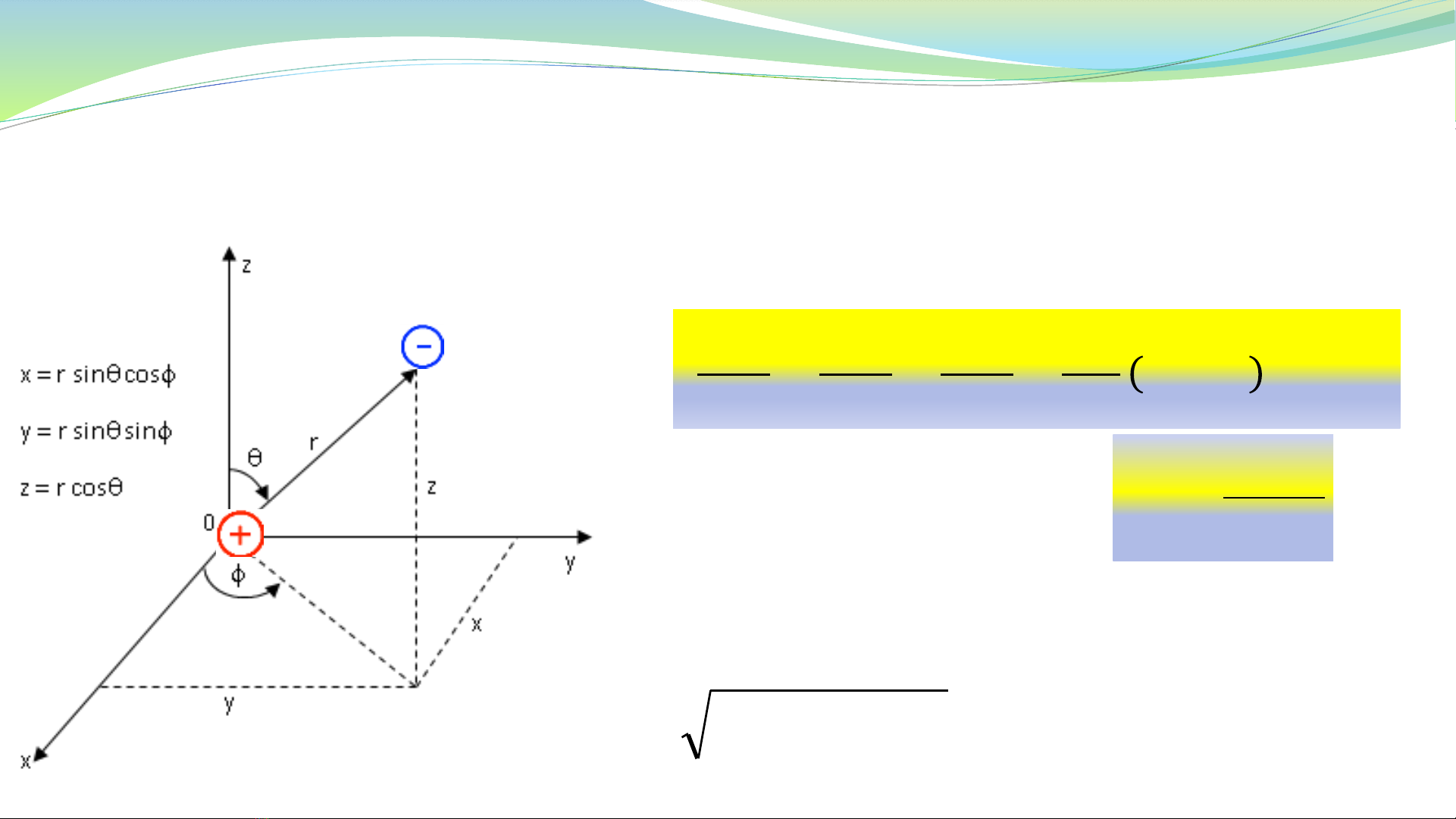
222 zyxr ++=
U tọa độ Decartes (x, y, z)
Tọa độ cầu (r,
,
)

5.1 Phương trình Schrӧdinger
( )
2
2
2 2 2 2 2 2
1 1 1 2m
r sin E U(r) 0
r r r r sin r sin
+ + + − =
được gọi là hàm sóng
)()()(),,(
= rRr
=
−
+
+
−ERR
r
e
r
r
rrme
1
4sin
1
sin
sin
1
20
2
2
2
2
2
2
2
Phương trình Schrödinger cho nguyên tử hydro
trong tọa độ cầu
= ..R
Viết gọn

5.2. Giải Phương trình Schrӧdinger bằng
Phương pháp tách biến
)()()r(R),,r( =
5.2.3. Phổ năng lượng
5.2.1. và 5.2.2. Sinh viên đọc thêm trong giáo trình
Trị riêng của năng lượng Ekết hợp với hàm sóng
mn
222
0
42
e
nn2)4(
eZm
E
−=
Nguyên tử hydro Z = 1
,....)3,2,1(
.1
32 2
1
2222
0
2
4
=
=−=
−=
n
n
E
n
hR
n
em
Ee
n
R= 3,27.1015 s-1 cũng được gọi là hằng số Rydberg
n được gọi là số lượng tử chính

5
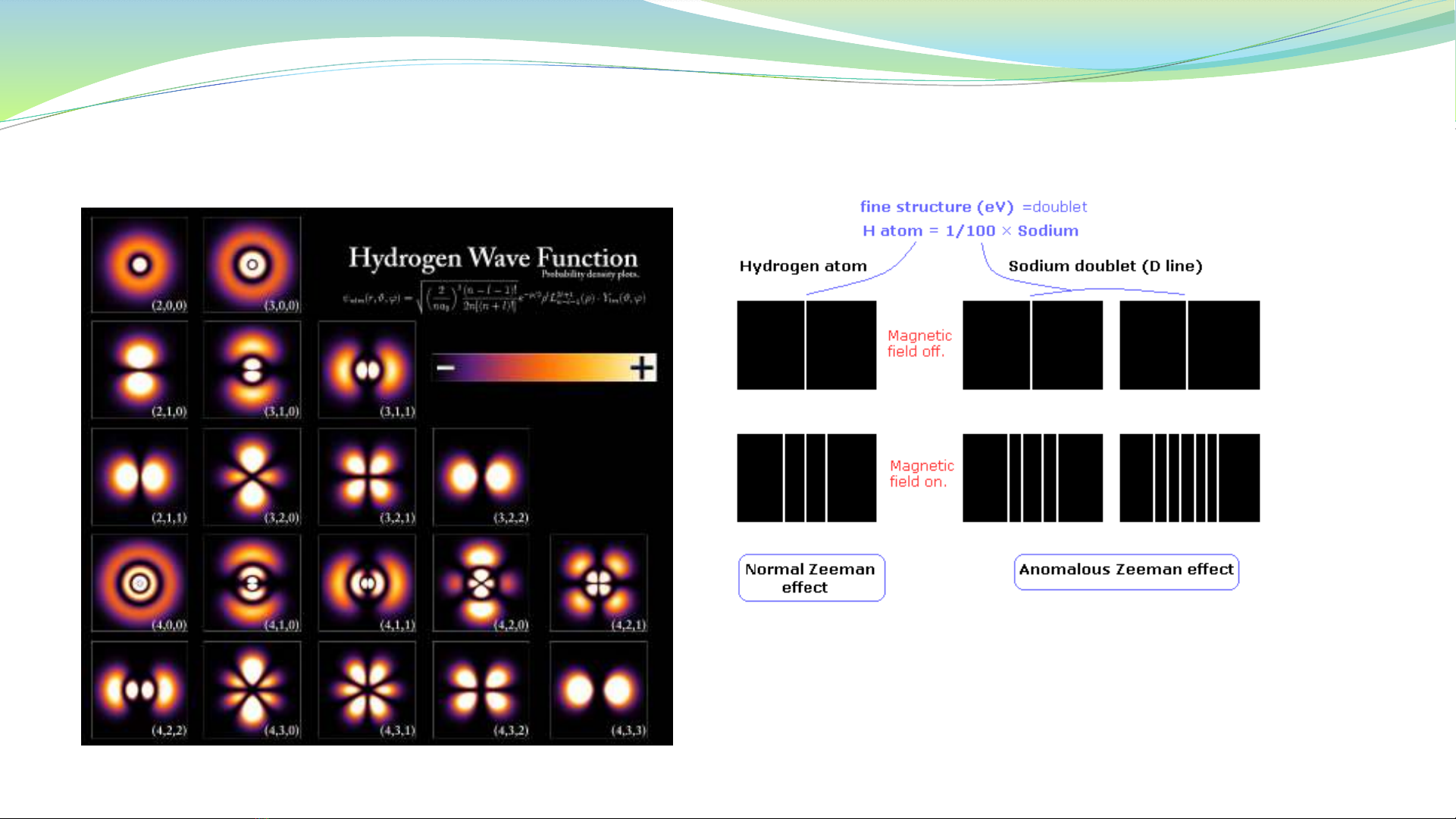
5.3 Hàm sóng toàn phần
),()()()()(
m
nm
m
nmn YrRrR ==
Số lượng tử chính n = 1, 2, 3, …, ,
Số lượng tử quỹ đạo ℓ= 0, 1, 2, …, (n - 1),
Số lượng tử từ: 𝑚ℓ= 0, 1, 2, …, ±ℓ,



















![Đề thi học kì 2 môn Vật lí 1 năm 2023-2024 có đáp án [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/64291778553454.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2023-2024 có đáp án [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/1381778553461.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2022-2023 có đáp án [kèm PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/21778553462.jpg)




