Bài giảng
VẬT LÝ HIỆN ĐẠI
HUỲNH TRÚC PHƯƠNG
Email: htphuong.oarai@gmail.com
CHƯƠNG 4B
LÝ THUYẾT LƯỢNG TỬ CỦA NGUYÊN TỬ HYDRO
4B.1. Phương trình Schrodinger
Nguyên tửHydro gồmcómộthạt nhân
mang điệntích+evàmột electron mang
điện tích −e chuyểnđộng quanh hạt nhân.
Hạt nhân đượccoilàđứng yên tạiO, còn
electron quay xung quanh.
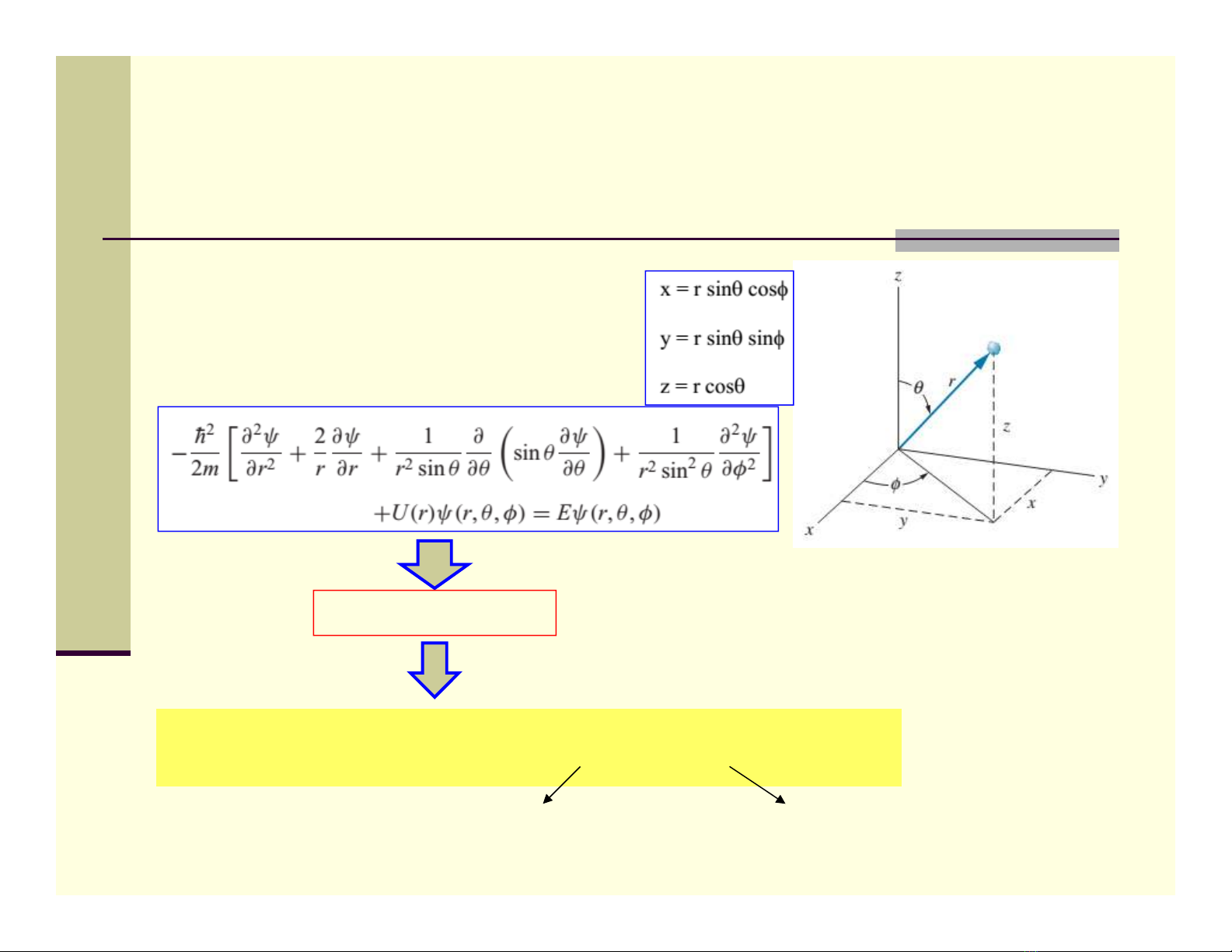
Trong tọa độ De-cát
Phương pháp để giải phương trình này là tách biến
Tuy nhiên, hàm thế năng
Không thể
tách biến
(4b.1)
(4b.2)
(4b.3)
11/29/2017
Thế năng tương tác:
r
e
k)r(U
2
−=
)z,y,x(E)z,y,x()z,y,x(U)z,y,x(
m2
2
ψ=ψ+ψΔ− h
)z(Z).y(Y).x(X)z,y,x( =ψ
222
0
2zyx4/e)z,y,x(U ++πε−=
4B.1. Phương trình Schrodinger
Trong tọa độ cầu:
Tách biến
(4b.4)
),(Y)r(R),,r( m,,nm,,n
φ
θ
=
φ
θ
Ψ=Ψ ll lll
Hàm xuyên tâm Hàm cầu
(4b.5)
CHƯƠNG 4B
LÝ THUYẾT LƯỢNG TỬ CỦA NGUYÊN TỬ HYDRO

4B.1. Phương trình Schrodinger
*Trạng thái lượng tửcủamộthạt chuyểnđộng trong trường thếU(r) đượcmô
tảbởi3sốlượng tửn,ℓvà mℓ.
11/29/2017
Trong đó: nđượcgọilàsốlượng tửchính,ℓlà sốlượng tửquỹđạovà mℓlà
sốlượng tửtừ.Cácsốlượng tửbịchi phốibởi qui luật sau:
n = 1, 2, 3,... ∞
ℓ=0,1,2,3,...n-1.
mℓ=0,±1, ±2, . . ±ℓ
|mℓ|≤ℓ.
oỨng với mỗi giá trị ncó ngiá trị có thể có của l.
oỨng với mỗi giá trị lcó (2l+ 1) giá trị khác nhau của ml.
CHƯƠNG 4B
LÝ THUYẾT LƯỢNG TỬ CỦA NGUYÊN TỬ HYDRO
4B.1. Phương trình Schrodinger
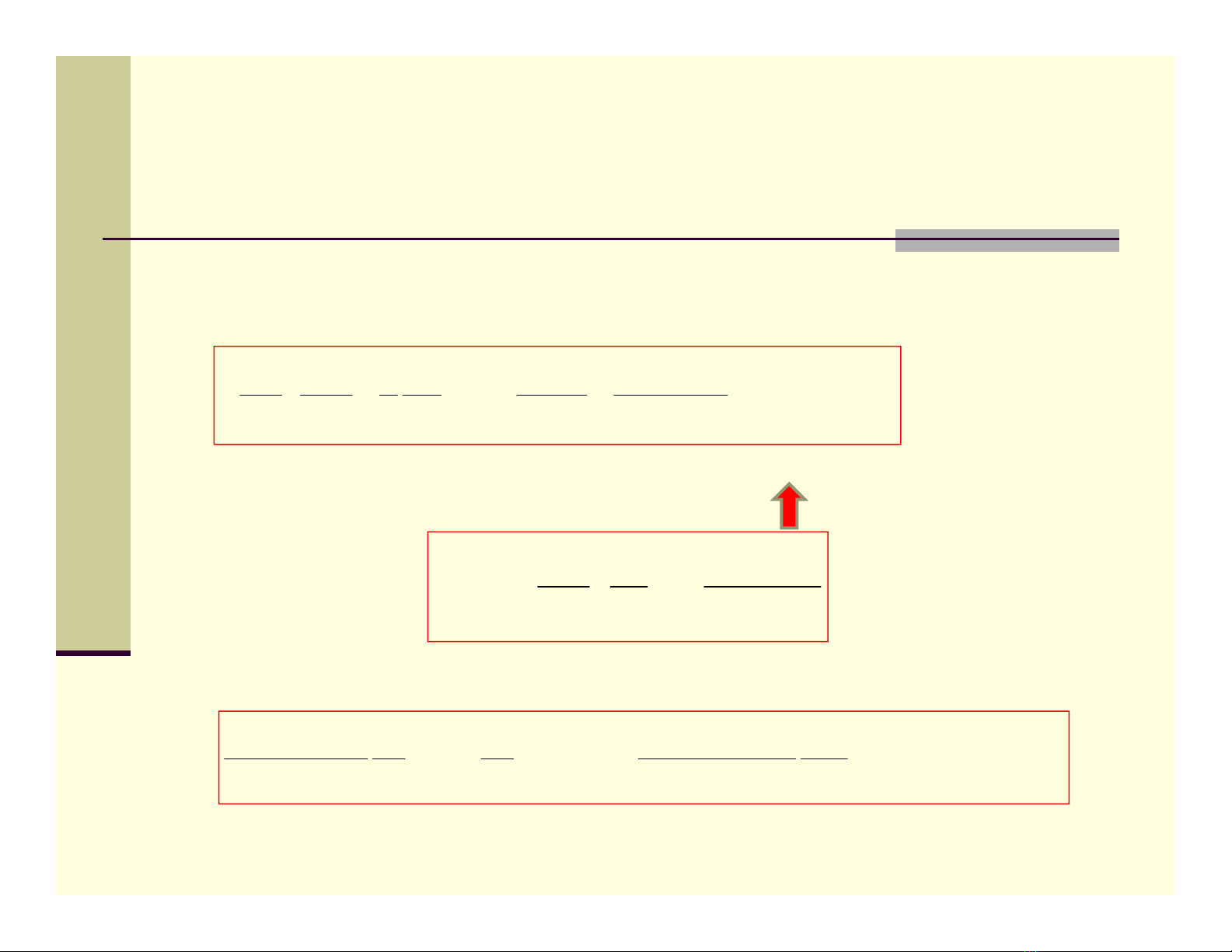
* Hàm bán kính (hàm xuyên tâm):
11/29/2017
* Giải phương trình Rnlta thu được năng lượng:
22
0
2
nn
)eV(6,13
n
1
a2
ke
E−=
⎟
⎟
⎠
⎞
⎜
⎜
⎝
⎛
−= (4b.6)
Năng lượng bị lượng
tử hóa
CHƯƠNG 4B
LÝ THUYẾT LƯỢNG TỬ CỦA NGUYÊN TỬ HYDRO
)r(ER)r(R
mr2
)1(
r4
e
dr
dR
r
2
dr
Rd
m2 2
2
0
2
2
22
=
⎟
⎟
⎠
⎞
⎜
⎜
⎝
⎛+
+
πε
−+
⎟
⎟
⎠
⎞
⎜
⎜
⎝
⎛+− hllh
* Hàm góc (hàm cầu):
)1(),(Y
sin),(Y
1
),(Ysin
sin),(Y
1
2
2
2+−=φθ
φ∂
∂
θφθ
+φθ
⎟
⎠
⎞
⎜
⎝
⎛
θ∂
∂
θ
θ∂
∂
θφθ ll



















![Đề thi học kì 2 môn Vật lí 1 năm 2023-2024 có đáp án [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/64291778553454.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2023-2024 có đáp án [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/1381778553461.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2022-2023 có đáp án [kèm PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/21778553462.jpg)




