ĐỀ CHÍNH THỨC
SỞ GDĐT TỈNH QUẢNG NAM
TRƯỜNG THPT ÂU CƠ
(Đề gồm có 3 trang)
KIỂM TRA GIỮA KỲ II NĂM HỌC 2024 - 2025
Môn: Hóa học – Lớp 12
Thời gian: 45 phút (không kể thời gian giao đề)
MÃ ĐỀ GỐC
Cho Mg=24; Ca=40; N=14; H=1; Cl=35,5; S=32; O=16; Br= 80; C=12.
A. TRẮC NGHIỆM (7,0 điểm).
Phần I. (3,0 điểm) Câu trắc nghiệm nhiều phương án lựa chọn. Học sinh trả lời từ câu 1 đến câu
12. Mỗi câu hỏi học sinh chỉ chọn 1 phương án.
Câu 1: Tính chất hoá học đặc trưng của kim loại là
A. tính oxi hoá. B. tính acid. C. tính base. D. tính khử.
Câu 2: Trong nhiều thiết bị có bộ phận tản nhiệt làm bằng nhôm.Vai trò tản nhiệt của nhôm được gây ra
bởi tính chất vật lí nào sau đây?
A. Tính dẫn nhiệt. B. Tính dẻo. C. Tính dẫn điện. D. Ánh kim.
Câu 3: Kim loại nào sau đây điều chế được bằng phương pháp nhiệt luyện với chất khử là CO?
A. Ca. B. Cu. C. K. D. Ba.
Câu 4: Với quá trình tách sodium bằng phương pháp điện phân sodium chloride nóng chảy, phát biểu nào
sau đây là đúng?
A. Tại anode xảy ra quá trình khử ion Na+.B. Tại cathode xảy ra quá trình khử ion Cl–.
C. Tại cathode xảy ra quá trình khử ion Na+.D. Tại anode xảy ra quá trình khử ion Cl–.
Câu 5: Hợp kim là vật liệu kim loại chứa một kim loại cơ bản với
A. một số kim loại khác hoặc phi kim. B. một số oxide của kim loại đó.
C. một số oxide kim loại khác hoặc phi kim. D. một số phi kim và oxide của phi kim đó.
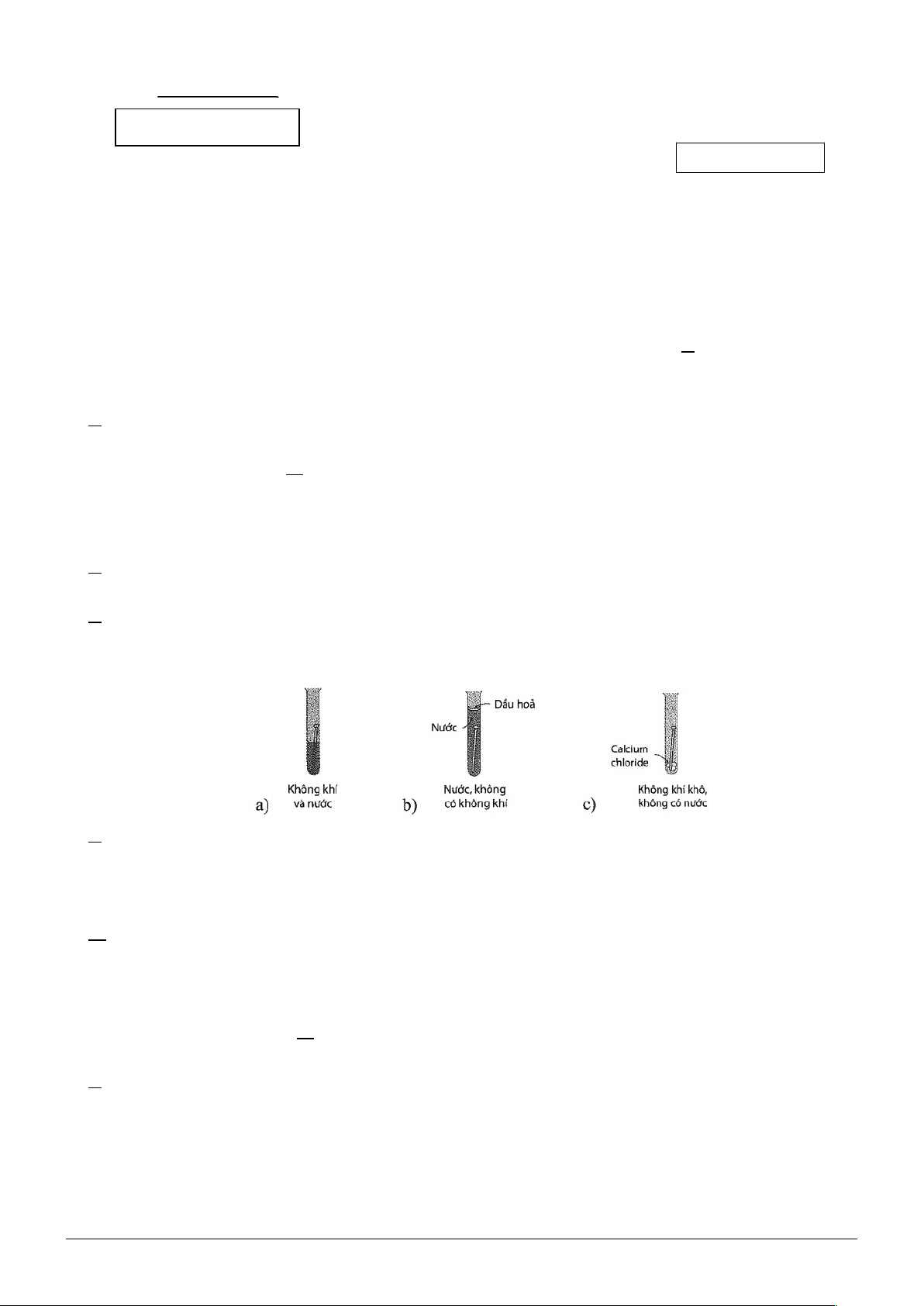
Câu 6: Ống nghiệm nào dưới đây, đinh sắt sẽ bị gỉ sau vài ngày?
A. chỉ có ống nghiệm (a). B. chỉ có ống nghiệm (b).
C. ống nghiệm (a) và (c). D. ống nghiệm (b) và (c).
Câu 7: Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường, tạo ra dung dịch có môi trường
kiềm là
A. Na, Li, K. B. Na, Fe, K. C. Be, Na, Ca. D. Na, Cr, K.
Câu 8: Nước muối sinh lí là dung dịch của chất X với nồng độ 0,9%, được dùng trong việc ngăn ngừa
nguy cơ mất muối do đổ quá nhiều mồ hôi, sau phẫu thuật, mất muối do tiêu chảy hay các nguyên nhân
khác. X là muối nào sau đây?
A. NaClO. B. NaCl. C. Na2SO4.D. NaNO3.
Câu 9: Ở điều kiện chuẩn, kim loại nào sau đây khử được ion H+ thành H2?
A. Mg. B. Cu. C. Hg. D. Au.
Câu 10: Bột nở baking powder có thành phần gồm baking soda kết hợp với tinh bột ngô và một số muối
vô cơ khác, có tác dụng làm cho bánh nở xốp, bông mềm. Phản ứng hoá học nào sau đây của bột nở xảy
ra làm cho bánh nở xốp?
A. NaHCO3 + Ca(OH)2 Na2CO3 + CaCO3 + H2O.
B. Na2CO3 + Ca(OH)2 NaHCO3 + CaCO3.
C. NaHCO3 + HCl NaCl + CO2 + H2O.
Trang 1/3 – Mã đề Gốc
D. NaHCO3 Na2CO3 + H2O + CO2.
Câu 11: Thực hiện các thí nghiệm sau:
(1) Cho khí CO đi qua ống đựng Fe2O3 nung nóng.
(2) Ngâm một đinh sắt nguyên chất vào dung dịch H2SO4 loãng có nhỏ thêm vài giọt dung dịch CuSO4.
(3) Nhỏ từng giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3.
(4) Đặt một thanh thép trong không khí ẩm.
(5) Ngâm một lá kẽm nguyên chất vào dung dịch CuSO4.
(6) Quấn hai sợi dây điện làm bằng nhôm và đồng rồi để trong không khí ẩm.
Số trường hợp xảy ra ăn mòn điện hoá là
A. 3. B. 4. C. 5. D. 6.
Câu 12: Cho các phản ứng xảy ra theo sơ đồ sau
X1 + H2O X2 + X3 + H2↑.
X2 + X4 → BaCO3 ↓ + K2CO3 + H2O.
Chất X2, X4 lần lượt là
A. KOH, Ba(HCO3)2. B. KHCO3, Ba(OH)2.
C. NaOH, Ba(HCO3)2. D. NaHCO3, Ba(OH)2.
Phần II. (2,0 điểm) Câu trắc nghiệm đúng sai. Học sinh trả lời từ câu 1 đến câu 2. Trong mỗi ý a),
b), c), d) ở mỗi câu, học sinh chọn đúng hoặc sai.
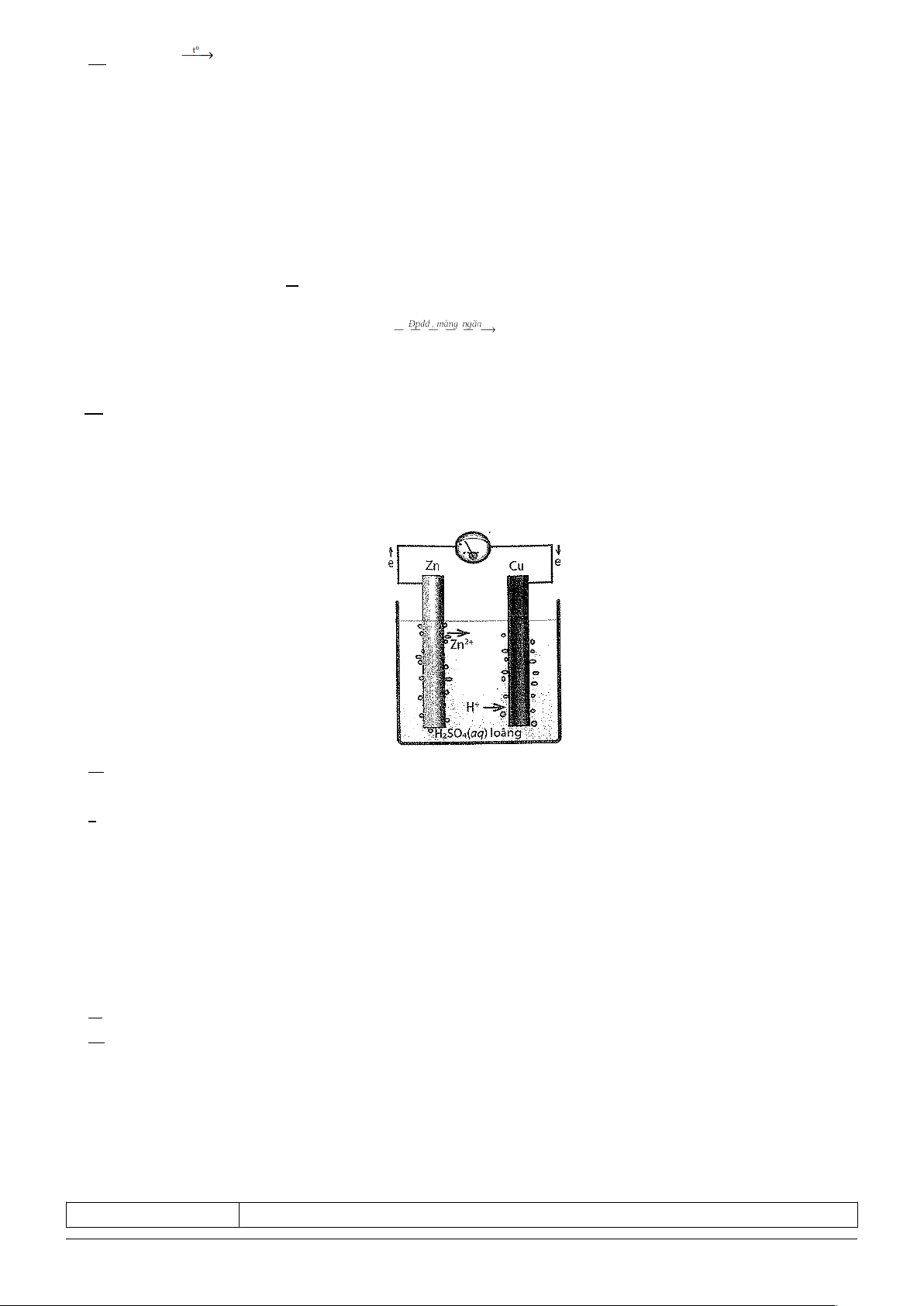
Câu 1: Tiến hành thí nghiệm về ăn mòn điện hoá như hình sau.
a) Điện cực Zn là anode, điện cực Cu là cathode.
b) Khí H2 chỉ thoát ra trên bề mặt thanh Cu, trên thanh Zn không có khí thoát ra.
c) Nồng độ cation Zn2+ trong dung dịch tăng dần.
d) Sau một thời gian màu xanh của dung dịch đậm dần.
Câu 2: Potassium là một trong số các nguyên tố quan trọng đối với cơ thể con người. Thiếu potassium,
cơ thể gây nguy cơ liệt cơ và rối loạn nhịp tim. Potassium cũng là nguyên tố cần thiết cho cây trồng, đặc
biệt là những cây ăn quả. Trong tự nhiên, potassium có ba loại đồng vị 39K (93,258%), 40K (0,012%), 41K
(6,730%).
a) Potassium là kim loại có tính khử mạnh, tan tốt trong nước dung dịch tạo thành có pH <7.
b) Tính khử của potassium yếu hơn sodium.
c) Nguyên tử khối trung bình của potassium là 39,134.
d) Chuối là một trong những loại hoa, quả giàu potassium . Khi thi đấu, nhiều vận động viên tennis
thường ăn chuối để bổ sung kịp thời lượng potassium cho cơ thể. Một quả chuối nặng 150 mg chứa
420 mg potassium. Khối lượng của đồng vị 40K và 41K lần lượt là 0,0517 mg và 29,716 mg.
Phần III. (2,0 điểm) Câu trắc nghiệm trả lời ngắn. Học sinh trả lời từ câu 1 đến câu 4.
Câu 1: Cho các tính chất vật lí ở cột (A) và giải thích ở cột (B) như sau:
Cột A Cột B
Trang 2/3 – Mã đề Gốc

(a) Tính dẻo (1) Dưới tác dụng của điện trường, các electron tự do trong tinh thể kim loại sẽ
chuyển động có hướng, tạo nên dòng điện.
(b) Tính dẫn điện (2) Các electron tự do phản xạ được những tia sáng nhìn thấy.
(c) Tính dẫn nhiệt (3) Do các electron tự do trong mạng tinh thể kim loại chuyển động, liên kết các
ion kim loại lại với nhau.
(d) Tính ánh kim (4) Các electron ở vùng có nhiệt độ cao truyền năng lượng cho ion dương và
electron khác trong toàn khối kim loại.
Hãy sắp xếp thứ tự giải thích của cột B với thứ tự tính chất vật lí ở cột A cho phù hợp.
Câu 2: Cho dãy các hợp chất của kim loại nhóm IA: Na2CO3, NaHCO3, KOH, K2SO4, K2CO3 và KHCO3.
Có bao nhiêu chất trong dãy trên thoả mãn cả hai tính chất sau:
- Tác dụng với dung dịch HCl tạo ra khí Y làm đục nước vôi trong.
- Đốt trên ngọn lửa đèn khí thấy ngọn lửa có màu tím.
Câu 3: Một chiếc cổng sắt khối lượng 1200 kg bị gỉ sét với tốc độ trung bình 800 gam mỗi ngày. Hỏi sau
bao nhiêu ngày thì chiếc cổng sắt đó sẽ bị gỉ hoàn toàn? (Làm tròn kết quả đến hàng đơn vị).
Câu 4: Phản ứng nhiệt nhôm tỏa rất nhiều nhiệt nên có thể làm nóng chảy kim loại sinh ra sau phản ứng.
Người ta dùng hỗn hợp gồm Al và Fe2O3 (hỗn hợp thermite) để hàn đường ray tàu hỏa, phản ứng sinh ra
sắt ở dạng nóng chảy nên lượng sắt này dùng để hàn gắn đường ray và Al2O3 sinh ra nổi lên trên bảo vệ
bề mặt trong lúc hàn, hạn chế sự oxi hóa sắt. Cho biết (Al2O3(s)) = - 1676 kJ/mol;
(Fe2O3(s)) = - 825,5 kJ/mol. Khi cho 42,8 gam hỗn hợp Al và Fe2O3 (có tỉ lệ số mol tương ứng
2:1) phản ứng hoàn toàn thì lượng nhiệt toả ra bằng bao nhiêu kJ? (làm tròn đến hàng đơn vị).
B. TỰ LUẬN (3,0 điểm).
Câu 1 (1,0 điểm): Thực hiện các thí nghiệm sau:
+ Thí nghiệm 1: Cho kim loại Na vào dung dịch CuSO4.
+ Thí nghiệm 2: Nhỏ từ từ dung dịch chloride acid vào backing soda.
Nêu hiện tượng và viết phương trình hóa học xảy ra của hai thí nghiệm trên.
Câu 2 (1,0 điểm): Phương pháp Solvay để sản xuất NaHCO3 và Na2CO3 sử dụng nguồn nguyên liệu dễ
tìm trong tự nhiên là muối ăn (NaCl), đá vôi (CaCO3) và ammonia (NH3). Quá trình cụ thể (không theo
thứ tự) như sau:
(1) Sản phẩm NH4Cl được chế hoá với vôi tôi, thu khí NH3:
2NH4Cl + Ca(OH)2 CaCl2 + 2NH3 + 2H2O
(2) Do NaHCO3 ít tan hơn các muối khác nên kết tinh trước. Tách NaHCO3 khỏi dung dịch, nung ở
nhiệt độ cao, thu được soda: 2NaHCO3 Na2CO3 + CO2 + H2O
(3) Hoà tan NaCl vào dung dịch NH3 đặc đến bão hoà.
(4) Nung CaCO3 rồi dẫn khí thoát ra vào dung dịch bão hoà của NaCl trong NH3:
CaCO3 CaO + CO2
NaCl + NH3 + CO2 + H2O NaHCO3 + NH4Cl
a. Sắp xếp theo thứ tự để đúng với quá trình Solvay (ví dụ: 1234, 4321,...).
b. Vì sao phương pháp Solvay được gọi là phương pháp tuần hoàn ammoniac.
Câu 3 (1,0 điểm): Quặng sắt là các khoáng vật chứa các hợp chất của sắt mà chủ yếu ở dạng các oxide.
Hematite là một loại quặng chứa hàm lượng sắt cao và được dùng để trực tiếp sản xuất gang bằng cách
nạp thẳng vào lò cao. Giả thiết 90% sắt trong quặng được chuyển vào gang. Từ 1000 tấn quặng hematite
(có hàm lượng 69,9% Fe) có thể sản xuất được bao nhiêu tấn gang loại 96% Fe?
------------- HẾT -------------
Học sinh không được sử dụng tài liệu. Cán bộ coi kiểm tra không giải thích gì thêm.
Họ và tên học sinhC:................................................................................SBD:...............................
Trang 3/3 – Mã đề Gốc

Đông Giang, ngày 14 tháng 3 năm 2025
DUYỆT
CỦA BAN GIÁM HIỆU
ALĂNG HẬU
GIÁO VIÊN
TRẦN THỊ NHƯ QUỲNH
Trang 4/3 – Mã đề Gốc


![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)




![Đề thi học kì 2 Vật lý lớp 11: Đề minh họa [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250709/linhnhil/135x160/711752026408.jpg)








