
TỔNG HỢP ĐỀ THI HK 2
MÔN HÓA HỌC 11
NĂM 2018 (CÓ ĐÁP ÁN)

1. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Lương Ngọc Quyến
2. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Đoàn Thượng
3. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Hương Khê
4. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Liễn Sơn
5. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Nguyễn Huệ
6. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Phan Ngọc Hiến
7. Đề kiểm tra HK 2 môn Hóa học 11 năm 2018 có đáp án
8. Đề thi HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Lý Thái Tổ
9. Đề thi HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường THPT
Yên Lạc 2
10. Đề thi KSCL HK 2 môn Hóa học 11 năm 2018 có đáp án – Trường
THPT Lý Thái Tổ

Trang 1/3 - Mã đề thi 001
SỞ GD & ĐT THÁI NGUYÊN
TRƯỜNG THPT
LƯƠNG NGỌC QUYẾN
ĐỀ KIỂM TRA HỌC KÌ II NĂM HỌC 2017- 2018
Môn: HOÁ HỌC- LỚP 11
Thời gian làm bài: 45 phút, không kể thời gian phát đề
H
ọ v
à tên h
ọc sinh:…………......……………SBD: …………....... Ph
òng:
………
Mã đề 001
Cho biết nguyên tử khối của các nguyên tố: H = 1; O = 16; C= 12; Mg = 24; Al = 27; S = 32; Cl = 35,5;
N = 14; Cl = 35,5; Fe = 56; Cu = 64; Zn = 65.
Chú ý: Học sinh GHI MÃ ĐỀ kẻ bảng sau vào giấy kiểm tra, chọn một đáp án đúng và trả lời phần trắc
nghiệm theo mẫu:
I/ TRẮC NGHIỆM KHÁCH QUAN (6 ĐIỂM, từ câu 1- 18)
Câu hỏi 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
Đáp án
Câu 1: Gần đây, rất nhiều trường hợp tử vong do uống phải rượu giả được pha chế từ cồn công nghiệp.
Một trong những hợp chất độc hại trong cồn công nghiệp chính là metanol (CH3OH). Tên gọi khác của
metanol là:
A. phenol. B. ancol etylic. C. etanol. D. ancol metylic.
Câu 2: Đun nóng hỗn hợp X gồm 2 ancol đơn chức no với H2SO4 đặc ở 1400 C. Sau khi phản ứng được
hỗn hợp 10,8 gam nước và 36 gam ba ete có số mol bằng nhau. Giả sử hiệu suất đạt 100%. Công thức 2
ancol nói trên là
A. C3H7OH và C4H9OH. B. C2H5OH và C3H7OH.
C. C2H5OH và C3H7OH. D. CH3OH và C2H5OH.
Câu 3: Khi cho phenol vào dung dịch NaOH thấy phenol tan. Sục CO2 vào dung dịch lại thấy phenol tách
ra. Điều đó chứng tỏ:
A. Phenol là axit mạnh B. Phenol là một ancol thơm.
C. Phenol là chất có tính bazơ mạnh D. Phenol là axit rất yếu, yếu hơn axit cacbonic
Câu 4: Cho hỗn hợp hai anken đi qua bình đựng nước brom thấy làm mất màu vừa đủ dung dịch chứa
8 gam brom. Tổng số mol hai anken là:
A. 0,05. B. 0,025. C. 0,1. D. 0,005.
Câu 5: Phản ứng đặc trưng của ankan là:
A. Phản ứng cháy. B. Phản ứng thế. C. Phản ứng tách. D. Phản ứng cộng.
Câu 6: Chất nào sau đây có khả năng làm mất màu brom:
A. propilen. B. butan. C. metylpropan. D. Cacbonđioxit.
Câu 7: Xét các loại phản ứng sau :(1) cộng (2) thế (3) cháy (4) trùng hợp . Loại phản ứng chỉ xảy ra
với etilen mà không xảy ra với metan là:
A. (1) và (2). B. (3) và (4). C. (1) và (4). D. (2) và (3).
Câu 8: Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni. Nung nóng bình một thời
gian, thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào lượng dư dung dịch AgNO3 trong
NH3 đến phản ứng hoàn toàn, thu được hỗn hợp khí Y và 24 gam kết tủa. Hỗn hợp khí Y phản ứng vừa
đủ với bao nhiêu mol Br2 trong dung dịch?
A. 0,20 mol. B. 0,15 mol C. 0,10 mol. D. 0,25 mol.
Câu 9: Một hỗn hợp X gồm hai anken hiđrat hóa (cộng nước, xúc tác thích hợp) cho hỗn hợp Y chỉ gồm
hai ancol.X gồm 2 anken nào sau đây ?
A. Propilen và but-2-en. B. Etilen và but -2-en.
C. Etilen và propilen. D. Etilen và but-1-en.
Câu 10: Trùng hợp etilen, sản phẩm thu được có cấu tạo là:
A. (-CH2=CH2-)n . B. (-CH=CH-)n. C. (-CH2-CH2-)n . D. (-CH3-CH3-)n.
Câu 11: Chất nào sau đây hòa tan được Cu(OH)2 ?
A. Phenol. B. Toluen C. Etanol. D. Etilen glicol.

Trang 2/3 - Mã đề thi 001
Câu 12: Cho các chất có công thức cấu tạo :
CH
2
OH
CH
3
OH
OH
(1) (2) (3)
Chất nào không thuộc loại phenol?
A. (1) . B. (3) C. (1) và (3). D. (2).
Câu 13: Có 5 chất: etan, axetilen, etilen, but - 1- in, but –2–in. Trong 5 chất đó, có mấy chất tác dụng
được với AgNO3/NH3 tạo thành kết tủa?
A. 5. B. 3. C. 2. D. 4.
Câu 14: Thuốc thử để phân biệt etanol và phenol là:
A. Dung dịch brom. B. Dung dịch KMnO4 C. Cu(OH)2. D. Quỳ tím
Câu 15: Đốt cháy một hỗn hợp gồm nhiều hiđrocacbon trong cùng một dãy đồng đẳng nếu ta thu được số
mol H2O > số mol CO2 thì công thức phân tử tương đương của dãy là:
A. CnH2n, n ≥ 2. B. CnH2n+2, n ≥1.
C. CnH2n-2, n≥ 2. D. CnH2n-2 , n ≥ 2 hoặc CnH2n, n ≥ 2.
Câu 16: Đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm CH4, C2H4, C4H10 thu được 0,14 mol CO2 và
0,23 mol H2O. Số mol của 2 ankan trong hỗn hợp là:
A. 0,01 B. 0,09 C. 0,05 D. 0,06
Câu 17: Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X (đktc) gồm 1 ankan X và 1 anken Y thu được 11,2 lít
khí CO2 (đktc) và 12,6 gam H2O. Công thức phân tử của X và Y lần lượt là:
A. C2H6 và C2H4. B. C2H6 và C3H6. C. CH4 và C2H4. D. CH4 và C3H6
Câu 18: Khi đun nóng ancol etylic với H2SO4 đặc ở 1700C thì sẽ tạo ra sản phẩm chính là:
A. CH3COOH. B. C2H4. C. C2H5OC2H5. D. CH3CHO.
II/ TỰ LUẬN (4 ĐIỂM)-----------
Câu 1: (2,0 điểm) Viết phương trình hóa học (ghi rõ điều kiện nếu có) theo sơ đồ sau:
CH4C2H2C2H4C2H5OH
PE (polietilen)
123
4
Câu 2: (2,0 điểm) Cho 15,2 gam hỗn hợp X gồm 2 ancol no, đơn chức, mạch hở kế tiếp nhau trong dãy
đồng đẳng tác dụng hết với Na dư thu được 3,36 lít khí H2 (đktc). Biết phản ứng xảy ra hoàn toàn.
a. Xác định công thức phân tử của 2 ancol và tính % khối lượng của mỗi ancol trong hỗn hợp ban đầu.
b. Đun nóng X với H2SO4 đặc ở 1400C. Tính khối lượng hỗn hợp ete tạo thành (Giả sử hiệu suất 100%).
----------- HẾT ----------
Học sinh không được dùng tài liệu. Cán bộ coi thi không giải thích gì thêm.
Trang 3/3 - Mã đề thi 001
ĐÁP ÁN – HƯỚNG DẪN CHẤM
Nội dung Điểm
Câu 1 2,0 điểm (0,5
4= 1,0 điểm)
CH4
0
t
C2H2 + 3H2 (1)
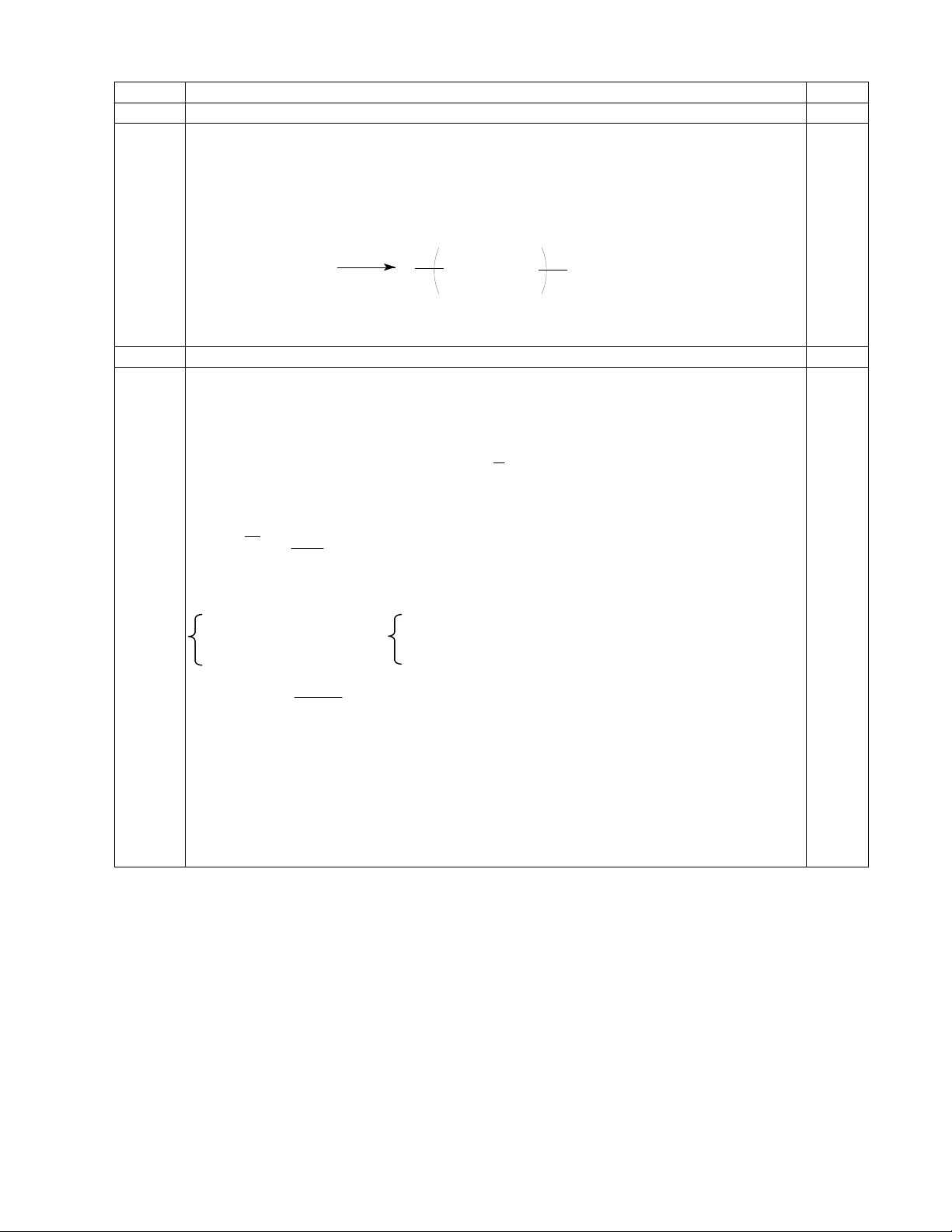
C2H2 + H2
0
3
Pd/PbCO ,t
C2H4 (2)
C2H4 + HOH +
H
C2H5OH (3)
n
CH2 - CH2
n CH2 = CH2
t0, p, xt
(4)
2,0
Câu 2 2,0 điểm
2
H
n 0,15 mol
Đặt công thức chung của 2 ancol là: CnH2n+ 1OH
CnH2n+ 1OH + Na
CnH2n+ 1ONa +
1
2
H2 (0,25 điểm)
0,3 mol 0,15 mol
Ta có: 15,2
M 51
0,3
(g/mol) Suy ra 2 ancol cần tìm là:
C2H5OH (M=46) <51< C3H7OH (M=60). (0,25 điểm)
Đặt số mol của C2H5OH, C3H7OH lần lượt là a và b.
a + b= 0,3 (I) a= 0,2
46 a+ 60b = 15,2 (II) b= 0,1 (0,25 điểm)
2 5 3 7
0,2.46
% m .100% 60,5%; % 39,5%.
15,2
C H OH C H OH
m (0,25 điểm)
Mặt khác :
2ROH 2 4
0
H SO
140 C
®Æc
ROR + H2O
0,3 mol 0,15 mol
Bảo toàn khối lượng : 2
ete H O
m m m
ancol
m ete = 15,2- 0,15. 18= 12,3 gam (0,5 điểm)
0,25
0,25
0,25
0,25
0,5


![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)




![Đề thi học kì 2 Vật lý lớp 11: Đề minh họa [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250709/linhnhil/135x160/711752026408.jpg)








