
CHƯƠNG 1:
HÓA HỌC TRONG KỸ THUẬT &
KHOA HỌC MÔI TRƯỜNG 1
(phần 3)
TS. Võ Nguyễn Xuân Quế

NỒNG ĐỘ CHẤT TAN TRONG NƯỚC
Nồng độ chất khí hòa tan
Ở trạng thái pha khí, nồng độ chất khí được biểu thị bằng áp suất (atm)
Nồng độ chất khí hòa tan trong nước được biểu thị bằng mg/L hoặc mmol/L.
Ngoài ra có mối liên hệ giữa nồng độ chất khí hòa tan trong nước và áp suất của
chất khí trong không khí ở trạng thái cân bằng thông qua định luật Henry:
Sw= KHPg
trong đó, Sw=nồng độ chất khí hòa tan trong nước ở trạng thái cân bằng (mg/L)
Pg=áp suất riêng phần của chất khí trên bề mặt dung dịch
KH=hằng số Henry (độ tan chất khí ở nhiệt độ xác định và áp suất
riêng phần 1 atm)

NỒNG ĐỘ CHẤT TAN TRONG NƯỚC
Nồng độ chất khí hòa tan
Trong khoa học về khí quyển, nồng độ chất khí được biểu thị
bằng tỷ lệ phối trộn (ppm hoặc ppb), thể hiện phần đóng góp của
khí vào tổng áp suất khí quyển.
Tỷ lệ phối trộn và đơn vị nồng độ khối lượng/thể tích (mg/m3
hoặc g/m3)có thể chuyển đổi qua lại nhờ vào định luật khí lý
tưởng (Boyle và Charles):
PV = nRT
trong đó, P = áp suất khí (atm);
V = thể tích khí (L);
T = nhiệt độ không khí (oK);
n = số mol khí (mol);
R = hằng số khí (0,082 L. atm.K-1. mol-1)

NỒNG ĐỘ CHẤT TAN TRONG NƯỚC
Nồng độ chất rắn trong nước
Nồng độ chất rắn trong nước tự nhiên (VD: chất rắn lơ lững;
bùn đáy) được biểu thị bằng đơn vị mg/g hoặc g/g
Đối với các pha rắn bao gồm một vài thành phần (VD: hỗn
hợp muối carbonate trong tự nhiên), nồng độ thành phần rắn
được biểu thị bằng phần mole
Ví dụ:đối với Ca0.95Mg0.05CO3(rắn) là tinh thể đá vôi có 5% Ca được
thay thế đồng hình bằng Mg, phần mole của MgCO3(rắn) trong đá
vôi là 0,05 và phần mole của CaCO3(rắn) là 0,95.
PHẢN ỨNG HÓA HỌC TRONG NƯỚC TỰ NHIÊN
Trong môi trường nước tự nhiên, có vô số các phản ứng hóa
học của các hợp chất vô cơ và hữu cơ, được phân thành một
vài nhóm phản ứng chính.
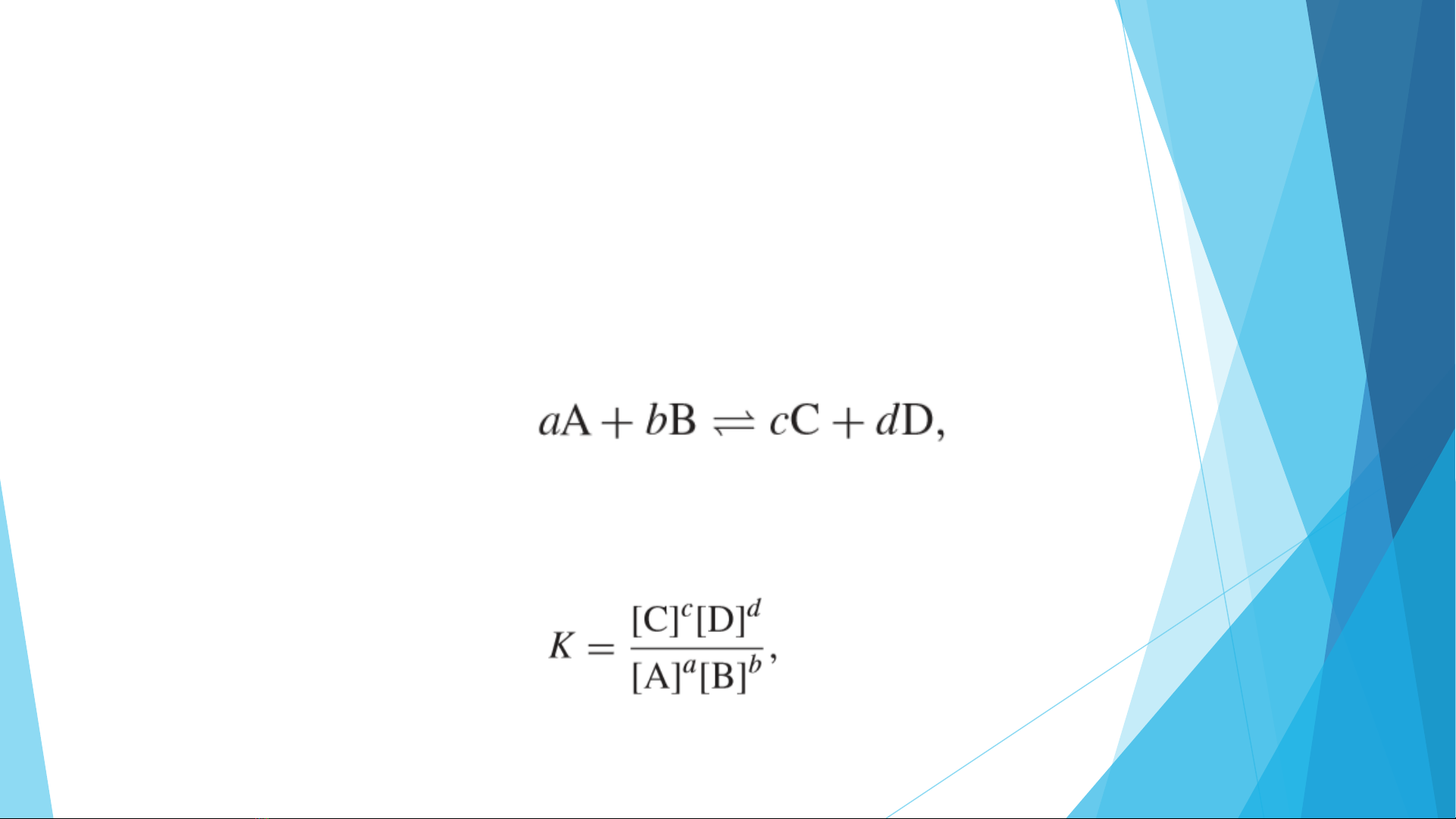
Phản ứng tổng quát:
Hằng số cân bằng của phản ứng là hằng số xác định tại điều
kiện áp suất và nhiệt độ xác định, biểu diễn trạng thái cân
bằng của phản ứng


![Bài giảng Hóa kỹ thuật môi trường 2 [năm]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250522/phongtrongkim2025/135x160/4021747906169.jpg)


![Bài giảng Hóa học xanh: Chương 0 - TS. Nguyễn Đăng Khoa [Full]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250508/antrongkim0609/135x160/1941952904.jpg)









![Ô nhiễm không khí từ nông nghiệp: Thách thức toàn cầu và định hướng hành động [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250917/kimphuong1001/135x160/52891758099584.jpg)










