
Trường Đại học Khoa học Tự nhiên
Khoa Hóa – Bộ môn Hóa Học Hữu cơ
HA HU CƠ 1
1
2
1. Liên kết cộng hóa trị phân cực
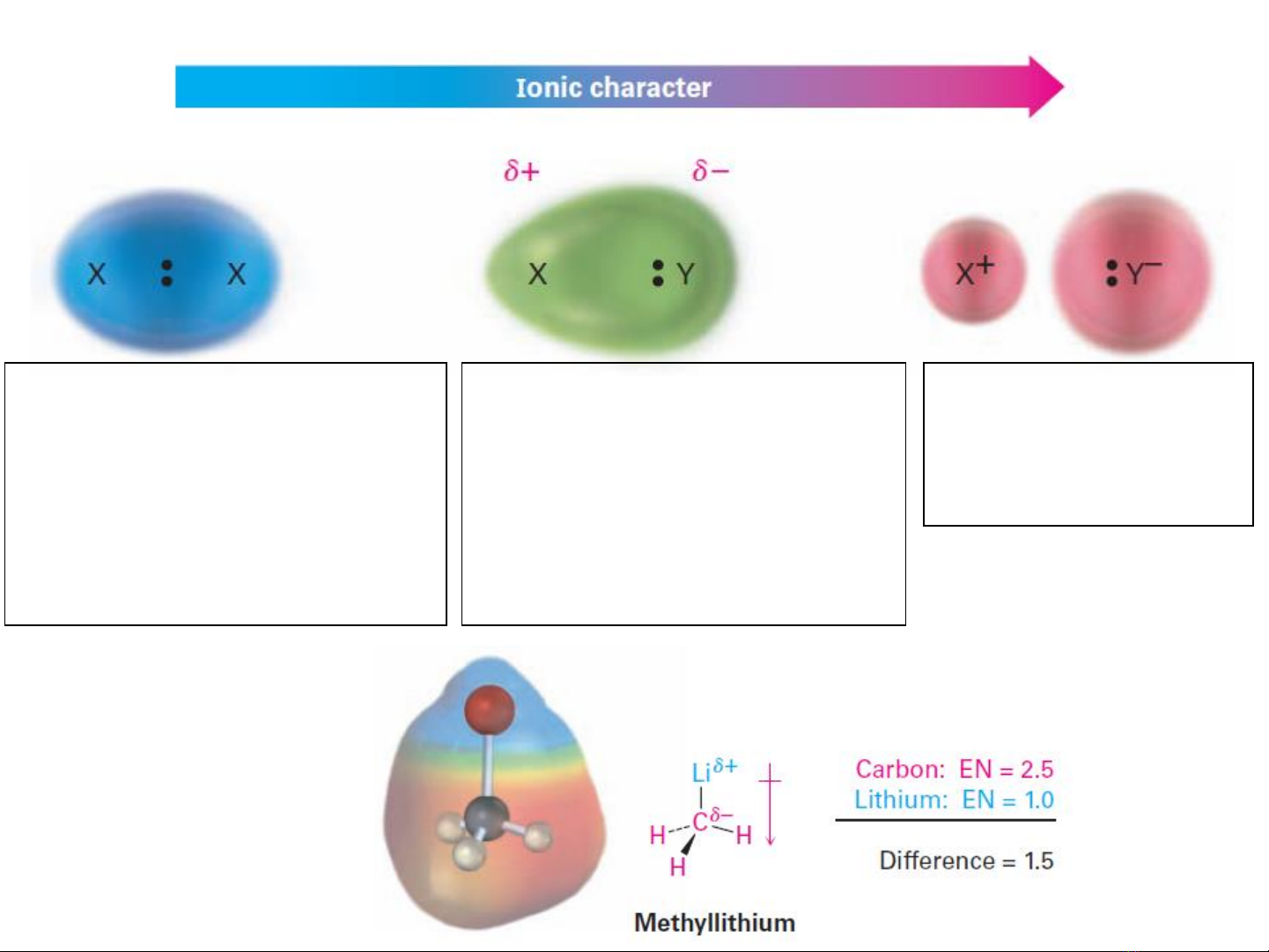
Độ âm điện của một số nguyên tố trong bảng phân loại tuần hoàn
Độ âm điện: Là tính chất của một nguyên tử có thể hút các điện tử về phía nó.
Các nguyên tố ở bên phải của BPLTH có độ âm điện mạnh hơn các nguyên tố
ở bên trái của bảng
Các liên kết hóa học: liên kết ion và liên kết cộng hóa trị.
Chương 2: Liên kết hóa trị phân cực – acid và base
3
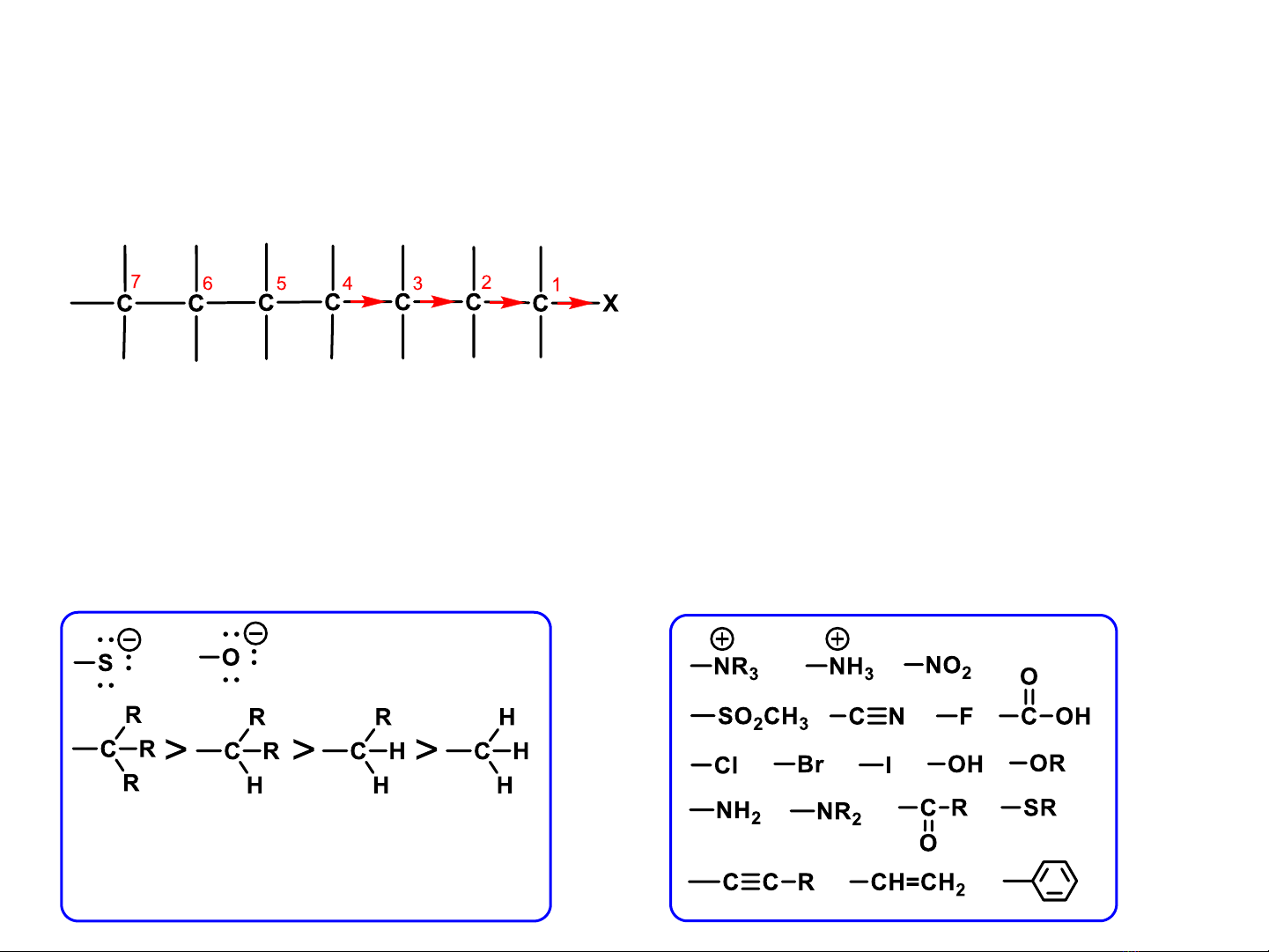
Tính ion (ionic character)
Nối ion
(ionic bond)
Chênh lệch ĐÂĐ > 2
Nối hoá trị không phân cực
(covalent bond)
Chênh lệch ĐÂĐ < 0.5
HH, ClCl, H3CCH3,
H2C=CH2, HCCH, NN, ...
Nối hoá trị phân cực
(polar covalent bond)
Chênh lệch ĐÂĐ từ 0.5 – 2.0
CH3 Cl, CH3 NH2,
CH3OH,CH3Li, …
4
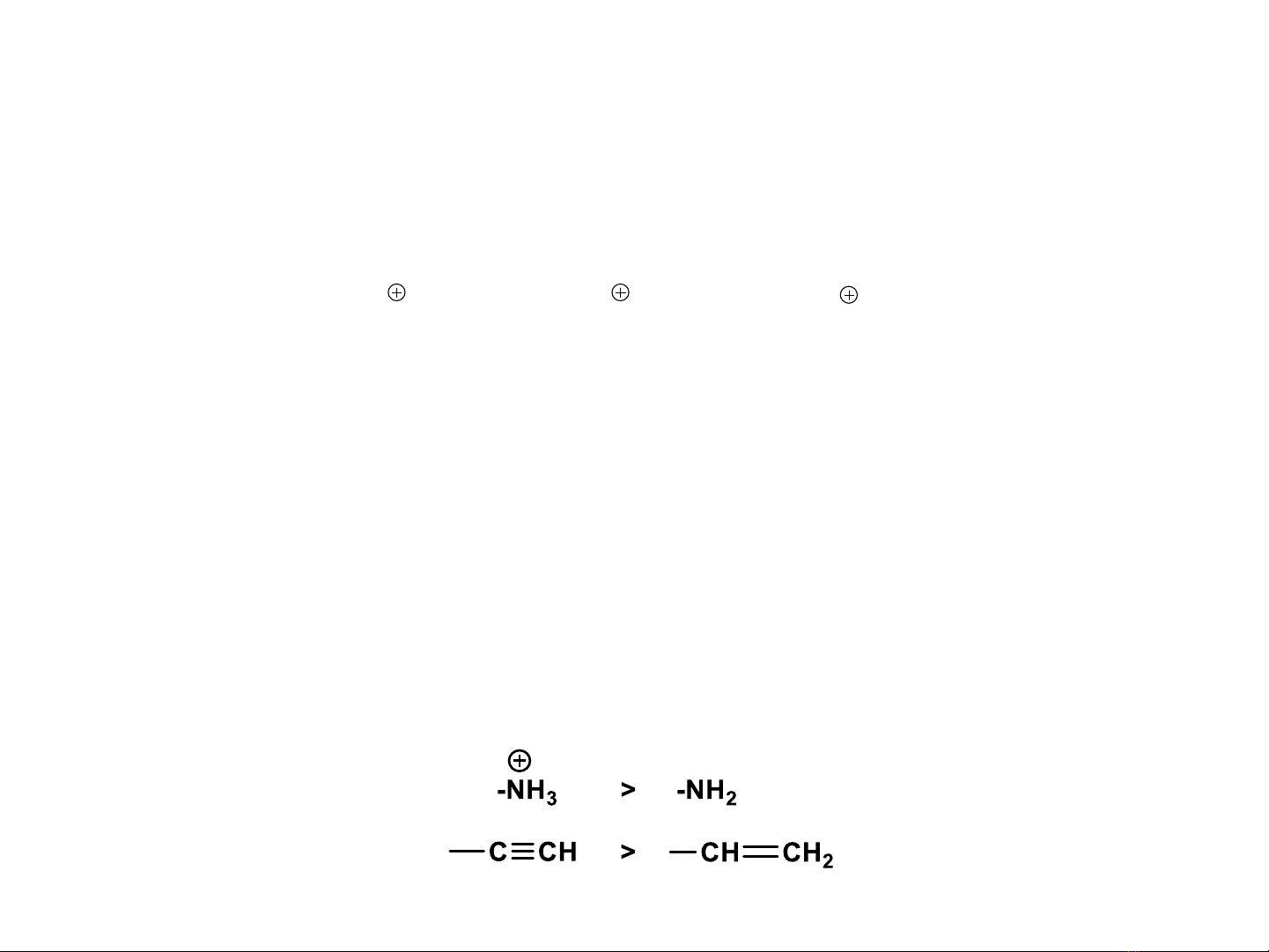
Hiệu ứng cảm I (inductive effect)
Hiệu ứng cảm: Là hiện tượng đôi điện tử nối không còn ở vị trí khoảng giữa
hai nhân, mà bị lệch về phía nguyên tử có ĐÂĐ lớn hơn.
Nhóm gây hiệu ứng cảm dương (+I):
khi lực đẩy gây ra bởi nguyên tử hay
nhóm nguyên tử có ĐÂĐ nhỏ hơn C.
I truyền dọc theo nối và yếu dần khi
càng xa nguyên tử có ĐÂĐ mạnh.
I sẽ tắt khi truyền qua 3 hay 4 nối .
Có thể truyền xa hơn nếu qua nối .
Nhóm gây hiệu ứng cảm âm (-I):
khi lực hút gây ra bởi nguyên tử hay
nhóm nguyên tử có ĐÂĐ lớn hơn C.
5
Khi lực hút được gây ra bởi nguyên tử hoặc một nhóm có ĐÂĐ mạnh hơn carbon
•Halogen có hiệu ứng – I giảm theo thứ tự ĐÂĐ: -F > -Cl > -Br > -I
• Nhóm mang điện tích dương có hiệu ứng – I rất mạnh:
-NR3-PR3-SR2
Amonium Phosphonium Sulfonium
Hiệu ứng cảm âm -I
• Nhóm trung hòa có hiệu ứng – I yếu: -NH2 -OH -OR -SH -C6H5 -CH=CH2
• Nhóm carbonil có hiệu ứng –I yếu: -CHO, -COOH, -COR
•Trong cùng chu kỳ, -I tăng dần từ phảI qua trái: -NR2 < -OR < -F
•Trong cùng phân nhóm, -I giảm dần từ trên xuống dưới
• Điện tích dương càng lớn hay tạp chủng càng có nhiều tính s, -I càng mạnh


























