
Báo Cáo Thực Hành Hóa Hữu Cơ GVHD: ThS Nguyễn Ánh Nga
Nhóm thực hiện: Nhóm1 Trang 1
BÁO CÁO THỰC HÀNH HOÁ HỮU CƠ

Báo Cáo Thực Hành Hóa Hữu Cơ GVHD: ThS Nguyễn Ánh Nga
Nhóm thực hiện: Nhóm1 Trang 2
BÀI 2: HYDROCACBON VÀ DẪN XUẤT HALOGEN
Nhóm Thực Hiện: Nhóm 1
Ngày Thực Hành: 17-9-2009
Điểm Lời phê
I. MỤC ĐÍCH THÍ NGHIỆM:
– Điều chế ankan ( Mêtan), xác định tính chất của hidrocacbon no.
– Điều chế và tính chất của anken.
– Điều chế và tính chất của ankin.
– Tính chất của benzen và toluen.
– Tính chất của dẫn xuất halogen.
II. THỰC HÀNH:
Phần A: Hydrocacbon
Thí nghiệm 1: Điều chế và đốt cháy metan
+ Điều chế:
Mêtan được điều chế bằng cách đun hỗn hợp vôi tôi xút (tỉ lệ khối lượng tương ứng là
1.5:1) với CH3COONa đã được làm khan bằng cách đun nóng. Thu khí mêtan sinh ra
bằng cách đẩy nước.
Phương trình phản ứng:
CH3COONa NaOH CH4 Na2CO3
CaO, NaOH
to
Ta dùng vôi tôi trộn với xút là để ngăn không cho NaOH làm thủng ống nghiệm bằng
thủy tinh (SiO2) dẫn đến nguy hiểm theo phản ứng sau:
SiO2 + 2NaOH → Na2SiO3 + H2O
Đồng thời muối CH3COONa thường không khan phản ứng với NaOH là chất hút ẩm
mạnh sẽ gây cản trở do đó trước khi tiến hành phải được làm khan để loại nước.
Thu khí mêtan qua nước để làm giảm bớt tạp chất khí do khi qua nước bị nước hấp
thụ→ thu khí mêtan tinh khiết hơn.
+ Tính chất:
4

Báo Cáo Thực Hành Hóa Hữu Cơ GVHD: ThS Nguyễn Ánh Nga
Nhóm thực hiện: Nhóm1 Trang 3
Ta tiếp tục thử tính chất của khí mêtan bằng cách cho que đóm đến đầu óng dẫn khí thì
thấy que đóm cháy với ngọn lửa màu xanh→ khí metan duy trì sự cháy.
Đưa nắp chén sứ chạm vào ngọn lửa của metan đang cháy thì có hơi đọng lại trên chén
và có hơi đen do phản ứng oxi hóa xảy ra, kèm theo các quá tình phụ sinh muội than ,
mặt khác lượng CH4 ít dẫn đến lượng sản phẩm cũng ít.
Thí nghiệm 2: Phản ứng brôm hóa hydocacbon no
- Cho vài giọt brôm trong cacbontetraclorua vào ống nghiệm đã chứa n-hexan hoặc ete
dầu hỏa. Ta thấy, dung dịch brom ban đầu màu vàng, lắc nhẹ hỗn hợp phản ứng để
một thời gian thấy dung dịch bị mất màu.
Do tốc độ phản ứng thế Brom vào anken thường chậm nên dùng dung dịch CCl4 làm
dung môi vì nó có khả năng hòa tan tốt cả brom và ankan làm cho phản ứng xảy ra
nhanh và biến đổi màu rõ hơn.
- Phản ứng thế Brom hóa hidrocacbon no xảy ra theo cơ chế gốc tự do (SR), bao gồm
các giai đoạn: (R – góc ankyl)
o Khơi màu phản ứng:
Br Br as Br Br
o Phát triển mạch:
R
Br
R H HBr
R Br
Br2
RBr
o Ngắt mạch:
Br Br
R
Br Br
RR R
RBr R Br
Trong các giai đoạn trên, giai đoạn chậm quyết định tốc độ phản ứng chung là giai
đoạn hình thành góc tự do ankyl, giai đoạn này đòi hỏi năng lượng hoạt hóa cao hơn
nên mang tính chất quyết định chung cho vận tốc cả phản ứng, nên nhìn chung phản
ứng khó xảy ra hơn.
- Khi dùng n-hexan ta thường thu được hỗn hợp sản phẩm là đồng phân của nhau:
Khi dùng n-haxan ta thu được:

Báo Cáo Thực Hành Hóa Hữu Cơ GVHD: ThS Nguyễn Ánh Nga
Nhóm thực hiện: Nhóm1 Trang 4
Br2
nC6H14 CCl4
H3C CH2CH2CH2
H
C CH3
Br
H3C CH2CH2CH2
H2
CCH2Cl
6%
47%
H3C CH2CH2
H
C
H2
CCH3
47% Br
HBr
Thí nghiệm 3: Điều chế và tính chất của etilen
+ Điều chế:
Đun ống nghiệm chứa hỗn hợp C2H5OH và H2SO4 trên ngọn lửa đèn cồn, tiến hành
thu khí C2H4 sinh ra.Sau một thời gian, hỗn hợp có màu vàng nâu và sinh khí C2H4
không màu theo phương trình:
H CH2CH2OH H2SO4 98%
170-180oCH2C CH2H2O
Trước khi đun, ta thêm vào hỗn hợp vài hạt cát hoặc viên sứ xốp để làm hỗn hợp sôi
đều. Ngoài ra ta có thể lắp thêm ống đựng vôi tôi xút để hấp thụ nước, SO2, các sản
phẩm phụ khác của phản ứng trên ..để thu được etylen tinh khiết.
+ Tính chất:
- Tiếp tục quá trình, đốt khí etylen ở đầu ống dẫn khí thì ta thấy ngọn lửa cháy có màu
xanh hơi vàng ở trên và có ít khói thoát ra. Đưa nắp chén sứ vào ngọn lửa đang cháy
thấy có muội than bám trên nắp chén sứ. vi phản ứng oxy hóa xảy ra sinh ra CO2, H2O
kèm theo muội than là sản phẩm phụ,lửa màu vàng thường cho thấy có muội than
C2H4 + 3O2 o
t C
2CO2 + 2H2O.
- Dẫn khí etylen vào ống nghiệm chứa nước brôm bão hòa, quan sát ta thấy dung dịch
từ màu vàng hơi cam (màu của dung dịch brôm) chuyển sang nhạt dần nếu cứ cho tiếp
sục tiếp khí etylen vào thì dung dịch mất màu. Hiện tượng trên là do phản ứng xảy ra
theo cơ chế cộng hợp ái điện tử thông thường bẻ gảy liên kết
giữa etylen và brôm
tạo sản phẩm không màu theo phương trình:
Br2
H2C CH2BrH2C CH2Br
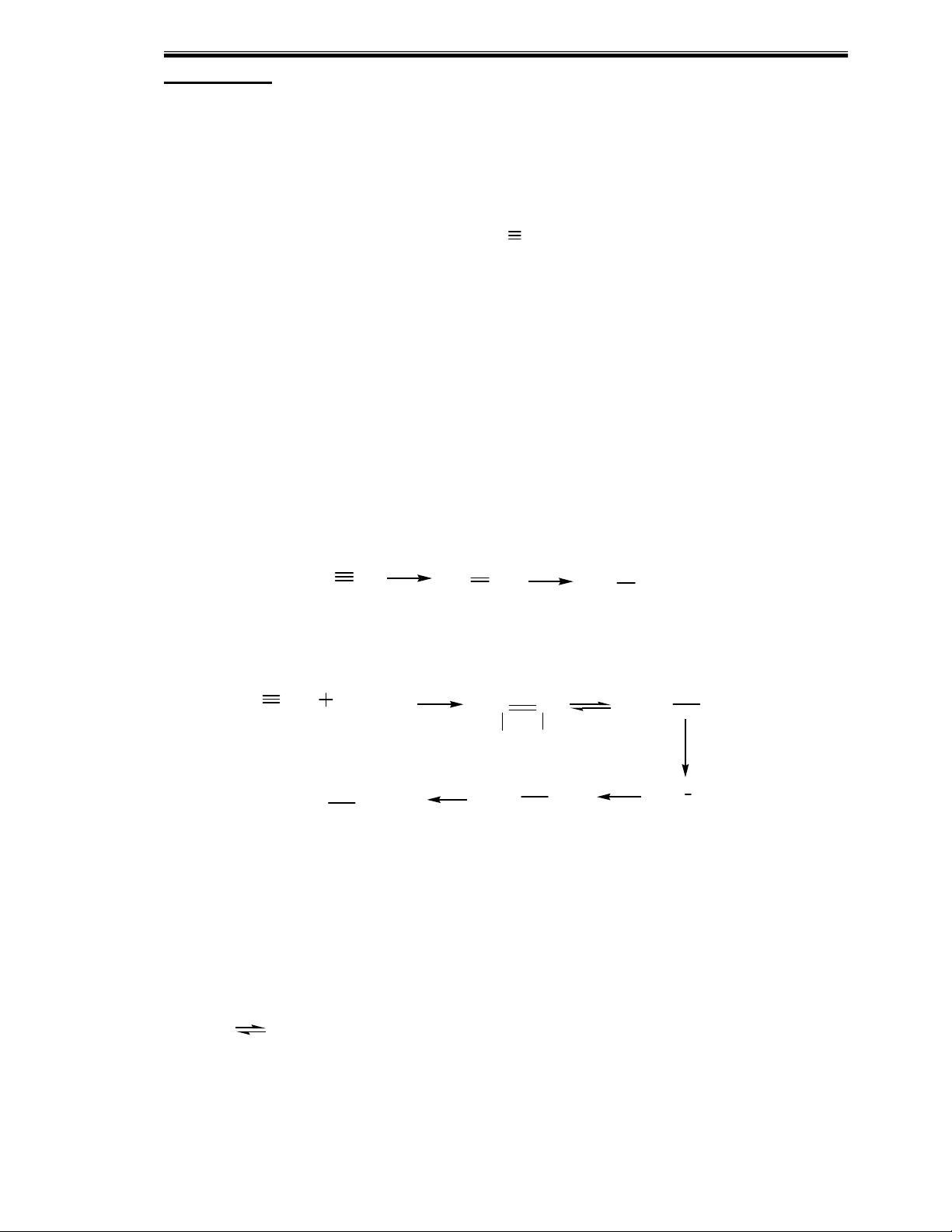
- Dẫn etilen vào ống nghiệm chứa KMnO4 thì dung dịch từ màu tím dần nhạt màu và
xuất hiện kết tủa đen.Do nối đôi etilen bị KMnO4 oxi hóa thành 1,2 diol đồng thời tạo
MnO2 dạng kết tủa đen theo phương trình:
H2C = CH2 + KMnO4 +H2O→ HOCH2-CH2OH + KOH + MnO2↓
Báo Cáo Thực Hành Hóa Hữu Cơ GVHD: ThS Nguyễn Ánh Nga
Nhóm thực hiện: Nhóm1 Trang 5
Thí nghiệm 4: Điều chế và tính chất của axetylen
+ Điều chế:
Cho nước vào ống nghiệm đã chứa sẵn canxi cacbua và đậy thật nhanh bằng nút cao su
có ống dẫn khí thì thấy trong ống ngiệm sủi bọt, đầu ống dẫn khí có khí không màu, có
mùi hôi thoát ra, đó là khí axetylen
CaC2 + H2O → HC CH + Ca(OH)2
Thực tế axetilen không có mùi, nhưng sản phẩm thu được có mùi là do trong sản phẩm
có lẫn nhiều tạp chất như H2S, NH3, PH3 … và các hợp chất gây mùi.
+ Tính chất:
a. Đốt cháy khí ở đầu ống dẫn thì ngọn lửa có màu sáng chói, muội than bám vào ống
nghiệm và muội than bay ra nhiều hơn so với trường hợp metan và etylen. Đưa nắp
chén sứ vào ngọn lửa đang cháy, thì ở nắp chén có vệt đen là muội than sinh ra từ phản
ứng oxy hóa axetylen.
b. Dẫn khí axetylen vào dung dịch nước brôm bão hòa thì nước brôm cũng bị mất màu,
nhưng tốc độ mất màu chậm hơn so với etylen. Phản ứng cộng diễn ra qua 2 giai đoạn:
HC CH Br2BrHC CHBr Br2Br2HC CHBr2
c. Khi dẫn khí vào dung dịch KMnO4 thì màu dung dịch từ tím chuyển sang nhạt dần,
có tủa nâu đen của MnO2.
H2O
KMnO4
HC CH HC CH
OH OH
OHC CH2OH
OHC CHO
HOOC CHO
COOHHOOC
d. Phản ứng với phức amiacat bạc và amiacat đồng:
Phản ứng với amiacat bạc:
Amiacat bạc được điều chế theo phương trình sau:
Cho dung dịch AgNO3 vào ống nghiệm, nhỏ vào đó dung dịch NH3 đến khi nào kết tủa
Ag2O vừa sinh ra tan hoàn toàn.
AgNO3 + NH3 + H2O → AgOH + NH4NO3
2AgOH Ag2O + H2O
Ag2O + 2NH3 + H2O → 2(Ag(NH3)2)OH


























