
Trang 1/3 – MÃ ĐỀ 02
Trường THPT PHAN ĐĂNG LƯU KIỂM TRA HỌC KÌ II (2010-2011)
TỔ HÓA MÔN HÓA KHỐI 12
Thời gian làm bài : 45 phút
Đề kiểm tra gồm có 3 trang. Ngày kiểm tra: 03/4/2011
MÃ ĐỀ 02
C©u 1 :
Cho các phản ứng :
1- M + 2HCl → MCl2 + H2.
2. MCl2 + 2NaOH → M(OH)2 + 2NaCl.
3. 4M(OH)2 + O2 + H2O → 4M(OH)3.
4. M(OH)2 + NaOH → Na[M(OH)4] hay NaMO2 + 2H2O
M là kim loại nào sau đây ?
A.
Fe. B.
Al. C.
Pb. D.
Cr.
C©u 2 :
Cho dung dịch NH3 đến dư vào dung dịch hỗn hợp AlCl3, ZnCl2 thu được kết tủa A. Nung A
đến khối lượng không đổi thu được chất rắn B. Cho H2 (dư) qua B nung nóng thu được chất
rắn ...
A.
Al2O3. B.
ZnO và Al. C.
ZnO và Al2O3. D.
Zn và Al2O3.
C©u 3 :
Phát biểu nào sau đây là phù hợp với tính chất hóa học chung của kim loại ?
A.
Kim loại có tính khử, nó bị oxi hóa thành ion dương.
B.
Kim loại có tính oxi hóa, nó bị oxi hóa thành ion dương
C.
Kim loại có tính khử, nó bị khử thành ion âm
D.
Kim loại có tính oxi hóa, nó bị khử thành ion âm
C©u 4 :
Nung nóng 16,8g bột sắt và 6,4g bột lưu huỳnh ( không có không khí) thu được sản phẩm X.
Cho X tác dụng với dung dịch HCl dư thì có V lít khí thoát ra ( đktc). Các phản ứng xảy ra
hoàn toàn. Giá trị của V là:
A.
6,72 lít B.
2,24 lít C.
4,48 lít. D.
3,36 lít.
C©u 5 :
Cần phải thêm bao nhiêu ml dung dịch NaOH 0,25M vào 50ml dung dịch hỗn hợp HCl 0,1M
và H2SO4 0,05M để thu được dung dịch có pH = 2,0 ?
A.
43,75ml. B.
40,75ml. C.
27,75ml. D.
36,54ml.
C©u 6 :
Cho 4,48 lít CO2 đkc vào 40 lít dung dịch Ca(OH)2 ta thu được 12 g kết tủa . Vậy nồng độ
Mol/lít của dung dịch Ca(OH)2 là :
A.
0,004 B.
0,006 C.
0,008 D.
0,002
C©u 7 :
Khi hoà tan một vật bằng nhôm vào dung dịch NaOH, phản ứng đầu tiên xảy ra sẽ là :
A.
2Al + 6H2O
2Al(OH)3 + 3H2
B.
2Al + 2NaOH + 2H2O
2NaAlO2 + 3H2
C.
Al2O3 + 2NaOH
2NaAlO2 + H2O
Hay Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
D.
Al(OH)3 + NaOH
NaAlO2 + 2H2O
C©u 8 :
10,2 gam Al2O3 tác dụng vừa đủ với bao nhiêu ml dung dịch NaOH 0,8M.
A.
300 ml B.
700 ml C.
600 ml D.
250 ml
C©u 9 :
Khi cắt miếng Na kim loại,bề mặt vừa cắt có ánh kim lập tức mờ đi,đó là do có sự hình thành
các sản phẩm rắn nào sau đây?
A.
Na2O , NaOH , Na2CO3 B.
Na2O, NaOH , Na2CO3 , NaHCO3.
C.
Na2O , Na2CO3 , NaHCO3 D.
NaOH , Na2CO3 , NaHCO3.
C©u 10 :
Cho Ca vào dung dịch Na2CO3.
A.
Ca khử Na+ thành Na, Na tác dụng với nước tạo H2 bay hơi, dung dịch xuất hiện kết tủa trắng.
B.
Ca khử Na+ thành Na, dung dịch xuất hiện kết tủa trắng CaCO3
C.
Ca tác dụng với nước, đồng thời dung dịch đục do Ca(OH)2 ít tan
D.
Ca tan trong nước sủi bọt khí H2, dung dịch xuất hiện kết tủa trắng CaCO3.
C©u 11 :
Khi cho các chất: Ag, Cu, CuO, Al, Fe vào dung dịch axit HCl thì các chất đều bị tan hết là:
A.
Cu, Al, Fe B.
Al, Fe, Ag C.
CuO, Al, Fe. D.
Cu, Ag, Fe

Trang 2/3 – MÃ ĐỀ 02
C©u 12 :
Hai thuốc thử nào dưới đây có thể phân biệt được các kim loại: Al, Fe, Mg, Ag?
A.
Dung dịch HCl, qùi tím. B.
Dung dịch HCl, dung dịch AgNO3.
C.
Dung dịch CuSO4, dung dịch BaCl2. D.
Dung dịch HCl, dung dịch NaOH.
C©u 13 :
Lần lượt tiến hành 2 thí nghiệm sau
- Thí nghiệm 1: Cho từ từ dd NH3 đến dư vào dd Al(NO3)3.
- Thí nghiệm 2: Cho từ từ dd NaOH đên dư vào dd Al(NO3)3.
Phát biểu nào sau đây đúng
A.
Thí nghiệm 1 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan
Thí nghiệm 2 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan .
B.
Cả 2 thí nghiệm đều xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan
C.
Thí nghiệm 1 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan .
Thí nghiệm 2 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan.
D.
Cả 2 thí nghiệm đều xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan
C©u 14 :
Từ Mg(OH)2 người ta điều chế Mg bằng cách nào trong các cách sau
1/ Điện phân Mg(OH)2 nóng chảy .
2/ Hoà tan Mg(OH)2 vào dung dịch HCl sau đó điện phân dung dịch MgCl2 có màng ngăn
.
3/ Nhiệt phân Mg(OH)2 sau đó khử MgO bằng CO hoặc H2 ở nhiệt độ cao
4/ Hoà tan Mg(OH)2 vào dung dịch HCl , cô cạn dung dịch sau đó điện phân MgCl2 nóng
chảy
Cách làm đúng là
A.
Chỉ có 4. B.
1 và 4 C.
Cả 1 , 2 , 3 và 4 D.
1 , 3 và 4
C©u 15 :
Hỗn hợp chứa 5,6 gam Fe và 4,8 gam Mg. Cho hỗn hợp tác dụng với axit HCl dư thì thể tích
khí (đktc) thu được là:
A.
6,72 lit B.
8,96 lit C.
4,48 lit D.
11,2 lit.
C©u 16 :
Câu nào đúng trong các câu sau đây ? Trong ăn mòn điện hoá học, xảy ra :
A.
sự khử ở cực âm B.
sự oxi hóa ở cực dương
C.
sự oxi hóa ở cực dương và sự khử ở cực
âm
D.
sự oxi hóa ở cực âm và sự khử ở cực
dương.
C©u 17 :
Nung hỗn hợp muối cacbonat của 2 kim loại kế tiếp nhau trong nhóm IIA tới khối lượng không
đổi thu được 2,24 lít CO2 (đktc) và 4,64 g hỗn hợp hai oxit. Hai kim loại đó là :
A.
Ca và Sr B.
Mg và Ca. C.
Sr và Ba D.
Be và Mg
C©u 18 :
Trong khi làm các thí nghiệm ở lớp hoặc trong các giờ thực hành hóa học có một số khí thải:
Cl2, H2S, SO2, NO2, HCl. Biện pháp để khử các khí trên là
A.
dùng bông tẩm giấm ăn nút ngay ống nghiệm sau khi đã quan sát hiện tượng
B.
dùng bông tẩm xút hoặc nước vôi trong nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
C.
sục khí vào cốc đựng nước
D.
sục khí vào cốc đựng thuốc tím hoặc bông tẩm thuốc tím nút ngay ống nghiệm sau khi đã quan sát
hiện tượng
C©u 19 :
Hòa tan hoàn toàn 7,8g bột Al và Mg trong dd HCl. Sau khi phản ứng xong khối lượng dung
dịch axit tăng thêm 7g. Khối lượng nhôm và magiê trong hỗn hợp đầu là :
A.
7,1g và 0,7g B.
5,4g và 2,4g C.
2,7g và 5,1g D.
3,0g và 4,8g
C©u 20 :
Dung dịch NaOH tác dụng được với tất cả các chất trong dãy nào sau đây ?
A.
CO2, Al, HNO3 , Cu. B.
ZnCl2, Al(OH)3, AgNO3, Ag.
C.
CuSO4 , SO2, H2SO4, NaHCO3 . D.
HCl, NaHCO3, Mg, Al(OH)3
C©u 21 :
Điện phân muối clorua của một kim loại kiềm nóng chảy thu được 0,896 lít khí (đktc) ở anot
và 1,84g kim loại ở catot. Công thức hoá học của muối là:
A.
LiCl. B.
RbCl. C.
NaCl. D.
KCl.
C©u 22 :
Có 5 lọ mất nhãn đựng các dung dịch: KNO3, Cu(NO3)2, FeCl3, AlCl3, NH4Cl. Có thể dùng
hóa chất nào sau đây để nhận biết các dung dịch trên?
A.
Dung dịch AgNO3 B.
Dung dịch Na2SO4 C.
Dung dịch NaOH. D.
Dung dịch HCl
C©u 23 :
Cho các phản ứng:
1. CaCl2 + Na2CO3 → CaCO3 + 2NaCl
2. Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O

Trang 3/3 – MÃ ĐỀ 02
3. CaCO3 + 2CH3COOH → (CH3COO)2Ca + CO2 + H2O
4. CaCO3 + 2KCl → CaCl2 + K2CO3
Phản ứng xảy ra là
A.
2, 3, 4 B.
1, 2, 3, 4 C.
1, 2, 3. D.
1, 3, 4
C©u 24 :
Cho phản ứng : Ag+ + Fe2+ → Ag + Fe3+
Fe2+ là :
A.
Chất khử yếu nhất. B.
Chất oxi hoá yếu nhất.
C.
Chất oxi hoá mạnh nhất. D.
Chất khử mạnh nhất.
C©u 25 :
Cho phản ứng hoá học :
Al + HNO3 → Al(NO3)3 + NO + H2O
Số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat trong phản ứng là :
A.
1 và 3. B.
4 và 3. C.
3 và 2 D.
3 và 4.
C©u 26 :
Khi cho lượng sắt dư tan trong HNO3 loãng thu được dung dịch X có mầu xanh nhạt. Hỏi
trong X chủ yếu có chất gì cho dưới đây:
A.
Fe(NO3)3 + H2O B.
Fe(NO3)2 + H2O.
C.
Fe(NO3)2 + HNO3 + H2O D.
Fe(NO3)2 + Fe(NO3)3 + H2O
C©u 27 :
Cho khí CO (dư) đi vào ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4, CuO thu
được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z.
Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
A.
Mg, Al, Fe, Cu. B.
MgO, Fe, Cu. C.
MgO, Fe3O4, Cu. D.
Mg, Fe, Cu.
C©u 28 :
Trong các phản ứng sau, phản ứng nào không là phản ứng oxi hóa – khử?
A.
4H2SO4 + Fe3O4 → FeSO4 + Fe2(SO4)3
+ 4H2O
B.
6H2SO4 + 2Fe → Fe2(SO4)3 + 3SO2 +
6H2O
C.
H2SO4 + Fe → FeSO4 + H2 D.
4H2SO4 + 2FeO → Fe2(SO4)3 + SO2 +
4H2O
C©u 29 :
Cho 0,04 mol bột Fe vào dung dịch chứa 0,07 mol AgNO3. Khi phản ứng hoàn toàn thì khối
lượng chất rắn thu được là
A.
1,12 gam B.
7,84 gam. C.
4,32 gam D.
6,48 gam
C©u 30 :
Làm sạch Ag có lẫn tạp chất là Al, có thể dùng
1. Dung dịch NaOH dư 2. Dung dịch HCl dư
3. Dung dịch Fe(NO3)2 dư 4. Dung dịch AgNO3 dư
A.
2, 3, 4 B.
1, 2, 4 C.
1, 2, 3 D.
1, 3, 4
Cho : Na = 23 ; Mg = 24 ; Ca = 40 ; Al = 27 ; Fe = 56 ; Ag = 108 ; S = 32 ; C = 12 ; O = 16 ; N = 14.
HẾT
Trang 4/3 – MÃ ĐỀ 02
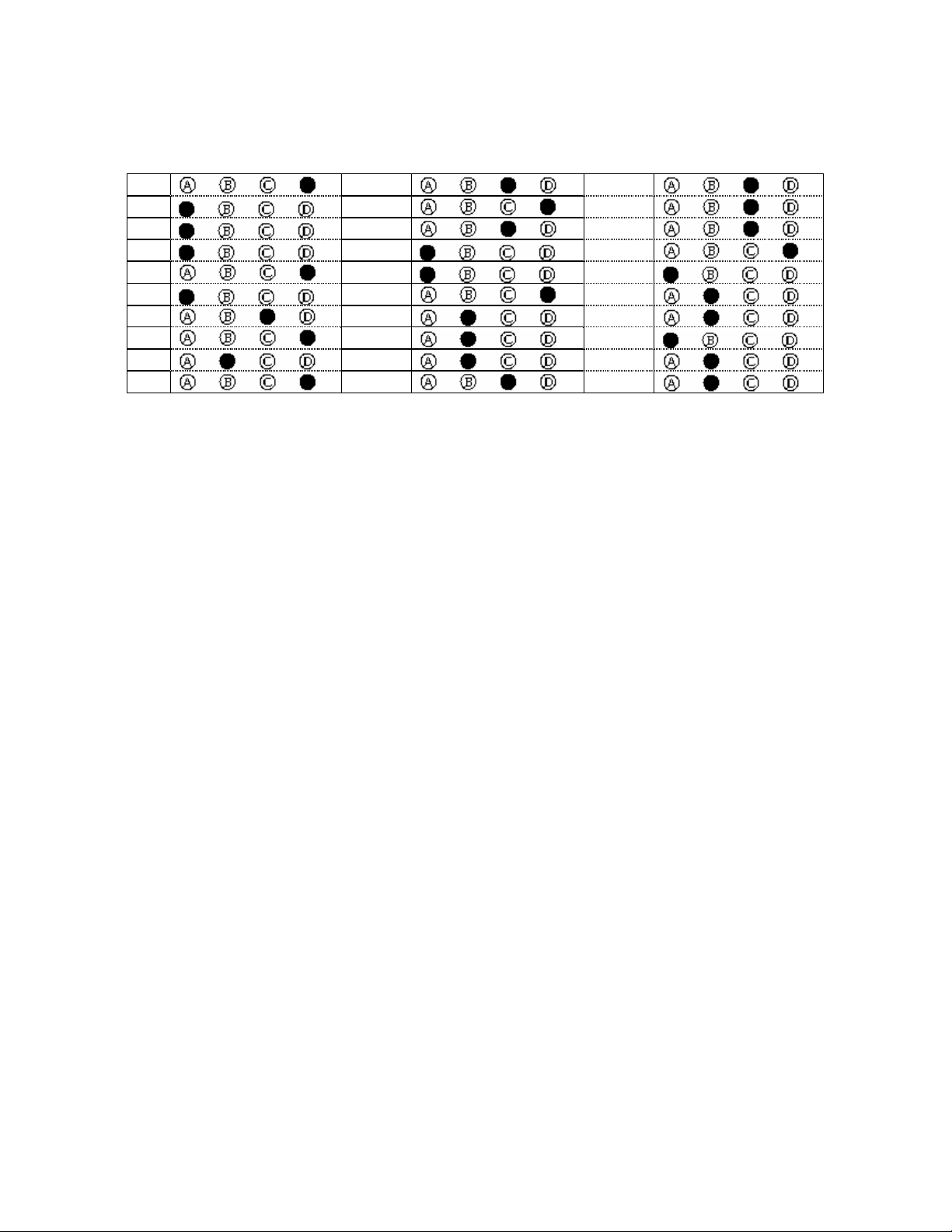
ph iÕu so i - ®¸ p ¸ n
(Dµnh cho gi¸m kh¶o)
k t h o c k i 2 h o a 12
M· ®Ò : 02
01
11
21
02
12
22
03
13
23
04
14
24
05
15
25
06
16
26
07
17
27
08
18
28
09
19
29
10
20
30

Trang 1/3 – MÃ ĐỀ 03
Trường THPT PHAN ĐĂNG LƯU KIỂM TRA HỌC KÌ II (2010-2011)
TỔ HÓA MÔN HÓA KHỐI 12
Thời gian làm bài : 45 phút
Đề kiểm tra gồm có 3 trang. Ngày kiểm tra: 03/4/2011
MÃ ĐỀ 03
C©u 1 :
Cho dung dịch NH3 đến dư vào dung dịch hỗn hợp AlCl3, ZnCl2 thu được kết tủa A. Nung A
đến khối lượng không đổi thu được chất rắn B. Cho H2 (dư) qua B nung nóng thu được chất
rắn ...
A.
Al2O3. B.
ZnO và Al2O3. C.
Zn và Al2O3. D.
ZnO và Al.
C©u 2 :
Cần phải thêm bao nhiêu ml dung dịch NaOH 0,25M vào 50ml dung dịch hỗn hợp HCl 0,1M
và H2SO4 0,05M để thu được dung dịch có pH = 2,0 ?
A.
36,54ml. B.
40,75ml. C.
27,75ml. D.
43,75ml.
C©u 3 :
Cho phản ứng hoá học :
Al + HNO3 → Al(NO3)3 + NO + H2O
Số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat trong phản ứng là :
A.
3 và 4. B.
4 và 3. C.
3 và 2 D.
1 và 3.
C©u 4 :
Khi hoà tan một vật bằng nhôm vào dung dịch NaOH, phản ứng đầu tiên xảy ra sẽ là :
A.
Al2O3 + 2NaOH
2NaAlO2 + H2O
Hay Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
B.
2Al + 2NaOH + 2H2O
2NaAlO2 + 3H2
C.
Al(OH)3 + NaOH
NaAlO2 + 2H2O
D.
2Al + 6H2O
2Al(OH)3 + 3H2
C©u 5 :
Lần lượt tiến hành 2 thí nghiệm sau
- Thí nghiệm 1: Cho từ từ dd NH3 đến dư vào dd Al(NO3)3.
- Thí nghiệm 2: Cho từ từ dd NaOH đên dư vào dd Al(NO3)3.
Phát biểu nào sau đây đúng
A.
Cả 2 thí nghiệm đều xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan
B.
Thí nghiệm 1 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan .
Thí nghiệm 2 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan.
C.
Cả 2 thí nghiệm đều xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan
D.
Thí nghiệm 1 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa tan
Thí nghiệm 2 xuất hiện kết tủa keo trắng đến tối đa sau đó kết tủa giữ nguyên không tan .
C©u 6 :
Khi cắt miếng Na kim loại,bề mặt vừa cắt có ánh kim lập tức mờ đi,đó là do có sự hình thành
các sản phẩm rắn nào sau đây?
A.
Na2O , Na2CO3 , NaHCO3 B.
Na2O, NaOH , Na2CO3 , NaHCO3.
C.
Na2O , NaOH , Na2CO3 D.
NaOH , Na2CO3 , NaHCO3.
C©u 7 :
Phát biểu nào sau đây là phù hợp với tính chất hóa học chung của kim loại ?
A.
Kim loại có tính khử, nó bị oxi hóa thành ion dương.
B.
Kim loại có tính oxi hóa, nó bị oxi hóa thành ion dương
C.
Kim loại có tính khử, nó bị khử thành ion âm
D.
Kim loại có tính oxi hóa, nó bị khử thành ion âm
C©u 8 :
Hai thuốc thử nào dưới đây có thể phân biệt được các kim loại: Al, Fe, Mg, Ag?
A.
Dung dịch HCl, qùi tím. B.
Dung dịch HCl, dung dịch NaOH.
C.
Dung dịch CuSO4, dung dịch BaCl2. D.
Dung dịch HCl, dung dịch AgNO3.
C©u 9 :
Cho phản ứng : Ag+ + Fe2+ → Ag + Fe3+
Fe2+ là :
A.
Chất khử yếu nhất. B.
Chất oxi hoá yếu nhất.
C.
Chất oxi hoá mạnh nhất. D.
Chất khử mạnh nhất.
C©u 10 :
Điện phân muối clorua của một kim loại kiềm nóng chảy thu được 0,896 lít khí (đktc) ở anot
và 1,84g kim loại ở catot. Công thức hoá học của muối là:






















![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



