
S
Ở GD&ĐT NINH THUẬN
TRƯỜNG THPT TRƯỜNG CHINH
ĐỀ THI HỌC KỲ II – Năm học 2012-2013
MÔN: HÓA HỌC 10
Thời gian làm bài: 45 phút;
(40 câu trắc nghiệm)
(Đề gồm có 3 trang) Mã đề thi 209
Họ, tên thí sinh:…......................................................................SBD:………….
(Cho Na = 23, Mg =24, Al =27, Mn = 55, Fe =56, Cu = 64, Zn = 65, Ag =108, F = 19, Br =80,
S = 32, O = 16, H =1 và Cl =35,5 )
I. PHẦN CHUNG (7,0 điểm) (Dành cho tất cả học sinh )
Câu 1: Trong các phương pháp sau đây, phương pháp nào được dùng để điều chế O2 trong phòng thí nghiệm?
A. Chưng cất phân đoạn không khí lỏng. B. Điện phân dung dịch CuSO4.
C. Điện phân H2O. D. Phân hủy H2O2 với xúc tác MnO2.
Câu 2: Cho 8,7 g MnO2 tác dụng với HCl đậm đặc sinh ra V lít khí clo (đktc). V có giá trị là:
A. 2,24 lit B. 4,48 lít C. 1,904 lít D. 3,36 lít
Câu 3: Hằng số cân bằng của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Áp suất B. Chất xúc tác
C. Nhiệt độ D. Nồng độ các chất phản ứng
Câu 4: Cho phản ứng ở trạng thái cân bằng: N2 (k) + 3H2 (k) 2NH3 (k)
H
< 0. Những thay đổi nào sau
đây làm cân bằng dịch chuyển theo chiều thuận?
A. Tăng nồng độ các chất N2 và H2 B. Tăng nhiệt độ
C. Giảm áp suất. D. Tăng nồng độ NH3
Câu 5: Để pha loãng dung dịch H2SO4 đặc trong phòng thí nghiệm, người ta tiến hành theo cách nào dưới đây?
A. cho nhanh axit vào nước và khuấy đều. B. cho từ từ nước vào axit và khuấy đều.
C. cho từ từ axit vào nước và khuấy đều. D. cho nhanh nước vào axit và khuấy đều.
Câu 6: Chất khí được dùng để diệt trùng nước sinh hoạt, nước bể bơi... là :
A. F2 B. Cl2 C. N2 D. CO2
Câu 7: Chỉ ra phương trình hóa học của phản ứng sản xuất clo trong công nghiệp :
A. 4HCl + MnO2 MnCl2 + Cl2 + 2H2O
B. NaCl
®pnc
Na + 1/2Cl2
C. 2NaCl + 2H2O → Cl2 + H2 + 2NaOH
D. 16HCl + 2KMnO4 2MnCl2 + 5Cl2 + 2KCl + 8H2O
Câu 8: Tốc độ phản ứng phụ thuộc vào các yếu tố nào sau đây :
A. chất xúc tác, diện tích bề mặt . B. Nồng độ, áp suất.
C. Nhiệt độ. D. Tất cả các yếu tố.
Câu 9: Phản ứng được dùng để sản xuất HCl trong công nghiệp :
A. 2NaCl + H2SO4 0
400 C
Na2SO4 + 2HCl
B. Cl2 + H2 0
t
2HCl
C. NaCl + H2SO4 0
250 C
NaHSO4 + HCl
D. CH4 + 4Cl2
askt
CCl4 + 4HCl
Câu 10: Chất nào được dùng để khắc chữ lên thủy tinh ?
A. Dung dịch H2SO4 đặc. B. Dung dịch HF
C. Dung dịch HClO4. D. Dung dịch NaOH.

Câu 11: Cho5,6 gam sắt tác dụng vừa đủ với dung dịch HCl 2M thu được khí H2 ở đktc. Thể tích (ml) dung
dịch HCl cần dùng là:
A. 400 B. 100 C. 200 D. 300
Câu 12: Cho m gam Fe tác dụng hoàn toàn với dung dịch H2SO4 dư thu được 4,48 lít khí H2 (ở đktc). Giá trị
của m là :
A. 16,8 gam B. 1,68 gam C. 11,2 gam D. 1,12 gam
Câu 13: Thứ tự tăng dần tính axit của các axit halogen hiđric (HX) là
A. HF < HCl < HBr < HI. B. HCl < HBr < HI < HF.
C. HBr < HI < HCl < HF. D. HI < HBr < HCl < HF.
Câu 14: Cho Zn phản ứng vừa đủ với 4,8 g S. Cho dung dịch H2SO4 dư vào sản phẩm thu được. Thể tích khí
(đktc) thu được sau phản ứng là( biết các phản ứng xảy ra hoàn toàn)
A. 2,24 lit B. 5,60 lít C. 3,36 lít D. 4,48 lít
Câu 15: Dùng không khí nén thổi vào lò cao để đốt cháy than cốc ( trong sản xuất gang), yếu tố nào ảnh hưởng
đến tốc độ phản ứng ?
A. Nồng độ. B. tăng diện tích tiếp xúc.
C. Nhiệt độ, áp suất. D. xúc tác.
Câu 16: Dãy kim loại phản ứng được với H2SO4 loãng là:
A. K, Mg, Al, Fe, Zn B. Au, Pt, Al
C. Cu, Zn, Na D. Ag, Ba, Fe, Sn
Câu 17: Có 4 dung dịch NaF, NaCl, NaBr, NaI đựng trong các lọ bị mất nhãn. Nếu dùng dung dịch AgNO3 thì
có thể nhận được
A. 1 dung dịch. B. 4 dung dịch. C. 3 dung dịch. D. 2 dung dịch.
Câu 18: Trong các phản ứng sau, phản ứng nào có thể dùng để điều chế SO2 trong phòng thí nghiệm?
A. S + O2 ->SO2 B. 4FeS2 + 11O2 ->2Fe2O3 + 8SO2
C. 2H2S + 3O2 ->2SO2 + 2H2O D. Na2SO3 + H2SO4 ->Na2SO4 + H2O + SO2
Câu 19: Trong nhóm VIA, đi từ O đến Te thì bán kính nguyên tử
A. tăng, tính oxi hoá giảm. B. giảm, tính oxi hoá giảm.
C. tăng, tính oxi hoá tăng. D. giảm, tính oxi hoá tăng.
Câu 20: Để phân biệt SO2 và CO2 người ta thường dùng thuốc thử nào?
A. Dung dịch brom. B. Nước clo.
C. Nước vôi trong D. Hồ tinh bột.
II. PHẦN RIÊNG (3,0 điểm)
(Học sinh học chương trình nào thì làm phần dành riêng cho chương trình đó)
A. Dành cho chương trình nâng cao:
Câu 21: Phản ứng nào sau đây không xảy ra?
A. H2S + Pb(NO3)2 PbS + 2HNO3. B. FeS + 2HCl FeCl2 + H2S.
C. K2S + Pb(NO3)2 PbS + 2KNO3. D. CuS + 2HCl CuCl2 + H2S.
Câu 22: Cho 4,28g hỗn hợp (Al, Zn) tác dụng với dung dịch H2SO4 đặc, nguội thu được 896 ml khí SO2 (đkc).
Phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu là:
A. 35,75% và 64,25% B. 48,67% và 51,33%
C. 50%và 50% D. 60,75% và 39,25%
Câu 23: Một hỗn hợp gồm 3 muối NaF, NaCl và NaBr nặng 4,82g. Hoà tan hoàn toàn trong nước được dung
dịch X. Sục khí clo dư vào dung dịch X rồi cô cạn hoàn toàn dung dịch sau phản ứng thu được 3,93g muối
khan. Lấy 1/2 lượng muối khan này hoà tan vào nước rồi cho sản phẩm phản ứng với dung dịch AgNO3 dư thì
thu được 4,305g kết tủa. Phần trăm khối lượng muối NaCl trong hỗn hợp ban đầu là:
A. 48,55% B. 42,74% C. 34,85% D. 8,71%
Câu 24: Cho phản ứng : N2 (k) + 3H2 (k) 2NH3 (k) số mol ban đầu của N2 và H2 lần lượt là 2 và 5 mol. Khi

phản ứng đạt đến trạng thái cân bằng thì thu được 1,5 mol NH3. Vậy hằng số cân bằng của phản ứng trên là:
A. 4,2.10-4 B. 8,5.10-4 C. 9.10-3 D. 0,0866
Câu 25: Axit cloric có công thức
A. HClO4. B. HClO. C. HClO3. D. HClO2.
Câu 26: Chất nào được dùng để tráng lên phim ảnh ?
A. AgBr B. AgF C. AgI D. AgCl
Câu 27: Cho các cân bằng sau:
(1): 2 SO2 (k) + O2 (k) 2SO3(k) (2): N2 (k) + 3 H2 (k) 2NH3 (k)
(3): CO2 (k) + H2 (k) CO (k) + H2O (k) (4): 2 HI (k) H2 (k) + I2 (k)
Khi thay đổi áp suất, nhóm gồm các cân bằng hoá học đều không bị chuyển dịch là:
A. (1) và (3) B. (1) và (2) C. (3) và (4) D. (2) và (4).
Câu 28: Lớp ozon ở tầng bình lưu khí quyển là tấm lá chắn tia tử ngoại của mặt trời, bảovệ sự sống trên trái
đất. Hiện tượng suy giảm tầng ozon đang là một vấn đề môi trường toàn cầu. Nguyên nhân của hiện tượng này
là do :
A. Một nguyên nhân khác. B. Chất thải CFC do con người gây ra.
C. Sự thay đổi khí hậu. D. Các hợp chất hữu cơ.
Câu 29: Trong phản ứng hóa học : H2O2 + 2KI → I2 + 2KOH.
A. KI là chất oxi hóa. B. H2O2 là chất khử.
C. H2O2 vừa là chất oxi hóa, vừa là chất khử. D. H2O2 là chất oxi hóa.
Câu 30: Chất nào trong các chất dưới đây có thể nhận ngay được bột gạo ?
A. Dung dịch H2SO4 B. Dung dịch HCl C. Dung dịch Br2 D. Dungdịch I2.
B. Dành cho chương trình cơ bản:
Câu 31: Cho phản ứng: Fe2O3 (r) + 3CO (k) 2Fe (r) + 3CO2 (k). Khi tăng áp suất của phản ứng này
thì
A. cân bằng chuyển dịch theo chiều thuận. B. cân bằng không bị chuyển dịch.
C. cân bằng chuyển dịch theo chiều nghịch. D. phản ứng dừng lại.
Câu 32: Cho khí H2S lội qua dd CuSO4 thấy có kết tủa màu xám đen xuất hiện, chứng tỏ:
A. Có phản ứng oxi hoá – khử xảy ra. B. axit sunfuric mạnh hơn axit sunfuhiđric.
C. có kết tủa CuS tạo thành, không tan trong axit mạnh D. axit sunfuhiđric mạnh hơn axit sunfuric.
Câu 33: Đặc điểm nào dưới đây là đặc điểm chung của các nguyên tố halogen ?
A. Tác dụng mạnh với nước B. Ở điều kiện thường là chất khí
C. Có tính oxi hóa mạnh D. Vừa có tính oxi hoá, vừa có tính khử
Câu 34: Các khí sinh ra khi cho saccarozơ vào dung dịch H2SO4 đặc, dư gồm:
A. SO3 và CO2. B. SO2 và CO2
C. H2S và CO2. D. H2S và SO2.
Câu 35: Để nhận ra sự có mặt của ion sunfat trong dung dịch, người ta thường dùng
A. dung dịch muối Mg2+. B. dung dịch chứa ion Ba2+
C. quỳ tím. D. thuốc thử duy nhất là Ba(OH)2
Câu 36: Trong 4 hỗn hợp sau đây, hỗn hợp nào là nước Javen
A. NaCl + NaClO + H2O B. NaCl +HClO+ H2O
C. NaCl + NaClO3 + H2O D. NaCl + NaClO2 + H2O
Câu 37: Brom có lẫn một ít tạp chất là clo. Một trong các hoá chất có thể loại bỏ clo ra khỏi hỗn hợp là
A. KCl. B. H2O. C. NaOH. D. KBr.
Câu 38: Hiện tượng xảy ra khi cho giấy quỳ tím vào nước clo :
A. Quỳ tím hoá đỏ. B. Quỳ tím mất màu.
C. Quỳ tím không đổi màu. D. Lúc đầu quỳ tím hoá đỏ, sau đó mất màu.
Câu 39: Cho 11,2 g hỗn hợp (Mg, Cu) tan hết trong H2SO4 loãng dư, thu được 4,48 lít khí(đkc). Phần trăm khối
lượng của Mg và Cu trong hỗn hợp đầu là:
A. 42,86% và 57,14% B. 50%và 50%
C. 75,75% và 24,25% D. 8,57% và 91,43%
Câu 40: SO2 vừa có tính oxi hoá, vừa có tính khử vì trong phân tử SO2
A. S có mức oxi hoá cao nhất. B. S có mức oxi hoá trung gian.
C. S còn có một đôi electron tự do. D. S có mức oxi hoá thấp nhất.
-----------------------------------------------
----------- HẾT ----------
SỞ GD&ĐT NINH THUẬN ĐÁP ÁN THI HỌC KỲ II - Năm học 2012-2013
TRƯỜNG THPT TRƯỜNG CHINH MÔN: HÓA HỌC 10.
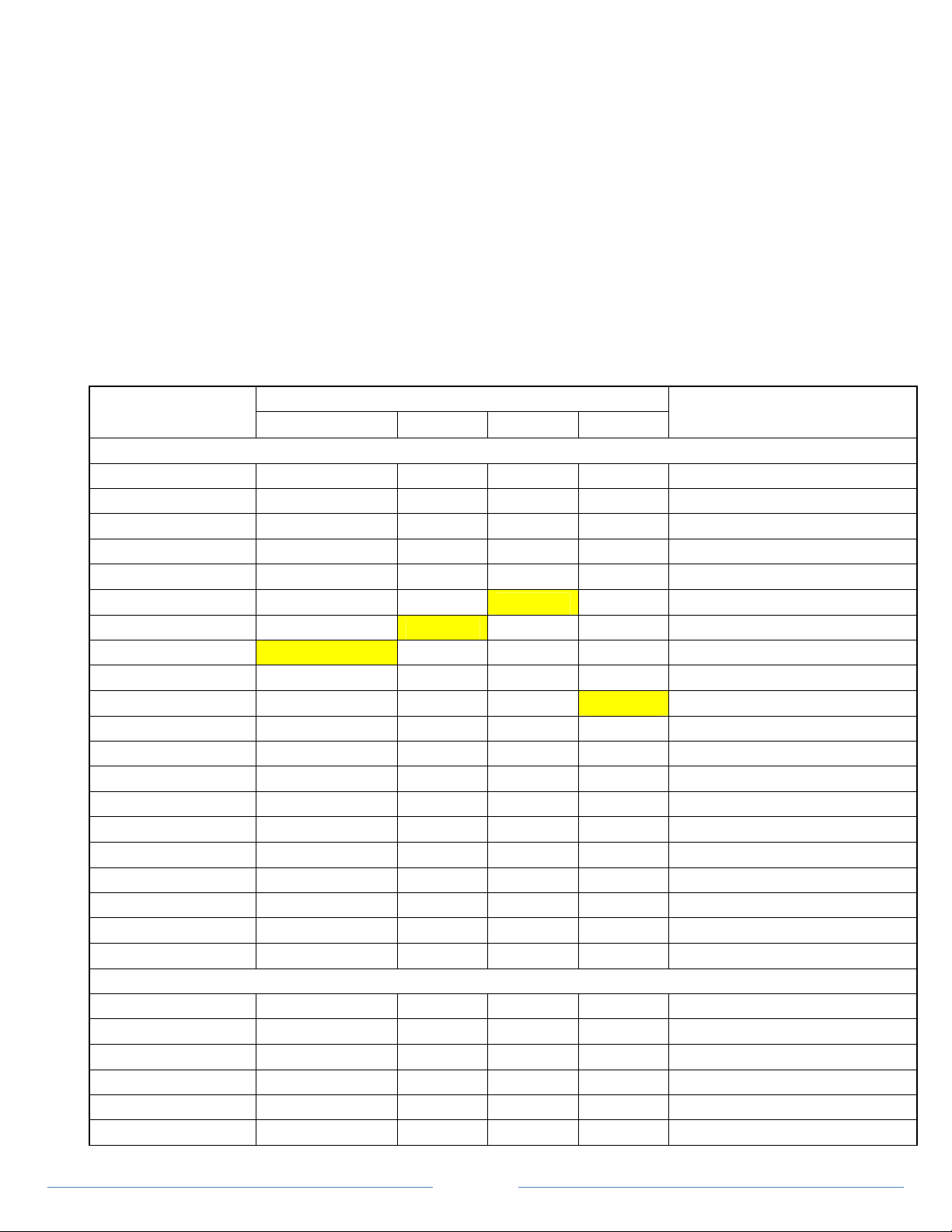
Câu Đáp án các mã đề Biểu điểm
132 209 357 485
I. PHẦN CHUNG (7,0 điểm)
1 B D C B 0,35
2 C A C A 0,35
3 D C D D 0,35
4 B A C C 0,35
5 D C A D 0,35
6 A B C D 0,35
7 B C D D 0,35
8 C D C A 0,35
9 B B B A 0,35
10 B B A A 0,35
11 C B A A 0,35
12 D C A A 0,35
13 A A B A 0,35
14 A C C D 0,35
15 B C A A 0,35
16 C A B C 0,35
17 A B D C 0,35
18 B D A C 0,35
19 D A B B 0,35
20 C A C C 0,35
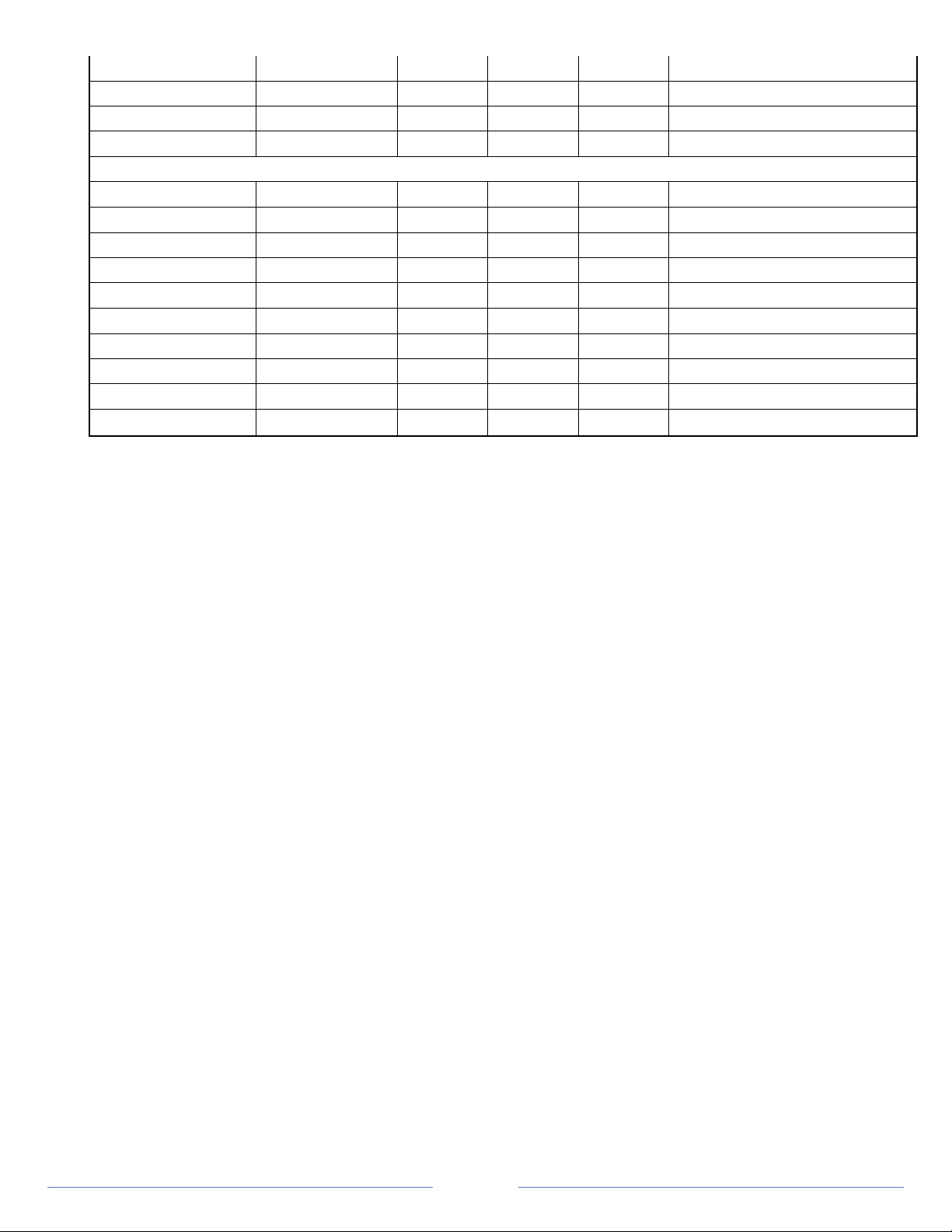
II.A. PHẦN NÂNG CAO (3,0 điểm)
21 A D C B 0,3
22 C D A C 0,3
23 D A C B 0,3
24 D D D B 0,3
25 C C B D 0,3
26 C A C C 0,3
27 D C D D 0,3
28 A B A B 0,3
29 D D B C 0,3
30 A D B B 0,3
II.B. PHẦN CƠ BẢN (3,0 điểm)
31 D B B B 0,3
32 D C A C 0,3
33 A C D A 0,3
34 C B B B 0,3
35 B B A C 0,3
36 A A D D 0,3
37 C D D A 0,3
38 B D D B 0,3
39 B A B D 0,3
40 A B D D 0,3












![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



