KIỂM TRA HỌC KÌ I
I. MỤC TIÊU:
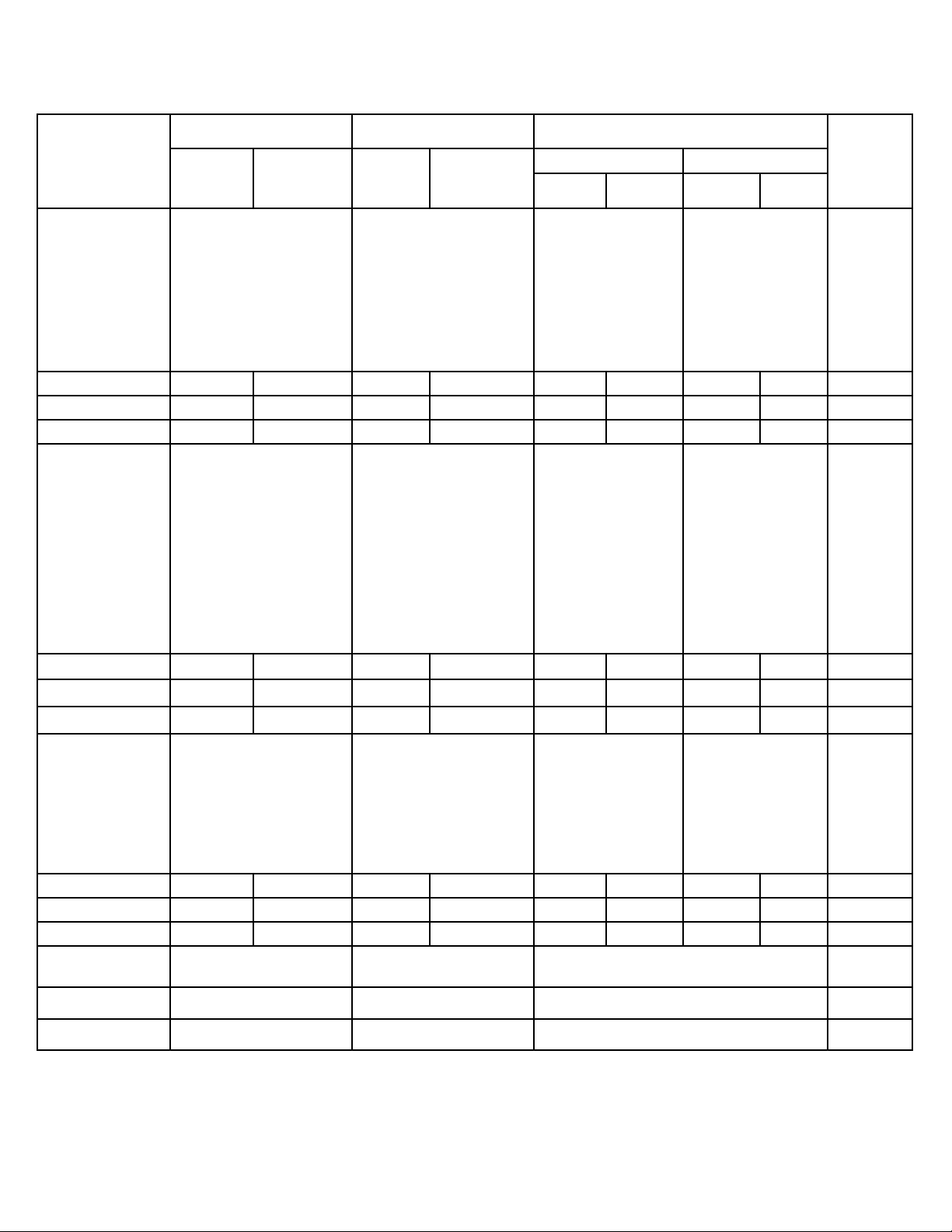
Cấp
độ
Chủ
đề
Nhận biết Thông hiểu Vận dụng
Tổng
TN TL TN TL
Cấp thấp Cấp cao
TN TL TN TL
Các hợp chất
vô cơ
Nắm được tính chất
của từng loại hợp
chất vơ cơ và phân
loại được chúng
Dựa vào mối quan
hệ giữa các hợp
chất vô cơ để hoàn
thành dãy chuyển
hóa. Tính chất của
từng loại hợp chất
vô cơ.
Dựa vào mối
quan hệ giữa
các hợp chất vô
cơ để hoàn
thành dãy
chuyển hóa
Số câu 8 2 1/3 1/3 9+2/3
Số điểm 2,7 0,7 0,5 0,5 4,4
Tỉ lệ% 27% 7% 5% 5% 44%
Kim loại. Phi
kim
Nắm được tính chất
hóa học của kim
loại, biết cách sắp
xếp dãy hoạt động
hóa học. Nắm được
các tính chất vật lý
của khí clo
Nhận biết muối
sunfat và axit
sunfuric. Dựa vào
tính chất hóa học
của kim loại để
hoàn thành dãy
chuyển hóa.
- Tính chất hóa học
của kim loại
Nêu hiện tượng
xảy ra khi cho
kim loại vào
dung dịch axit
Số câu 4 1 1/3+1/3 1 6+2/3
Số điểm 1,3 0,3 1,5 1 4,1
Tỉ lệ % 13% 3% 5% 10% 41%
Tính toán Tính khối lượng
dung dịch axit
Tính thành
phần phần trăm
theo khối
lượng mỗi chất
có trong hốn
hợp ban đầu.
Số câu 1/3 1/3 2/3
Số điểm 0,5 1 1,5
Tỉ lệ % 5% 10% 15%
Tổng số câu 12 3+1/3+2/3 1+1/3+2/3 18
Tổng số điểm 4,0 3,0 3,0 10
Tổng tỉ lệ 40% 30% 30% 100%

BẢNG ĐẶC TẢ
Chủ đề Mức độ Nội dung Câu hỏi
TN/TL
Các loại
hợp chất
vô cơ
- Nêu hiện tượng xảy ra của các phản ứng hóa học.
- Nhận biết hợp chất oxit axit.
- Những kim loại nào phản ứng được với dung dịch
axit loãng.
- Một số bazơ không tan bị nhiệt phân hủy.
- Sự đổi màu của quỳ tím khi nhúng vào dung dịch
axit/bazơ.
- Nhận biết các loại phân bón hóa học.
- Phản ứng trung hòa.
- Nhận biết muối sunfat và axit sunfuric.
- Cách pha loãng axit đặc.
- Hiểu được các chất tồn tại trong một dung dịch.
Kim loại.
Phi kim
- Sắp xếp các kim loại theo chiều tăng/giảm dần
khả năng hoạt động hóa học.
- Những kim loại nào phản ứng được với dung
dịch axit HNO3 và H2SO4 đặc.
- Tính chất vật lí của clo.
- Tính chất vật lí của kim loại.
- Xác định kim loại để tinh chế muối.
- Nêu hiện tượng và viết phương trình hóa học xảy
ra khi cho các chất phản ứng với nhau.
Tính
toán
Vận dụng - Tính thành phần phần trăm theo khối lượng mỗi
chất có trong hốn hợp ban đầu.
- Tính khối lượng dung dịch axit

ĐỀ 1
I.TRẮC NGHIỆM: (5,0 điểm)
Trả lời các câu hỏi sau bằng cách chọn đáp án đúng A,B,C hoặc D và ghi vào giấy làm bài.
Câu 1: Dãy kim loại đươWc săXp xêXp theo chiêYu hoaWt đôWng hoXa hoWc tăng dần là:
A. K, Al, Mg, Cu, Fe B. Cu, Fe, Mg, Al, K
C. Cu, Fe, Al, Mg, K D. K, Cu, Al, Mg, Fe
Câu 2: Kim loại nào sau đây tác dụng được với dd H2SO4 loãng?
A. Al, Mg, Cu B. Fe, Ag, Al.
C. Fe, Al, Mg. D. Mg, Fe, Ag
Câu 3: Hãy cho biết hiện tượng hóa học khi cho dung dịch HCl vào ống nghiệm chứa dung dịch
Na2CO3?
A. Sủi bọt khí B. Không có hiện tượng gì
C. Dung dịch chuyển sang màu xanh D. Xuất hiện kết tủa màu trắng
Câu 4: Kim loại nào không phản ứng với HNO3 và H2SO4 đặc nguội ?
A. Zn, Fe B. Mg, Al C. Fe, Al D. Zn, Mg
Câu 5: Trong các oxit sau oxit nào là oxit axit?
A. NO2, CO2, P2O5 B. CuO, NO2, CO2
C. FeO, MgO, K2O D. CaO, ZnO, CO2
Câu 6: Sản phẩm của phản ứng phân huỷ Fe(OH)3 bởi nhiệt là :
A. FeO và H2O B. FeO và H2
C. Fe2O3 và H2 D. Fe2O3 và H2O
Câu 7: Quỳ tím làm dung dịch axit biến đổi thành màu gì?
A. Màu xanh B. Màu đỏ C. Không đổi màu D. Màu vàng
Câu 8: Khí clo có màu gì?
A. Màu đỏ nâu. B. Màu xanh lam.
C. Màu vàng lục. D. Màu tím.
Câu 9: Trong tất cả các kim loại sau đây, kim loại nào dẫn điện tốt nhất?
A. Vàng (Au) B. Bạc (Ag)
C. Đồng (Cu) D. Nhôm (Al)
Câu 10: Để tinh chế dung dịch ZnSO4 có lẫn tạp chất CuSO4 có thể dùng lượng dư kim loại
A. Zn B. Fe C. Cu D. Al
Câu 11: Muối pha loãng axit sunfuric đặc người ta làm như thế nào?
A. Rót từ từ nước vào lọ đựng axit B. Rót từ từ axit đặc vào lọ đựng nước
C. Rót nhanh nước vào lọ đựng axit D. Rót nhanh axit đặc vào lọ đựng nước
Câu 12: Phân bón nào sau đây thuộc loại phân bón đơn?
A. NPK B. (NH4)2HPO4C. CO(NH2)2D. KNO3
Câu 13: Phản ứng giữa H2SO4 và NaOH thuộc loại phản ứng
A. thế B. phân hủy C. hóa hợp D. trung hòa
Câu 14: Cặp chất nào sau đây cùng tồn tại trong dung dịch?(không phản ứng được với nhau)
A. HCl, KCl B. HCl và Ca(OH)2
C. H2SO4 và BaO D. NaOH và H2SO4
Câu 15: Để nhận biết 3 dung dịch bị mất nhãn : Na2SO4, HCl, H2SO4 loãng , người ta dùng
A. quỳ tím B. quỳ tím và dd BaCl2
C. quỳ tím và Fe D. dd BaCl2 và dd AgNO3
II. TỰ LUẬN: (5,0 điểm)
Câu 1: (1,5 điểm) Viết các phương trình hóa học thực hiện sơ đồ chuyển hoá sau: (ghi điều kiện
phản ứng nếu có).
Fe
(1)
FeCl3
(2)
Fe(OH)3
(3)
Fe2O3

Câu 2: (2,5 điểm) Hòa tan 6,3 gam hỗn hợp A gồm magie và nhôm vào dung dịch axit H2SO4
19,6% . Sau phản ứng thu được 6,72 lit khí hiđro (đktc).
a/ Viết phương trình hóa học xảy ra.
b/ Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp A.
c/ Tính khối lượng dung dịch H2SO4 đã dùng.
Câu 3: (1,0 điểm) Nêu hiện tượng và viết phương trình hóa học của phản ứng xảy ra khi nhúng kim
loại kẽm vào dung dịch đồng (II) sunfat.
( Cho Mg = 24 , Cu = 64 , O = 16 , H = 1 , S = 32, Al = 27 )
-----Hết-----
(Cán bộ coi thi không giải thích gì thêm)
ĐỀ 2
I. TRẮC NGHIỆM: (5,0 điểm)
Trả lời các câu hỏi sau bằng cách chọn đáp án đúng A,B,C hoặc D và ghi vào giấy làm bài.
Câu 1: Phân bón nào sau đây thuộc loại phân bón đạm (urê)?
A. NPK B. (NH4)2HPO4C. CO(NH2)2D. KNO3
Câu 2: Kim loại nào sau đây tác dụng được với dd H2SO4 loãng?
A. Al, Mg, Cu B. Fe, Ag, Al.
C. Fe, Al, Mg. D. Mg, Fe, Ag
Câu 3: Khí clo có màu gì?
A. Màu đỏ nâu. B. Màu xanh lam.
C. Màu vàng lục. D. Màu tím.
Câu 4: Kim loại nào không phản ứng với HNO3 và H2SO4 đặc nguội ?
A. Zn,Fe B. Mg,Al C. Fe,Al D. Zn,Mg
Câu 5: Để nhận biết 3 dung dịch bị mất nhãn : Na2SO4, HCl, H2SO4 loãng , người ta dùng
A. qùy tím B. qùy tím và dd BaCl2
C. qùy tím và Fe D. dd BaCl2 và dd AgNO3
Câu 6: Sản phẩm của phản ứng phân huỷ Cu(OH)2 bởi nhiệt là :
A. CuO và H2O B. CuO và H2
C. Cu2O và H2 D. CuO2 và H2O
Câu 7: Dãy kim loại đươWc săXp xêXp theo chiêYu hoaWt đôWng hoXa hoWc tăng dần là:
A. K, Al, Mg, Cu, Fe B. Cu, Fe, Mg, Al, K
C. Cu, Fe, Al, Mg, K D. K, Cu, Al, Mg, Fe
Câu 8: Quỳ tím làm dung dịch bazơ biến đổi thành màu gì?
A. Màu xanh B. Màu đỏ C. Không đổi màu D. Màu vàng
Câu 9: Cặp chất nào sau đây cùng tồn tại trong dung dịch?(không phản ứng được với nhau)
A. HCl, KCl B. HCl và Ca(OH)2
C. H2SO4 và BaO D. NaOH và H2SO4
Câu 10: Trong các oxit sau oxit nào là oxit bazơ?
A. NO2, CO2, P2O5 B. CuO, NO2, CO2
C. FeO, MgO, K2O D. CaO, ZnO, CO2
Câu 11: Để tinh chế dung dịch ZnSO4 có lẫn tạp chất CuSO4 có thể dùng lượng dư kim loại
A. Zn B. Fe C. Cu D. Al
Câu 12: Phản ứng giữa axit và bazơ thuộc loại phản ứng
A. thế B. phân hủy C. hóa hợp D. trung hòa

Câu 13: Trong tất cả các kim loại sau đây, kim loại nào có nhiệt độ nóng chảy cao nhất?
A. Wonfram (W) B. Bạc (Ag)
C. Đồng (Cu) D. Nhôm (Al)
Câu 14: Hãy cho biết hiện tượng hóa học khi cho dung dịch HCl vào ống nghiệm chứa dung dịch
Na2CO3?
A. Sủi bọt khí B. Không có hiện tượng gì
C. Dung dịch chuyển sang màu xanh D. Xuất hiện kết tủa màu trắng
Câu 15: Muối pha loãng axit sunfuric đặc người ta làm như thế nào?
A. Rót từ từ nước vào lọ đựng axit B. Rót từ từ axit đặc vào lọ đựng nước
C. Rót nhanh nước vào lọ đựng axit D. Rót nhanh axit đặc vào lọ đựng nước
II. TỰ LUẬN: (5,0 điểm)
Câu 1: (1,5 điểm) Viết các phương trình hóa học thực hiện sơ đồ chuyển hoá sau: (ghi điều kiện
phản ứng nếu có).
Al
(1)
AlCl3
(2)
Al(NO)3
(3)
Al(OH)3
Câu 2: (2,5 điểm) Cho 9,2 gam hỗn hợp A gồm nhôm và kẽm vào dung dịch axit H2SO4 19,6%. Sau
phản ứng thu được 5,6 lit khí hiđro (đktc).
a/ Viết phương trình hóa học xảy ra.
b/ Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp A.
c/ Tính khối lượng dung dịch H2SO4 đã dùng
Câu 3: (1,0 điểm) Nêu hiện tượng và viết phương trình hóa học của phản ứng xảy ra khi nhúng kim
loại đồng vào dung dịch bạc nitrat.
( Cho Zn = 65 , Cu = 64 , O = 16 , H = 1 , S = 32, Al = 27 )
-----Hết-----
(Cán bộ coi thi không giải thích gì thêm)












![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



