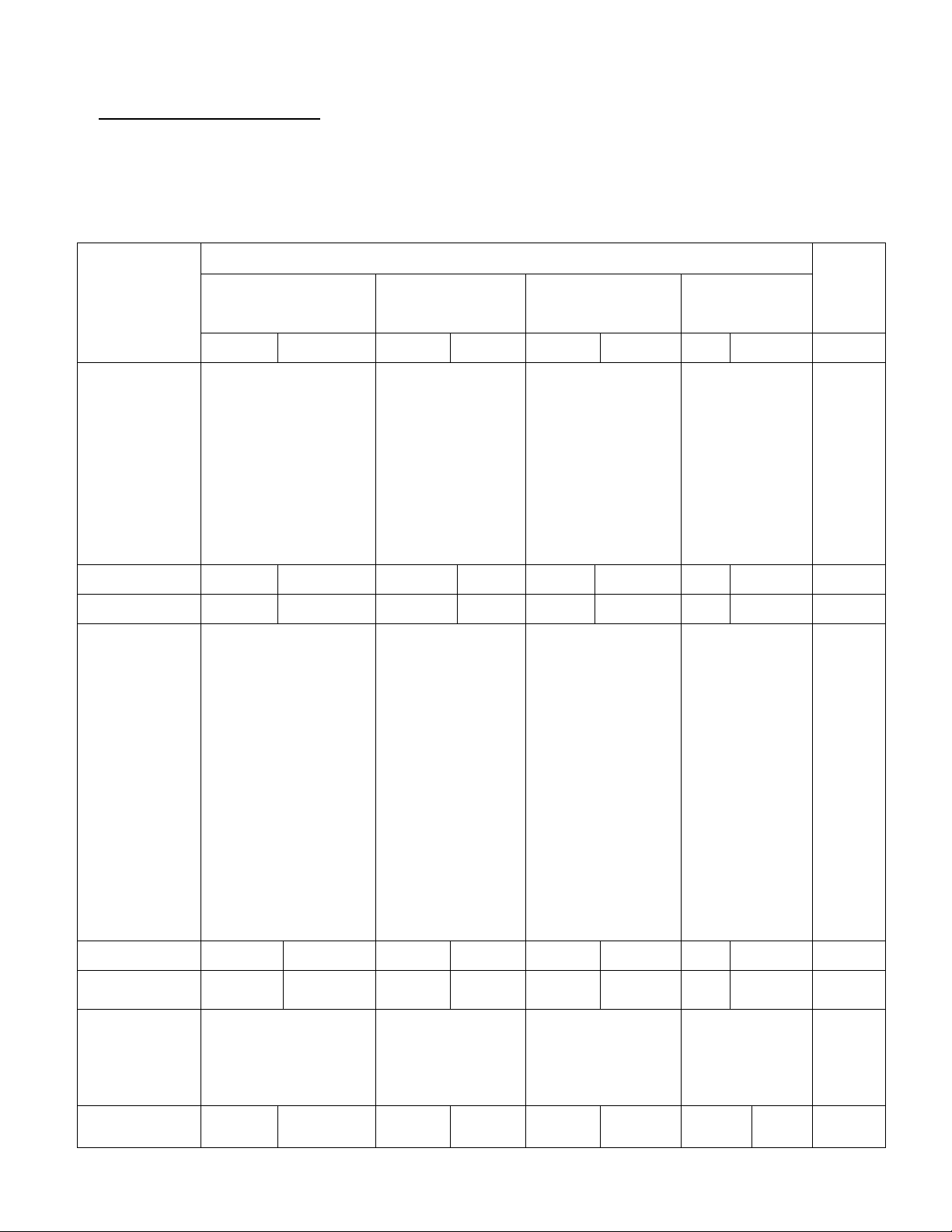
PHÒNG GD & ĐT ĐÔNG HƯNG MA TRẬN ĐỀ KIỂM TRA HỌC KÌ II
TRƯỜNG THCS QUANG DƯƠNG MÔN HÓA HỌC 8
NĂM HỌC 2022 – 2023
Nội dung
kiến thức
Mức độ nhận thức
Cộng
Nhận biết Thông hiểu Vận dụng
Vận dụng
cao
TN TL TN TL TN TL TN TL
1. Oxi-
không khí
Biết được những
chất dùng để điều
chế oxi trong
phòng thí nghiệm
và thế nào là
phản ứng phân
hủy
Phân biệt được
đâu là phản
ứng có xảy ra
sự oxi hóa
Hiểu được tính
chât hóa học
để hoàn thiện
dãy phản ứng
Số câu hỏi 1 1 1 1 4
Số điểm 0,5 0,5 0,5 1,0 2,5
2. hidro-
nước
Từ công thức
của oxit, axit,
bazo, muối
học sinh hiểu
bản chất để
làm bài tập
chuyển đổi
( cho biết một
dữ kiện=> tìm
các dữ kiện
còn lại)
Số câu hỏi 1 1 1 1 4
Số điểm 0,5 0,5
0,5 2,0
3,5
3. Dung
dịch
Công thức tính
nồng độ phần
trăm
Làm bài tập
tính toán
Tính lượng
chất dư
Số câu hỏi 1 1 2/3 1/3 3

Số điểm 0,5
0,5 2.0 1 4,0
Tổ
ng
Số
câu
3 2 3 2+2/3 1/3 14
Số
điểm
Tỉ lệ
%
(1,5đ)
15%
(1,0đ)
10%
(1,5đ)
15%
(5,0đ)
50%
(1đ)
10%
10
100%

PHÒNG GD & ĐT ĐÔNG HƯNG ĐỀ KIỂM TRA HỌC KÌ II
TRƯỜNG THCS QUANG DƯƠNG NĂM HỌC 2022 – 2023
MÔN: HÓA HỌC 8
(Thời gian làm bài: 45 phút )
ĐỀ BÀI
PHẦN I: Trắc nghiệm (4,0 điểm).
Hãy khoanh tròn một trong các chữ cái trước phương án chọn đúng.
Câu 1: Những chất được dùng để điều chế oxi trong phòng thí nghiệm là:
A. KMnO4 và không khí. B. KMnO4 và H2O.
C. KClO3 và CaCO3 . D. KMnO4 và KClO3.
Câu 2: Công thức hóa học của nhôm oxit gồm nhôm (Al) và oxi (O) là
A: AlO2 B: Al3O2
C: Al2O3 D: Al3O
Câu 3: Các hợp chất sau: NaCl, HCl, NaOH, Na2O thuộc loại hợp chất nào?
A: NaCl (Axit), HCl (Muối), NaOH (Bazơ) Na2O (Oxit)
B: NaCl (Muối), HCl (Axit), NaOH (bazơ) Na2O (oxit)
C: NaCl (Muối), HCl (Axit), NaOH (Oxit) Na2O (Bazơ)
D: NaCl (Oxit), HCl (Muối), NaOH (bazơ) Na2O (Axit)
Câu 4: Dãy nào gồm các chất là axit?
A. CuO; BaO; MgO C. HCl; H2SO4; HNO3
B. NaOH; Cu(OH)2; Ba(OH)2 D. NaCl; MgSO4; CuS
Câu 5: : Điểm khác biệt trong thu khí oxi và hidro bằng cách đẩy khí là do?
A. Hidro và oxi tan rất ít trong nước C. Hidro và oxi nhẹ hơn không khí
B. Hidro nhẹ hơn còn oxi nặng hơn không khí D. Tất cả đều sai.
Câu 6: Trường hợp nào dưới đây không phải là dung dịch?
A. Cốc nước sô cô la C. Nước mắm
B. Nước khoáng D. Nước muối sinh lý
Câu 7: Tính số gam nước tạo ra khi đốt cháy hoàn toàn 4,48 lít khí hidro (đktc) trong oxi?
A.3,6 g B. 7,2g C. 1,8 g D. 14,4g
(Cho biết: H = 1, O = 16)
Câu 8: Hòa tan 10 gam muối ăn vào 40 gam nước. Nồng độ phần trăm của dung dịch thu
được là:
A. 25% B. 20% C. 2,5% D. 2%

PHẦN II: Tự Luận (6,0 điểm)
Câu 9. (1,0đ) Viết phương trình biểu diễn chuyển hóa sau:
C CO2 CaCO3 CaO Ca(OH)2
Câu 10: Có 4 bình chứa khí riêng biệt Khí O2 , H2 , N2 , CO2 . hãy nhận biết các khí trên bằng
phương pháp hóa học.
Câu 11. (3,0đ)
Cho 6,5 gam kẽm tác dụng với 100 gam dd HCl 14,6%
a, Viết phương trình phản ứng xảy ra
b, Chất nào còn dư sau phản ứng và dư bao nhiêu ?
c, Tính thể tích khí hiđro thoát ra (ở ĐKTC)
(Cho biết: H = 1, Cl = 35,5 , Zn = 64)
……………………………….Hết…………………………………………..

HƯỚNG DẪN CHẤM ĐỀ KIỂM TRA HỌC KÌ II
MÔN: HÓA HỌC 8
I.Trắc nghiệm( 4,0 điểm). Đúng mỗi ý 0,5 điểm
Câu 1 2 3 4 5 6 7 8
Đáp án D C C A B C A B
II. Tự luận( 6,0 điểm).
Câu Đáp án Điểm
Câu 9
(1,0đ)
1. C+ O
2
CO
2
2. CaO + CO
2
CaCO
3
3. CaCO
3
CaO + CO
2
\
4. CaO + H
2
O
Ca(OH)
2
Mỗi ý
đúng
được
0,25
điểm
Câu 10
(2,0đ)
Dẫn khí lần lượt các khí ra đầu ống dẫn khí sau đó đưa tàn đóm đỏ vào các
đầu ống dẫn khí
- Khí ở lọ nào thoát ra làm que đóm bùng cháy là lọ chứa khí O
2
PTPƯ: O
2
+ C CO
2
Ba khí còn lại không làm cho tàn đóm đỏ bùng cháy đó là khí H
2
, N
2
,
CO
2
.
Ta tiếp tục đưa que đóm đang cháy vào hai đầu ống dẫn khí, khí nào cháy
trong không khí đó là khí H
2
PTPƯ : 2H
2
+ O
2
2H
2
0
- Khí còn lại là CO
2
và N
2
ta tiếp tục dẫn hai khó đó nội qua nước
vôi trong , khí nào làm cho nước vôi trong vẩn đục là khí CO
2
. Khí
còn lại là N
2
0,25đ
0,5đ
0,25đ
0,5đ
0,5đ
Câu 11
(3,0đ)
a. PTHH
Zn + 2HCl
ZnCl
2
+ H
2
b. HS tính được:
n
Zn
= 0,1 mol
n
HCl
= 0,4 mol
so sánh số mol của Zn và HCl-> HCl dư
n
HCl dư
= 0,2 mol => m
HCl dư
= 0,2. 36,5 = 7,3 (g)
c. Tính được:
n
H
2
= 0,1 mol => V
H
2
= n.22,4= 0,1. 22,4= 2,24 (l)
0,5 đ
1,5 đ
1 đ












![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



