§Þnh tÝnh anion nhãm I: Cl-, Br-, I-, SCN-, S2O32-
Môc tiªu
1. X¸c ®Þnh ®−îc tõng anion nhãm I dùa vµo c¸c ph¶n øng ®Æc tr−ng cña chóng.
2. Gi¶i thÝch c¸c hiÖn t−îng x¶y ra vµ viÕt c¸c ph−¬ng tr×nh ph¶n øng trong qu¸
tr×nh tiÕn hµnh thùc nghiÖm.
1. Dông cô - hãa chÊt - Thuèc thö
Hãa chÊt, thuèc thö
- Dung dÞch ph©n tÝch
chøa c¸c anion: Cl-, Br-, I-, SCN-, S2O32-
Dông cô
- §Ìn cån
- §òa thñy tinh
- KÑp gç
- èng nghiÖm ly t©m
- èng nghiÖm c¸c lo¹i
- M¸y ly t©m
- HNO3 2 N
- H2SO4 2 N
- NaOH ®Æc
- Na2CO3 b·o hßa
- AgNO3 0,1N
- (NH4)2CO3 b·o hßaà
- FeCl3 10%
- NaNO2 0,1 N
- Zn h¹t
- Hå tinh bét
- N−íc Javel
- Cloroform
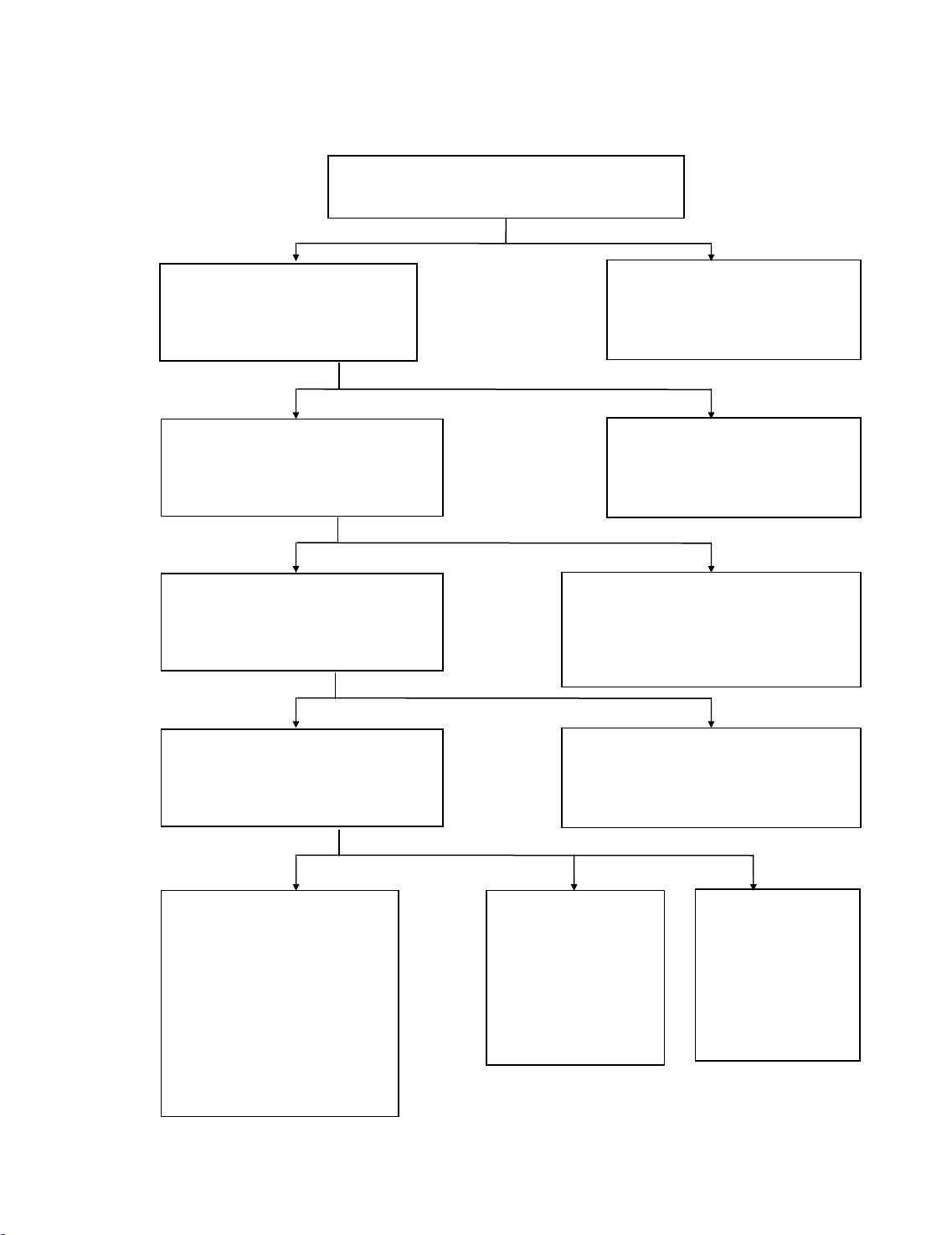
2. Thùc hµnh
2.1. LÊy 2 mL dung dÞch ph©n tÝch lµm n−íc soda (b»ng c¸ch cho thªm 2
mL Na2CO3 b·o hßa + 2-3 giät NaOH ®Æc). NÕu cã tña th× ly t©m, bá tña
(nÕu kh«ng cã tña th× ngay tõ ®Çu kh«ng cÇn lµm n−íc soda).
−
Thªm vµo n−íc ly t©m (n−íc soda) HNO3 2N vµ AgNO3 0,1N ®Õn kÕt
tña hoµn toµn anion nhãm I.
−
NÕu thÊy kÕt tña tõ mµu n©u chuyÓn thµnh mµu ®en lµ cã S2O32- trong
dung dÞch ph©n tÝch ban ®Çu
−
Ly t©m, lÊy kÕt tña vµ chia lµm 2 phÇn: phÇn nhá tña vµ phÇn lín tña
120