Giới thiệu tài liệu
Chương 2 của tài liệu này trình bày một cách tổng quan về cấu tạo phân tử và các loại liên kết hóa học cơ bản. Nội dung bao gồm khái niệm về độ âm điện của nguyên tố, các loại liên kết hóa học theo quan niệm cổ điển, tính chất của phân tử, và liên kết hóa học dưới góc độ cơ học lượng tử.
Đối tượng sử dụng
Tài liệu này phù hợp cho sinh viên, giảng viên và các nhà nghiên cứu trong lĩnh vực hóa học, vật lý và các ngành khoa học tự nhiên có liên quan, những người muốn tìm hiểu sâu về cấu trúc phân tử, các loại liên kết hóa học và các lý thuyết nền tảng trong hóa học đại cương.
Nội dung tóm tắt
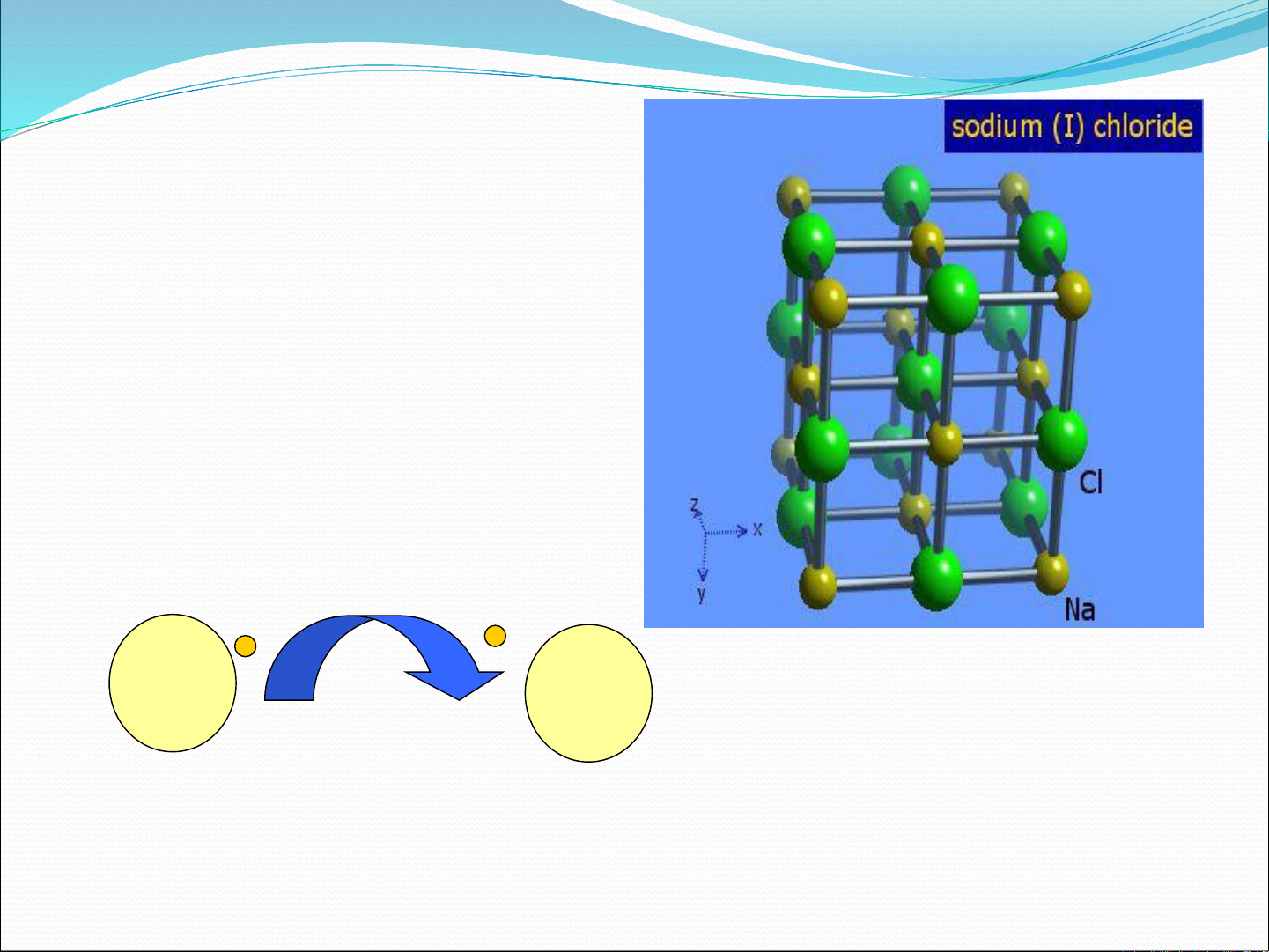
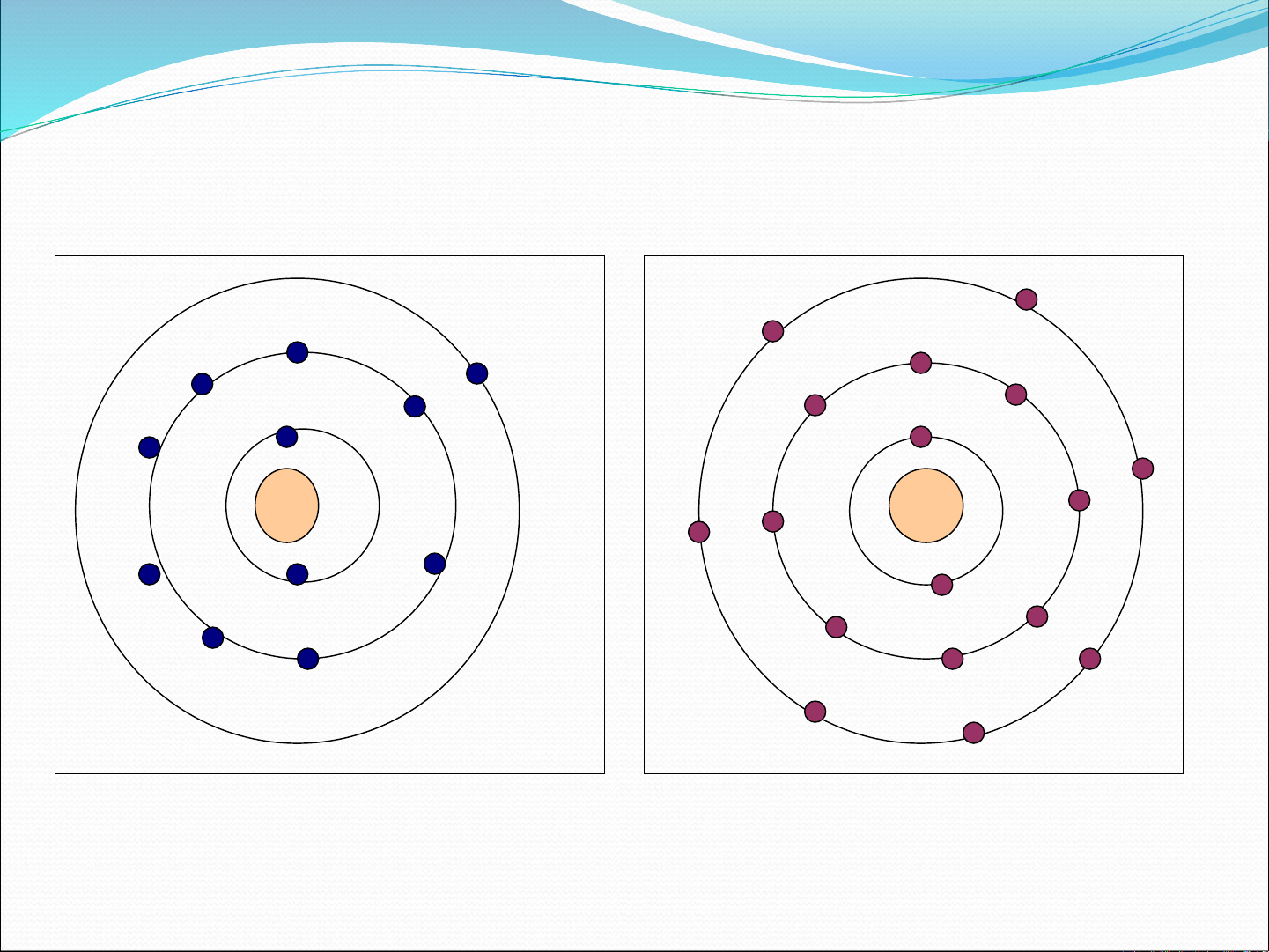
Chương 2 đi sâu vào cấu tạo phân tử và các loại liên kết hóa học, bắt đầu với khái niệm độ âm điện của nguyên tố, được định nghĩa là khả năng hút điện tử về phía mình và được ký hiệu là χ, tính bằng tổng năng lượng ion hóa và ái lực electron. Tiếp theo, chương trình bày chi tiết các loại liên kết theo quan niệm cổ điển. Liên kết ion được giải thích dựa trên thuyết tĩnh điện của Kossel, hình thành do sự chuyển electron hóa trị tạo thành các ion trái dấu hút nhau. Các ví dụ minh họa cơ chế hình thành liên kết ion như NaCl được đưa ra, cùng với mối quan hệ giữa độ chênh lệch độ âm điện và tính ion của hợp chất. Các tính chất đặc trưng của liên kết ion như tính không bão hòa và không định hướng cũng được đề cập, cùng với công thức tính năng lượng liên kết ion bao gồm năng lượng hút và năng lượng đẩy. Liên kết cộng hóa trị được trình bày theo quan niệm của Lewis, là loại liên kết hình thành do sự góp chung electron hóa trị tạo thành các cặp electron chung, tuân theo quy tắc bát tử. Các khái niệm về electron không liên kết, liên kết đơn, đôi, ba và bậc liên kết được giải thích. Tính chất có hướng và độ phân cực của liên kết cộng hóa trị cũng được làm rõ. Ngoài ra, chương còn giới thiệu liên kết cho nhận, một trường hợp đặc biệt của liên kết cộng hóa trị, nơi một nguyên tử đóng góp cả hai electron cho cặp chung. Cuối cùng, liên kết kim loại được định nghĩa là liên kết giữa các nguyên tử kim loại trong trạng thái tinh thể hoặc lỏng, hình thành do lực hút giữa các ion dương kim loại và các electron hóa trị tự do, giải thích khả năng dẫn điện của kim loại. Chương cũng đề cập đến tính chất của phân tử và liên kết hóa học theo quan niệm cơ học lượng tử, mặc dù chi tiết không được hiển thị trong đoạn trích.




![Bài giảng Hoá học đại cương Trường Đại học Nam Cần Thơ [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260310/hoaphuong0906/135x160/53091773287379.jpg)




















![Tập bài giảng Hoá học đại cương 1 - Đăng Thị Thu Huyền [Full, Chi Tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260312/hoabattu2026/135x160/11351773633935.jpg)



