
Tóm t t lý thuy t hoá h c 12ắ ế ọ
Ch ng 1: ESTE - LIPTươ
A-ESTE.
I – KHÁI NI M, DANH PHÁPỆ
C
2
H
5
OH + CH
3
COOH CH
3
COOC
2
H
5
+ H
2
O
H
2
SO
4
ñaëc, t
0
etyl axetat
CH
3
COOH + HO [CH
2
]
2
CH
CH
3
CH
3
CH
3
COO [CH
3
]
2
CH
CH
3
CH
3
+ H
2
O
H
2
SO
4
ñaëc, t
0
isoamyl axetat
T ng quát:ổ
RCOOH + R'OH RCOOR' + H
2
O
H
2
SO
4
ñaëc, t
0
Khi thay th nhóm OH nhóm cacboxyl c a axit cacboxylic b ng nhóm OR’ thì đ c este.ế ở ủ ằ ượ
CTCT c a este đ n ch c: RCOOR’ủ ơ ứ
R: g c hiđrocacbon c a axit ho c H.ố ủ ặ
R’: g c hiđrocacbon c a ancol (R # H)ố ủ
CTCT chung c a este no đ n ch c:ủ ơ ứ
- CnH2n+1COOCmH2m+1 (n ≥ 0, m ≥ 1)
- CxH2xO2 (x ≥ 2)
Tên g i: Tên g c hiđrocacbon c a ancol + tên g c axit.ọ ố ủ ố
- Tên g c axit: Xu t phát t tên c a axit t ng ng, thay đuôi ic→at. ố ấ ừ ủ ươ ứ
Thí d :ụ
CH3COOCH2CH2CH3: propyl axetat
HCOOCH3: metyl fomat
II – TÍNH CH T V T LÍẤ Ậ
- Các este là ch t l ng ho c ch t r n trong đi u ki n th ng, h u nh không tan trong n c.ấ ỏ ặ ấ ắ ề ệ ườ ầ ư ướ
- Có nhi t đ sôi th p h n h n so v i các axit đ ng phân ho c các ancol có cùng kh i l ngệ ộ ấ ơ ẳ ớ ồ ặ ố ượ
mol phân t ho c có cùng s nguyên t cacbon.ử ặ ố ử
Thí d :ụ
CH3CH2CH2C
OOH
(M = 88)
0
s
t
=163,50C
Tan nhi uề
trong n cướ
CH3[CH2]3C
H2OH
(M = 88),
0
s
t
=
1320C
Tan ít trong
n cướ
CH3COOC2H
5
(M = 88),
0
s
t
= 770C
Không tan
trong n cướ
Nguyên nhân: Do gi a các phân t este không t o đ c liên k t hiđro v i nhau và liên k tữ ử ạ ượ ế ớ ế
hiđro gi a các phân t este v i n c r t kém.ữ ử ớ ướ ấ
- Các este th ng có mùi đ c tr ng: isoamyl axetat có mùi chu i chín, etyl butirat và etylườ ặ ư ố
propionat có mùi d a; geranyl axetat có mùi hoa h ng…ứ ồ
III. TÍNH CH T HOÁ H CẤ Ọ
1. Thu phân trong môi tr ng axitỷ ườ
Tr ng THPT S 1 Nghĩa Hành Tháng 05/ 2010ườ ố
Giáo viên Chu Anh Tu n Trang ấ1

Tóm t t lý thuy t hoá h c 12ắ ế ọ
C
2
H
5
OH + CH
3
COOHCH
3
COOC
2
H
5
+ H
2
O
H
2
SO
4
ñaëc, t
0
* Đ c đi m c a ph n ng: ặ ể ủ ả ứ Thu n ngh ch và x y ra ch m.ậ ị ả ậ
2. Thu phân trong môi tr ng baz (Ph n ng xà phòng hoá)ỷ ườ ơ ả ứ
CH
3
COOC
2
H
5
+ NaOH CH
3
COONa + C
2
H
5
OH
t
0
•Đ c đi m c a ph n ng: ặ ể ủ ả ứ Ph n ng ch x y ra 1 chi u.ả ứ ỉ ả ề
IV. ĐI U CHỀ Ế
1. Ph ng pháp chungươ : B ng ph n ng este hoá gi a axit cacboxylic và ancol.ằ ả ứ ữ
RCOOH + R'OH RCOOR' + H
2
O
H
2
SO
4
ñaëc, t
0
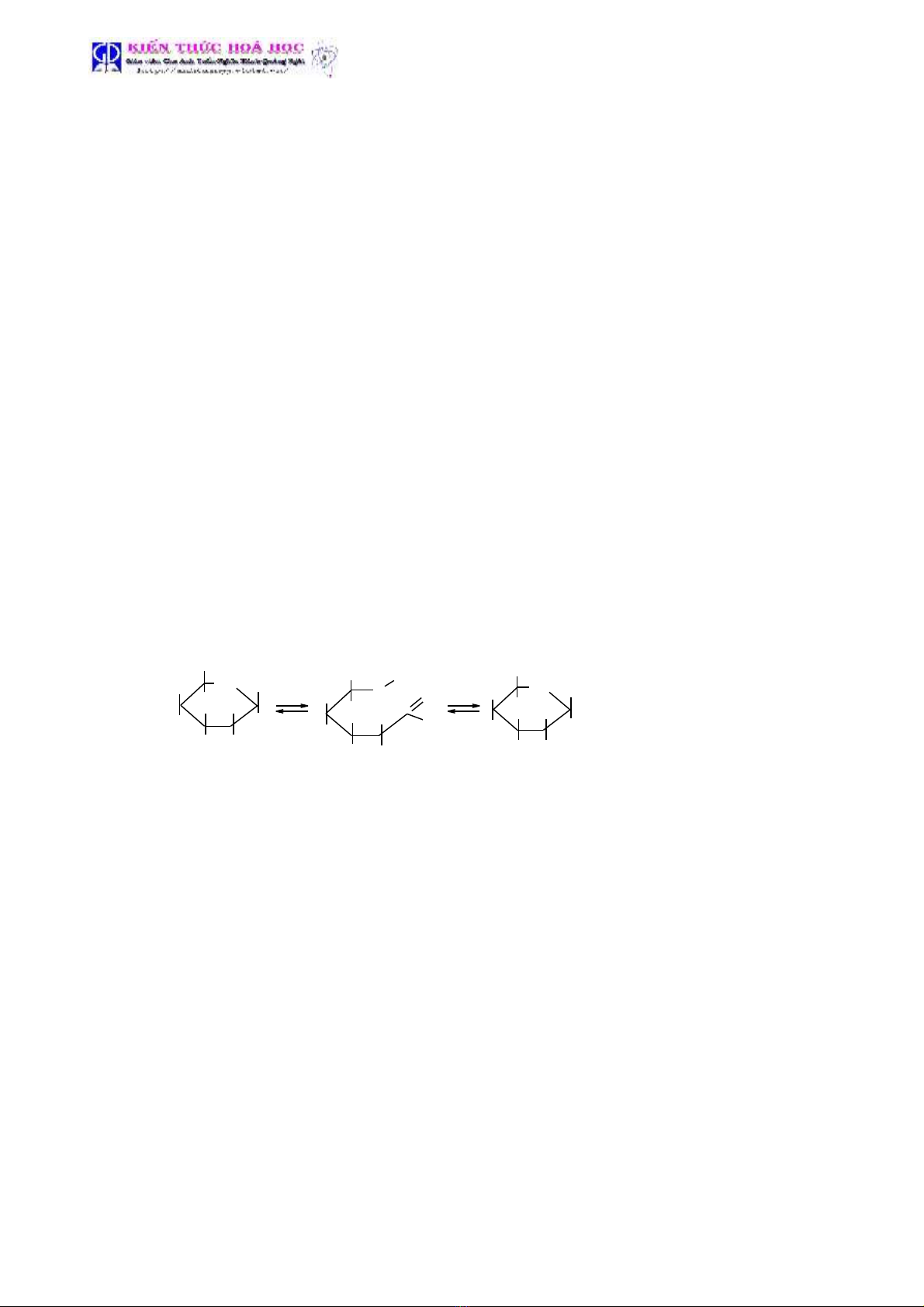
2. Ph ng pháp riêng:ươ Đi u ch este c a anol không b n b ng ph n ng gi a axitề ế ủ ề ằ ả ứ ữ
cacboxylic và ancol t ng ng.ươ ứ
CH
3
COOH +CH CH CH
3
COOCH=CH
2
t
0
, xt
V. NG D NGỨ Ụ
- Dùng làm dung môi đ tách, chi t ch t h u c (etyl axetat), pha s n (buể ế ấ ữ ơ ơ tyl axetat),...
- M t s polime c a este đ c dùng đ s n xu t ch t d o nh poli(vinyl axetat), poli (metylộ ố ủ ượ ể ả ấ ấ ẻ ư
metacrylat),.. ho c dùng làm keo dán.ặ
- M t s este có mùi th m, không đ c, đ c dùng làm ch t t o h ng trong công nghi pộ ố ơ ộ ượ ấ ạ ươ ệ
th c ph m (benzyl fomat, etyl fomat,..), mĩ ph m (linalyl axetat, geranyl axetat,…),…ự ẩ ẩ
B-LIPIT.
I – KHÁI NI M Ệ
Lipit là nh ng h p ch t h u c có trong t bào s ng, không hoà tan trong n c nh ng tanữ ợ ấ ữ ơ ế ố ướ ư
nhi u trong các dung môi h u c không c c.ề ữ ơ ự
•C u t o:ấ ạ Ph n l n lipit là các este ph c t p, bao g m ch t béo (triglixerit), sáp, steroitầ ớ ứ ạ ồ ấ
và photpholipit,…
II – CH T BÉOẤ
1. Khái ni mệ
Ch t béo là trieste c a glixerol v i axit béo, g i chung là triglixerit hay là triaxylglixerol.ấ ủ ớ ọ
Các axit béo hay g p:ặ
C17H35COOH hay CH3[CH2]16COOH: axit stearic
C17H33COOH hay cis-CH3[CH2]7CH=CH[CH2]7COOH: axit oleic
C15H31COOH hay CH3[CH2]14COOH: axit panmitic
Axit béo là nh ng axit đ n ch c có m ch cacbon dài, không phân nhánh, có th no ho cữ ơ ứ ạ ể ặ
không no.
CTCT chung c a ch t béo:ủ ấ
R
1
COO CH
2
CH
CH
2
R
2
COO
R
3
COO
R1, R2, R3 là g c hiđrocacbon c a axit béo, có th gi ng ho c khác nhau.ố ủ ể ố ặ
Thí d :ụ
(C17H35COO)3C3H5: tristearoylglixerol (tristearin)
(C17H33COO)3C3H5: trioleoylglixerol (triolein)
Tr ng THPT S 1 Nghĩa Hành Tháng 05/ 2010ườ ố
Giáo viên Chu Anh Tu n Trang ấ2

Tóm t t lý thuy t hoá h c 12ắ ế ọ
(C15H31COO)3C3H5: tripanmitoylglixerol (tripanmitin)
2. Tính ch t v tấ ậ lí
đi u ki n th ng: Là ch t l ng ho c ch t r n.Ở ề ệ ườ ấ ỏ ặ ấ ắ
- R1, R2, R3: Ch y u là g c hiđrocacbon no thì ch t béo là ch t r n.ủ ế ố ấ ấ ắ
- R1, R2, R3: Ch y u là g c hiđrocacbon không no thì ch t béo là ch t l ng.ủ ế ố ấ ấ ỏ
Không tan trong n c nh ng tan nhi u trong các dung môi h u c không c c: benzen,ướ ư ề ữ ơ ự
clorofom,…
Nh h n n c, không tan trong n c.ẹ ơ ướ ướ
3. Tính ch t hoá h c ấ ọ
a. Ph n ng thu phânả ứ ỷ
(CH
3
[CH
2
]
16
COO)
3
C
3
H
5
+ 3H
2
O 3CH
3
[CH
2
]
16
COOH + C
3
H
5
(OH)
3
H
+
, t
0
tristearin axit stearic glixerol
b. Ph n ng xà phòng hoáả ứ
(CH
3
[CH
2
]
16
COO)
3
C
3
H
5
+ 3NaOH 3CH
3
[CH
2
]
16
COONa + C
3
H
5
(OH)
3
t
0
tristearin natri stearat glixerol
c. Ph n ng c ng hiđro c a ch t béo l ngả ứ ộ ủ ấ ỏ
(C
17
H
33
COO)
3
C
3
H
5
+ 3H
2
(C
17
H
35
COO)
3
C
3
H
5
(loûng) (raén)
Ni
175 - 190
0
C
4. ng d ngỨ ụ
- Th c ăn cho ng i, là ngu n dinh d ng quan tr ng và cung c p ph n l n năng l ng choứ ườ ồ ưỡ ọ ấ ầ ớ ượ
c th ho t đ ng.ơ ể ạ ộ
- Là nguyên li u đ t ng h p m t s ch t khác c n thi t cho c th . B o đ m s v nệ ể ổ ợ ộ ố ấ ầ ế ơ ể ả ả ự ậ
chuy n và h p th đ c các ch t hoà tan đ c trong ch t béo.ể ấ ụ ượ ấ ượ ấ
- Trong công nghi p, m t l ng l n ch t béo dùng đ s n xu t xà phòng và glixerol. S nệ ộ ượ ớ ấ ể ả ấ ả
xu t m t s th c ph m khác nh mì s i, đ h p,…ấ ộ ố ự ẩ ư ợ ồ ộ
C-KHÁI NI M V XÀ PHÒNG VÀ CH T GI T R A T NG H PỆ Ề Ấ Ặ Ử Ổ Ợ
I – XÀ PHÒNG
1. Khái ni mệ
Xà phòng th ng dùng là h n h p mu i natri ho c mu i kali c a axit béo, có thêm m t sườ ỗ ợ ố ặ ố ủ ộ ố
ch t ph gia.ấ ụ
Thành ph n ch y u c a xà phòng th ng: Là mu i natri c a axit panmitic ho c axitầ ủ ế ủ ườ ố ủ ặ
stearic. Ngoài ra trong xà phòng còn có ch t đ n (làm tăng đ c ng đ đúc bánh), ch t t yấ ộ ộ ứ ể ấ ẩ
màu, ch t di t khu n và ch t t o h ng,…ấ ệ ẩ ấ ạ ươ
2. Ph ng pháp s n xu t ươ ả ấ
(RCOO)
3
C
3
H
5
+ 3NaOH 3RCOONa + C
3
H
5
(OH)
3
t
0
chaát beùo xaø phoøng
Xà phòng còn đ c s n xu t theo s đ sau:ượ ả ấ ơ ồ
Ankan axit cacboxylic muoái natri cuûa axit cacboxylic
Thí d :ụ
2CH
3
[CH
2
]
14
CH
2
CH
2
[CH
2
]
14
CH
3
4CH
3
[CH
2
]
14
COOH
O
2
, t
0
, xt
2CH
3
[CH
2
]
14
COOH + Na
2
CO
3
2CH
3
[CH
2
]
14
COONa + CO
2
+ H
2
O
Tr ng THPT S 1 Nghĩa Hành Tháng 05/ 2010ườ ố
Giáo viên Chu Anh Tu n Trang ấ3

Tóm t t lý thuy t hoá h c 12ắ ế ọ
II – CH T GI T R A T NG H PẤ Ặ Ử Ổ Ợ
1. Khái ni mệ
Nh ng h p ch t không ph i là mu i natri c a axit cacboxylic nh ng có tính năng gi t r aữ ợ ấ ả ố ủ ư ặ ử
nh xà phòng đ c g i là ch t gi t r a t ng h p.ư ượ ọ ấ ặ ử ổ ợ
2. Ph ng pháp s n xu t ươ ả ấ
Đ c t ng h p t các ch t l y t d u m .ượ ổ ợ ừ ấ ấ ừ ầ ỏ
Daàu moû axit ñoñexylbenzensunfonic natri ñoñexylbenzensunfonat
C
12
H
25
-C
6
H
4
SO
3
H C
12
H
25
-C
6
H
4
SO
3
Na
Na
2
CO
3
axit ñoñexylbenzensunfonic natri ñoñexylbenzensunfonat
3. TÁC D NG T Y R A C A XÀ PHÒNG VÀ CH T GI T R A T NG H PỤ Ẩ Ử Ủ Ấ Ặ Ử Ổ Ợ
- Mu i natri trong xà phòng hay trong ch t gi t r a t ng h p có kh năng làm gi m s c căngố ấ ặ ử ổ ợ ả ả ứ
b m t c a các ch t b n bám trên v i, da,… do đó v b n đ c phân tán thành nhi u ph nề ặ ủ ấ ẩ ả ế ẩ ượ ề ầ
nh h n và đ c phân tán vào n c.ỏ ơ ượ ướ
- Các mu i panmitat hay stearat c a các kim lo i hoá tr II th ng khó tan trong n c, do đóố ủ ạ ị ườ ướ
không nên dùng xà phòng đ gi t r a trong n c c ng (n c có ch a nhi u ion Caể ặ ử ướ ứ ướ ứ ề 2+, Mg2+).
Các mu i c a axit đođexylbenzensunfonic l i tan đ c trong n c c ng, do đó ch t gi t r aố ủ ạ ượ ướ ứ ấ ặ ử
có u đi m h n xà phòng là có th gi t r a c trong n c c ng.ư ể ơ ể ặ ử ả ướ ứ
Tr ng THPT S 1 Nghĩa Hành Tháng 05/ 2010ườ ố
Giáo viên Chu Anh Tu n Trang ấ4
Tóm t t lý thuy t hoá h c 12ắ ế ọ
Ch ng 2 : CACBONHIĐRATươ
A. KHÁI NI M V CACBONHIĐRATỆ Ề
Cacbonhiđrat là nh ng h p ch t h u c t p ch c, có ch a nhi u nhóm hyđroxyl (-ữ ợ ấ ữ ơ ạ ứ ứ ề
OH) và có nhóm cacbonyl ( -CO- ) trong phân t , th ng có công th c chung là Cử ườ ứ n(H2O)m.
B. MONOSACCARIT
Monosaccarit là nh ng cacbonhiđrat đ n gi n nh t không b thu phân.ữ ơ ả ấ ị ỷ
Ví d : Glucoz và fructoz có công th c phân t Cụ ơ ơ ứ ử 6H12O6.
* GLUCOZ .Ơ
I. Tính ch t v t lí và tr ng thái thiên nhiên: ấ ậ ạ
Ch t r n k t tinh, không màu, nóng ch y nhi t đ 146ấ ắ ế ả ở ệ ộ oC và có đ ng t kém đ ngộ ọ ườ
mía, có nhi u trong các b ph n c a cây và nh t là trong qu chín. Glucoz có trong c thề ộ ậ ủ ấ ả ơ ơ ể
ng i và đ ng v t (chi m 0,1% trong máu ng i).ườ ộ ậ ế ườ
II. C u trúc phân t .ấ ử
Glucoz có công th c phân t là Cơ ứ ử 6H12O6, t n t i d ng m ch h và m ch vòng.ồ ạ ở ạ ạ ở ạ
1. D ng m ch h .ạ ạ ở
Glucoz có c u t o c a anđehit đ n ch c và ancol 5 ch c, có công th c c u t o thu g n là ơ ấ ạ ủ ơ ứ ứ ứ ấ ạ ọ
CH2OH-CHOH-CHOH-CHOH-CHOH-CH=O Ho c vi t g n: CHặ ế ọ 2OH[CHOH]4CHO
2. D ng m ch vòng.ạ ạ
-Nhóm-OH ë C5 céng vµo nhãm C=O t¹o ra 2 d¹ng vßng 6 c¹nh α vµ β.
-Trong dung d ch, hai d ng này chi m u th h n và luôn chuy n hoá l n nhau theoị ạ ế ư ế ơ ể ẫ
m t cân b ng qua d ng m ch h . ộ ằ ạ ạ ở
CH OH
2
H
H
H
H
H
HO
OH
OH
OH
CH OH
2
H
H
H
H
HO
OH
OH
O
C
1
2
3
4
5
6
1
2
3
4
5
6
CH OH
2
H
H
HH
H
HO
OH
OH
OH
1
2
3
4
5
6
α-Glucoz Glucoz ơ ơ β-Glucozơ
- Nhóm OH v trí s 1 đ c g i là OH hemiaxetalở ị ố ượ ọ
III. Tính ch t hoá h c.ấ ọ
Glucoz có các tính ch t c a nhóm anđehit và ancol đa ch c.ơ ấ ủ ứ
1. Tính ch t c a ancol đa ch c (poliancol)ấ ủ ứ
a. Tác d ng v i Cu(OH)ụ ớ 2:
dd glucozo hoà tan Cu(OH)2 tở0 th ng t o dd ph c có màu xanhườ ạ ứ
2C6H12O6 + Cu(OH)2→(C6H11O6)2Cu + 2H2O
b. Ph n ng t o esteả ứ ạ
Khi Glucoz tác d ng v i anhidrit axetic có th t o ra este ch a 5 g cơ ụ ớ ể ạ ứ ố
axit :C6H7O(OCOCH3)5
2. Tính ch t c a nhóm anđehitấ ủ
a. Tính kh . ử
- Oxi hóa Glucoz b ng ph c b c amoniac (AgNOơ ằ ứ ạ 3 trong dung d ch NHị3)
AgNO3+ 3NH3+H2O→[Ag(NH3)2]OH+ NH4NO3
CH2OH[CHOH]4CHO+2[Ag(NH3)2]OH→CH2OH[CHOH]4COONH4+ 2Ag+3NH3+ H2O.
Tr ng THPT S 1 Nghĩa Hành Tháng 05/ 2010ườ ố
Giáo viên Chu Anh Tu n Trang ấ5
OO
O
H


![Lý thuyết và bài tập Hóa học lớp 12 năm 2022 (KHXH) - Trường THPT Đào Sơn Tây [Tổng hợp]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230310/phuogchi205/135x160/2351678432530.jpg)

![Lý thuyết và bài tập Hóa học lớp 12 (KHTN) năm 2021 - Trường THPT Đào Sơn Tây [Đầy đủ]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230310/phuogchi205/135x160/491678432840.jpg)





















