
TẠP CHÍ Y HỌC VIỆT NAM TẬP 490 - THÁNG 5 - SỐ 1 - 2020
29
các thử nghiệm hành vi của chuột. Hoạt tính AChE
ở nhóm sử dụng cao chiết alcaloid Thạch tùng đuôi
ngựa thấp hơn nhóm tiêm scopolamin với sự khác
biệt có ý nghĩa thống kê ở liều 150mg/kg. Kết quả
này cũng phù hợp với kết quả trong các thử
nghiệm hành vi.
IV. KẾT LUẬN
Cao chiết alcaloid của cây Thạch tùng đuôi
ngựa liều 150mg/kg thể hiện tác dụng cải thiện
trí nhớ làm việc trên mô hình mê lộ chữ Y, cải
thiện trí nhớ không gian dài hạn trên mô hình
mê lộ nước Morris và có tác dụng ức chế hoạt
tính của AChE ex-vivoở hồi hải mã trên động vật
thực nghiệm gây suy giảm trí nhớ bằng
scopolamin. Các kết quả nghiên cứu cho thấy
cây Thạch tùng đuôi ngựa có thể là dược liệu
tiềm năng điều trị các triệu chứng sa sút trí tuệ
trong bệnh Alzheimer’s.
TÀI LIỆU THAM KHẢO
1. Burns A., Iliffe S. (2009), “Alzheimer's disease”,
British Medical Journal, 338, pp. 467 – 471.
2. Konrath E.L., Neves B.M., Passos C.S.,
Lunardi P.S., Ortega M.G., Cabrera J.L.,
Goncalves C.A., Henriques A.T. (2012),
"Huperzia quadrifariata and Huperzia reflexa
alkaloids inhibit acetylcholinesterase activity in vivo
in mice brain", Phytomedicine, 19, pp. 1321- 1324.
3. Ellman G.L., Courtney K. D., Valentinoandress
J.R., and Featherstone R.M. (1961), "A new and rapid
colorimetric determination of acetylcholinesterase
activity", Biochemical Pharmacology, 7, pp. 88-95.
4. Wolf A., Bauer B., Abner E.L., Ashkenazy-
Frolinger T., Hartz A.M. (2016), "A
Comprehensive Behavioral Test Battery to Assess
Learning and Memory in 129S6/Tg2576 Mice", PloS
one, Vol. 11 (1), pp. 1-23.
5. Harada K. et al (2012), "A novel glycine
transporter-1 (GlyT1) inhibitor, ASP2535 (4-[3-
isopropyl-5-(6-phenyl-3-pyridyl)-4H-1,2,4-triazol-4-
yl]-2,1,3-benzoxadiazole), improves cognition in
animal models of cognitive impairment in
schizophrenia and Alzheimer's disease", European
Journal of Pharmacology, 685(1-3), pp.59-69.
6. Bromley-Brits K., Deng Y., Song W. (2011),
"Morris Water Maze Test for Learning and Memory
Deficits in Alzheimer’s Disease Model Mice", Journal
of Visualized Experiments, 53, pp. 1-5.
7. Vorhees C.V., Williams M.T. (2014), "Assessing
Spatial Learning and Memory in Rodents", Laboratory
Animal Research Journal, 55 (2), pp. 310-332.
8. Hasselmo M.E. (2006), "The Role of
Acetylcholine in Learning and Memory", Current
Opinion in Neurobiology, 16 (6), pp. 710-715.
ĐÁNH GIÁ KẾT QUẢ ĐIỀU TRỊ UNG THƯ VÒM MŨI HỌNG GIAI ĐOẠN
DI CĂN HẠCH N1-N3, M0 TẠI BỆNH VIỆN QUÂN Y 103
Phạm Khánh Hưng*, Trần Đình Thiết*, Nguyễn Ngọc Sáng*
Phạm Đình Phúc*, Nguyễn Văn Ba*
TÓM TẮT8
Mục tiêu: Đánh giá kết quả hóa xạ trị đồng thời ở
bệnh nhân ung thư vòm mũi họng giai đoạn di căn
hạch N1-N3M0. Đối tượng và phương pháp: 62
bệnh nhân (48 nam, 14 nữ) UTVMH giai đoạn di căn
hạch N1-N3, M0 điều trị tại Trung tâm Ung bướu-
Bệnh viện quân y 103 từ tháng 01/2015 đến tháng
06/2019 bằng phác đồ hóa xạ trị đồng thời Cisplatin
100 mg/m2 (N1, N22, N43), hóa trị bổ trợ 3 chu kỳ
phác đồ Cisplatin – 5FU. Kết quả và kết luận: Tỷ lệ
đáp ứng tại u: đáp ứng hoàn toàn 60/62 (96,8%), đáp
ứng một phần 2/62 (3,2%). Tỷ lệ đáp ứng hoàn toàn
tại hạch 58/62 (93,5%), đáp ứng một phần
4/62(6,5%). Tỷ lệ đáp ứng chung: đáp ứng hoàn toàn
58/62 (93,5%), đáp ứng một phần 4/62 (6,5%). Có
51 bệnh nhân được theo dõi từ 3 năm trở lên. Tỉ lệ
sống thêm toàn bộ sau 3 năm là 46/51 (90,2%). Độc
*Bệnh viện 103, Học viện Quân y
Chịu trách nhiệm chính: Nguyễn Văn Ba
Email: bsnguyenvanba@yahoo.com
Ngày nhận bài: 9/2/2020
Ngày phản biện khoa học: 3/3/2020
Ngày duyệt bài: 16/3/2020
tính đối với hệ tạo huyết đa phần là độ 1, độ 2; có
6,5% giảm bạch cầu độ 3; 4,8% giảm bạch cầu độ 4.
Độc tính trên gan thận ít gặp và là độ 1. Viêm niêm
mạc chiếm tỷ lệ 100%, độ 3 chiếm 24,2%.
Từ khóa:
Hóa xạ trị đồng thời, hóa chất bổ trợ
SUMMARY
THE TREATMENT RESULT OF THE
NASOPHARYNGEAL CANCER STAGE N1-
N3M0 AT 103 MILITARY HOSPITAL
Objectives: Evaluating the results of concurrent
chemoradiotherapy in nasopharygeal cancer stage N1-
N3M0. Methods: 62 patients (48 males, 14 females)
with lympho node metastasis nasopharynxgeal cancer
in the stage N1-N3M0 treated at Center of Oncology -
103 military hospital from 01/2015 to 06/2019 with
concurrent chemoradiotherapy with Cisplatin 100
mg/m2 (N1, N22, N43), followed by 3 cycles of
adjuvant chemotherapy with CF. Results and
conclusion: Tumor response rate: complete response
rate was 60/62 (96.8%), partial response rate was
2/62 (3.2%). Lympho node response rate: complete
response rate was 58/62 (93.5%), partial response
rate was 4/62 (6.5%). Overall response rate: complete
response rate was 58/62 (93.5%), partial response

vietnam medical journal n01 - MAY - 2020
30
rate was 4/62 (6.5%). 51/62 patients were followed
up for 3 years or more. Overall survival rate after 3
years was 46/51 (90.2%). Hematopoietic toxicity
occurred at grade 1. There were 6.5% for grade 3 and
4.8% for grade 4 leukopenia. Hepatorenal toxicity was
rare and mainly at grade 1. Mucositist cocurred in
100% patients, 24,2% at grade 3.
Key words:
Concurrent chemoradiotherapy,
adjuvant chemotherapy.
I. ĐẶT VẤN ĐỀ
Ung thư biểu mô vòm mũi họng (UTVMH) là
một bệnh lý ác tính của tế bào biểu mô phủ
vùng vòm họng. Đây là ung thư thường gặp nhất
trong ung thư vùng đầu cổ. UTVMH là một trong
những ung thư phổ biến ở Việt Nam và một số
nước vùng Nam Á như Trung Quốc, Hồng Kông,
Đài Loan, Singapore… Theo Globocan 2018, tại
Việt Nam, UTVMH đứng hàng thứ 4 ở nam giới
với tỷ lệ mắc chuẩn theo tuổi là 9,0/100.000 dân
và đứng hàng thứ 9 ở nữ giới với tỷ lệ mắc
chuẩn theo tuổi là 2,8/100.000 dân [1].
Nhờ các tiến bộ trong chẩn đoán, quản lý cũng
như điều trị bệnh, đặc biệt là sự ra đời và phát
triển của hệ thống máy xạ trị gia tốc tuyến tính
với những kỹ thuật xạ trị 3D- CRT, IMRT, VMAT...
tiên lượng chung của UTVMH đã được cải thiện
rõ rệt. UTVMH đa phần là loại ung thư biểu mô
không biệt hóa đáp ứng tốt với cả hóa trị và xạ
trị. Vì vậy, những năm gần đây đã có nhiều thử
nghiệm lâm sàng tiến hành hóa xạ trị đồng thời
làm tăng tỉ lệ kiểm soát tại chỗ, giảm tỉ lệ tái phát
di căn xa và làm tăng tỉ lệ sống thêm toàn bộ,
sống thêm không bệnh một cách có ý nghĩa so
với xạ trị đơn thuần [2], từ đó xu hướng hóa xạ trị
đồng thời cho UTVMH giai đoạn tiến xa tại chỗ, tại
vùng được xem là điều trị tiêu chuẩn.
Tại Việt Nam, ung thư biểu mô không biệt
hóa chiếm trên 90% trong các loại UTVMH. Do
đó, hiện nay hóa xạ trị đồng thời cho UTVMH
giai đoạn tại chỗ, tại vùng với tác nhân hóa chất
là Cisplatin chu kỳ hàng tuần hoặc 03 tuần kết
hợp với xạ trị, theo sau có bổ trợ phác đồ CF 03
chu kỳ được xem là điều trị phổ biến. Từ năm
2014, khi được trang bị hệ thống máy gia tốc
tuyến tính đa lá, tại Bệnh viện quân y 103 đã áp
dụng phác đồ hóa xạ trị đồng thời cho UTVMH
giai đoạn tại chỗ, tại vùng. Để có tổng kết đánh
giá về hiệu quả cũng như độc tính của phác đồ
hóa xạ trị đồng thời cho UTVMH giai đoạn di căn
hạch vùng, chúng tôi thực hiện đề tài “Đánh giá
kết quả điều trị ung thư vòm mũi họng giai đoạn
di căn hạch N1-N3, M0 tại Bệnh viện Quân y
103” với các mục tiêu sau:
1. Đánh giá kết quả hóa xạ trị đồng thời ở
nhóm bệnh nhân nghiên cứu.
2. Đánh giá một số tác dụng không mong
muốn của điều trị
II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Đối tượng nghiên cứu. 62 bệnh nhân
UTVMH giai đoạn di căn hạch N1-N3, M0 điều trị
hóa xạ trị đồng thời tại Trung tâm Ung bướu-
Bệnh viện quân y 103 từ tháng 01/2015 đến
tháng 06/2019.
2.1.1. Tiêu chuẩn chọn bệnh nhân
- Tuổi 18 đến 70, chỉ số toàn trạng ECOG 0,1;
- Có chẩn đoán mô bệnh học;
- Chẩn đoán UTVMH giai đoạn di căn hạch
N1-N3, M0 theo phân loại của UICC/AJCC 2010.
- Bệnh nhân được điều trị lần đầu theo phác
đồ hóa xạ trị đồng thời với Cisplatin, hóa trị bổ
trợ 3 chu kỳ phác đồ CF.
- Không có chống chỉ định điều trị hóa chất,
xạ trị.
- Các bệnh nhân đồng ý tham gia nghiên cứu
được giải thích rõ liệu trình điều trị và tự nguyện
chấp nhận theo phác đồ điều trị của chuyên môn.
- Có hồ sơ lưu trữ đầy đủ.
- Có thông tin về tình trạng bệnh sau điều trị
qua các lần tái khám định kỳ và/hoặc qua trả lời
thư theo mẫu.
2.1.2. Tiêu chuẩn loại trừ
- Bệnh nhân bỏ dở điều trị không phải lý do
chuyên môn;
- Các bệnh nhân mắc các bệnh phối hợp khác
có chống chỉ định của hóa trị (tim mạch, gan,
thận…);
- Có hóa trị hoặc xạ trị trước đây.
- Phụ nữ có thai, cho con bú.
2.2. Phương pháp nghiên cứu
2.2.1. Thiết kế nghiên cứu.
Nghiên cứu mô tả
hồi cứu kết hợp tiến cứu.
2.2.2. Quy trình điều trị
- Bệnh nhân đáp ứng tiêu chuẩn chọn được
ghi nhận các thông tin về lâm sàng, cận lâm sàng.
- Bệnh nhân sẽ được kết hợp hóa xạ trị đồng
thời theo phác đồ sau: Cisplatin 100 mg/m2 Tĩnh
mạch ngày 1, 22, 43
Xạ trị: 70 Gy vào u và hạch; 50 Gy dự phòng
hạch vùng cổ. Phân liều 2Gy/ngày. Xạ trị 5 ngày/
tuần.
Hình 2.1. Lập kế hoạch xạ trị cho bệnh nhân
ung thư vòm họng
- Thiết bị:
Máy xạ trị gia tốc ELEKTA với
collimator đa lá (MLC), lập kế hoạch xạ trị 3D
TẠP CHÍ Y HỌC VIỆT NAM TẬP 490 - THÁNG 5 - SỐ 1 - 2020
31
theo hình dạng khối u trên chương trình phần
mềm Xi.O 4.0.
- 03 chu kỳ hóa chất bổ trợ tiến hành 4 tuần
sau kết thúc hóa xạ trị đồng thời. Phác đồ CF:
Cisplatin 75 mg/m2 (N1) + 5 FU 1000
mg/m2/ngày (N1-N5). Chu kỳ 28 ngày
*Đánh giá kết quả điều trị
- Đánh giá đáp ứng điều trị: theo tiêu chuẩn
RECIST thông qua các dữ liệu trong bệnh án kết
quả MRI, CT, siêu âm [ 3].
- Đánh giá độc tính sau điều trị: theo tiêu
chuẩn CTCAE của Viện Ung thư quốc gia Hoa Kỳ
năm 2010 (CTCAE V.4.0) [ 4].
2.2.3. Xử lý và phân tích số liệu. Nhập và
xử lý số liệu bằng phần mềm SPSS 16.0. Kết quả
được xử lý thống kê, tính trung bình, độ lệch
chuẩn, so sánh 2 trị số trung bình theo t-test;
đánh giá sống thêm toàn bộ theo Kaplan-Meier.
III. KẾT QUẢ NGHIÊN CỨU
3.1. Đặc điểm lâm sàng, cận lâm sàng
*Tuổi và giới
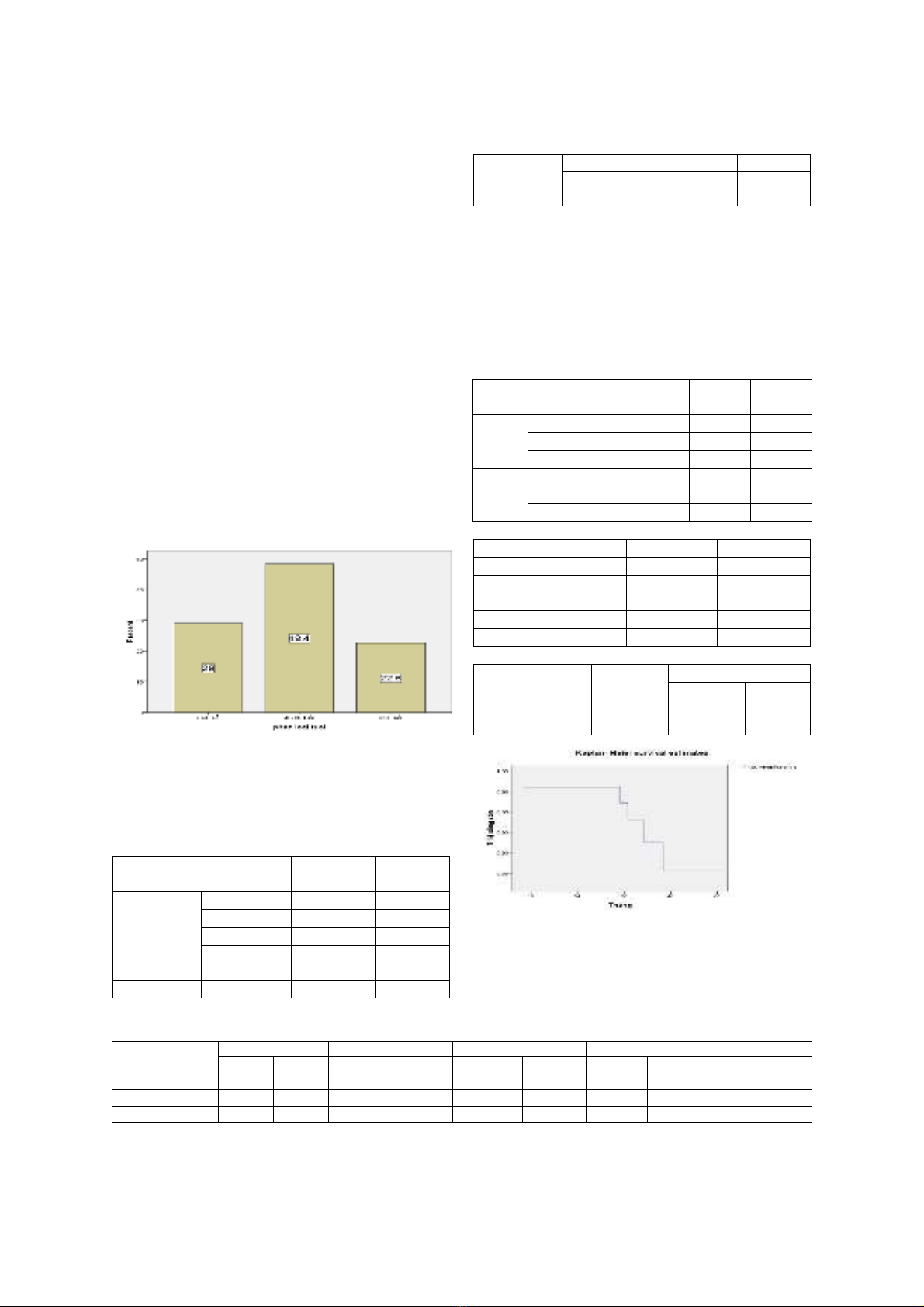
Biểu đồ 3.1. Phân loại theo nhóm tuổi
Nhận xét:
- Tuổi 20-70, trung bình 49,2 tuổi;
Độ tuổi 40-60 tuổi là hay gặp nhất (48,4%).
- Nam 77,4%; Nữ 22,6%
*Xếp loại TNM và giai đoạn bệnh theo
UICC/AJCC 2010
Bảng 3.1. Phân loại giai đoạn theo TNM
Phân loại theo TNM
Tần số
(n)
Tỷ lệ
(%)
Phân loại
theo T
T1
15
24.2
T2
18
29.0
T3
20
32.3
T4
9
14.5
Tổng
62
100.0
Phân loại
N1
42
67.7
theo N
N2
17
27.4
N3
3
4.8
Tổng
62
100.0
Nhận xét: - Giai đoạn T1 (24,2%), T2
(29%), T3 (32,3%), T4 (14,5%).
- Hạch N1 67,7%, hạch N2 27,4%, hạch N3 4,8%.
*Đặc điểm mô bệnh học
Ung thư biểu mô không biệt hóa: 54/62 BN,
chiếm 87,1%. Ung thư biểu mô vảy không sừng
hóa 5/52 BN, chiếm 8,1% và 3 trường hợp ung
thư biểu mô vảy kém biệt hóa chiếm 4,8%.
3.2. Đánh giá kết quả điều trị
Bảng 3.2. Đáp ứng sau điều trị tại u và hạch
Đáp ứng thực thể
Tần số
(n)
Tỷ lệ
(%)
Đáp
ứng tại
u
Đáp ứng hoàn toàn
60
96.8
Đáp ứng bán phần
2
3.2
Tổng
62
100.0
Đáp
ứng tại
hạch
Đáp ứng hoàn toàn
58
93,5
Đáp ứng bán phần
4
6,5
Tổng
62
100.0
Bảng 3.3. Đáp ứng chung sau điều trị
Đáp ứng chung
Tần số (n)
Tỷ lệ (%)
Đáp ứng hoàn toàn
58
93,5
Đáp ứng bán phần
4
6,5
Bệnh ổn định
0
0
Bệnh tiến triển
0
0
Tổng
62
100.0
*Sống thêm toàn bộ
Tổng số BN
theo dõi trên
3 năm
Số đã
tử
vong
Số còn sống
Tần số
(n)
Tỉ lệ
(%)
51
5
46
90.2%
Biểu đồ 3.2. Tỉ lệ sống còn toàn bộ 3 năm
Nhận xét:
Trong 51 bệnh nhân được theo
dõi từ 3 năm trở lên, tỉ lệ sống thêm toàn bộ 3
năm đạt 90,2%, có 05 bệnh nhân tử vong do
bệnh tái phát di căn.
3.3. Đánh giá tác dụng không mong muốn của điều trị
Bảng 3.4. Độc tính cấp trên huyết học
Độc tính
Độ 0
Độ 1
Độ 2
Độ 3
Độ 4
N
%
n
%
n
%
n
%
n
%
Giảm HC
38
61,3
23
37.1
1
1.6
0
0
0
0
Giảm BC
25
40.3
23
37.1
7
11.3
4
6.5
3
4.8
Giảm TC
54
87.1
6
9.7
1
1.6
1
1.6
0
0

vietnam medical journal n01 - MAY - 2020
32
Nhận xét:
Giảm bạch cầu độ 1, độ 2 với tỉ lệ tương ứng là 37,1%, 11,3%. Thiếu máu gặp ở
38,7%, trong đó chủ yếu là độ 1 (37,1%). Giảm tiểu cầu gặp ở 12,9%, chủ yếu là độ 1 (9,7%).
Bảng 3.5. Độc tính ngoài hệ tạo huyết
Độc tính
Độ 0
Độ 1
Độ 2
Độ 3
Độ 4
n
%
N
%
n
%
n
%
n
%
Tăng Ure
55
88.7
7
11.3
0
0
0
0
0
0
Tăng Creatinin
58
93,5
4
6,5
0
0
0
0
0
0
Tăng ALT
51
82.3
11
17.7
0
0
0
0
0
0
Tăng AST
55
88.7
7
11.3
0
0
0
0
0
0
Buồn nôn, nôn
26
41,9
12
19,4
18
29,0
6
9,7
0
0
Viêm da
0
0
15
24,2
36
51,8
11
17,7
0
0
Viêm niêm mạc
0
0
9
14,5
38
61,3
15
24,2
0
0
Nhận xét:
Độc tính trên gan, thận chỉ gặp ở độ 1. Có 11,3% tăng Ure, 6,5% tăng Creatinin ,
17,7% tăng ALT và 11,3% tăng AST. Tỷ lệ viêm niêm mạc là 100%, trong đó độ 3 chiếm 24,2%.
Nôn, buồn nôn 59,1%.
IV. BÀN LUẬN
Trong nghiên cứu của chúng tôi tuổi trung
bình của các bệnh nhân là 49,2 . Nhỏ nhất là 20
tuổi, lớn nhất là 70 tuổi. Độ tuổi 40-60 gặp nhiều
nhất ở cả hai giới (48,4%). Nam gặp nhiều hơn
nữ, tỷ lệ nam/nữ là 3,4/1. Kết quả này cũng
tương đồng với nhiều kết quả nghiên cứu trong
và ngoài nước. Nghiên cứu của Trần Hùng và CS
năm 2010 [ 5] có tuổi trung bình là 47,7. Nghiên
cứu của Bùi Quang Vinh năm 2012 [6] độ tuổi có
tỉ lệ mắc bệnh cao nhất từ 40- 59 (66,2%). Tỉ lệ
nam/nữ trong nghiên cứu của chúng tôi là 3,4/1
so với nghiên cứu của Trần Hùng và CS là 2,8/1,
Ngô Thanh Tùng là 2,7/1 [7]. Có thể lý giải điều
này do thói quen sinh hoạt của nam giới hay hút
thuốc, uống rượu nhiều, lao động trong môi
trường độc hại nhiều hơn nữ giới nên tỉ lệ nên tỉ
lệ ung thư vòm cao hơn nữ giới.
Trong nghiên cứu của chúng tôi đa phần
bệnh nhân ở giai đoạn II, III theo UICC/AJCC
2010 với tỉ lệ (41,9%) và (40,3%). Giai đoạn T1
(24,2%), T2 (29%), T3 (32,3%), T4 (14,5%).
Hạch N1 chiếm tỉ lệ cao nhất (67,7%), hạch N2
là (27,4%), hạch N3 là (4,8%). Tỉ lệ này có khác
với nghiên cứu của Đặng Huy Quốc Thịnh [8]
chủ yếu các bệnh nhân ở giai đoạn III (41,3%)
và IVb (37,2%). Nghiên cứu của Bùi Quang Vinh
[6] các bệnh nhân chủ yếu ở giai đoạn IV là
(51%), giai đoạn III là 49%.
Trong 62 BN nghiên cứu, tỷ lệ đáp ứng hoàn
toàn (ĐUHT) tại u đạt 96,8%; ĐUHT tại hạch đạt
93,5%. Tính chung, 100% BN có đáp ứng, trong
đó đáp ứng hoàn toàn (ĐƯHT) là 93,5% và đáp
ứng một phần là 6,5%. Kết quả trong nghiên
cứu của chúng tôi cao hơn kết quả nghiên cứu
của Bùi Quang Vinh (2012) áp dụng phác đồ
hướng dẫn của NCCN cho kết quả tỉ lệ đáp ứng
hoàn toàn tại u là 91,1%, đáp ứng một phần tại
u là 8,9%[6]. Đáp ứng hoàn toàn tại hạch là
92,8%, đáp ứng một phần tại hạch là 7,2%. Đáp
ứng chung hoàn toàn sau điều trị là 89,3%, đáp
ứng một phần là 10,7%. Điều này là do trong
nghiên cứu của chúng tôi giai đoạn II, III và
hạch N1 chiếm đa số.
Trong 51 bệnh nhân được theo dõi từ 3 năm
trở lên, tỉ lệ sống thêm toàn bộ 3 năm đạt
90,2%, có 05 bệnh nhân tử vong do bệnh tái
phát di căn. Kết quả này của chúng tôi có cao
hơn kết quả nghiên cứu của Bùi Quang Vinh
(2012) và Đặng Huy Quốc Thịnh (2012) có tỉ lệ
sống còn thêm 3 năm lần lượt là 85,1% và
80,6% [6],[8].
Độc tính trên hệ huyết học đa phần là giảm
bạch cầu độ 1, độ 2 với tỉ lệ tương ứng là
37,1%, 11,3%. Tuy nhiên cũng có 04 trường hợp
giảm bạch cầu độ 3 chiếm tỉ lệ 6,5%, 03 trường
hợp giảm bạch cầu nặng độ 4 chiếm tỉ lệ 4,8%.
Thiếu máu gặp ở 38,7%, trong đó chủ yếu là độ 1
(37,1%). Giảm tiểu cầu gặp ở 12,9%, chủ yếu là
độ 1 (9,7%), không có trường hợp nào giảm tiểu
cầu nặng độ 4. Trong nghiên cứu này, chỉ gặp các
độc tính trên gan, thận độ 1. Có 11,3% tăng Ure,
6,5% tăng Creatinin, 17,7% tăng GOT và 11,3%
tăng GPT sau điều trị. Không gặp các độc tính độ
2, 3, 4. Độc tính trên thận và gan là tác dụng phụ
của hóa trị nói chung, đặc biệt là của Cisplatin, là
một trong các tác nhân có nhiều độc tính trên
thận. Tuy nhiên theo nhiều nghiên cứu, mức độ
độc tính trên gan, thận của phác đồ hóa xạ dựa
trên Cisplatin đều ít gặp với mức độ thấp. Theo
Bùi Vinh Quang (2012), độc tính trên gan là
10,7% (chủ yếu độ 1), và thận là 5,4% độ 1[6].
100% BN có viêm da và viêm loét niêm mạc, chủ
yếu gặp độ 2.
V. KẾT LUẬN
- Tỷ lệ đáp ứng hoàn toàn tại u đạt 96,8%;
tại hạch đạt 93,5%. Tính chung, 100% BN có
đáp ứng, trong đó đáp ứng hoàn toàn là 93,5%

TẠP CHÍ Y HỌC VIỆT NAM TẬP 490 - THÁNG 5 - SỐ 1 - 2020
33
Tỉ lệ sống thêm toàn bộ 3 năm đạt 90,2%.
- Độc tính trên hệ huyết học đa phần là giảm
bạch cầu độ 1, độ 2 với tỉ lệ tương ứng là
37,1%, 11,3%. 03 trường hợp giảm bạch cầu
nặng độ 4 chiếm tỉ lệ 4,8%. Các độc tính trên
gan, thận ở độ 1. Viêm niêm mạc 100%, độ 3
chiếm 24,2%.
TÀI LIỆU THAM KHẢO
1. Estimating the global cancer incidence and
mortality in 2018: GLOBOCAN sources and
methods J. Ferlay, M. Colombet, I.
Soerjomataram, C. Mathers, D.M. Parkin, M.
Piñeros, A. Znaor, F. Bray 23 October 2018
https://doi.org/10.1002/ijc. 31937.
2. Al-Sarraf M., LeBlanc M., Giri P.G., et al.
(1998). Chemoradiotherapy versus radiotherapy
in patients with advanced nasopharyngeal cancer:
phase III randomized Intergroup study 0099. J
Clin Oncol, 16 (4), 1310-1317.
3. Therasse (2000). New guidelines to evaluate the
response to treatment in solid tumors J Natl
Cancer Inst, 92 (3), 205-216.
4. Institute N.C. (2010). Common Terminology
Criteria for Adverse Events (CTCAE) V.4.0.
5. Trần Hùng và CS (2010). Đánh giá kết quả bước
đầu hóa xạ trị cho bệnh nhân ung thư vòm mũi
họng giai đoạn IIB-IVB tại bệnh viện K năm 2007,
Luận văn thạc sĩ y học, Trường Đại học Y Hà Nội.
6. Bùi Quang Vinh (2012), “Nghiên cứu điều trị ung
thư vòm họng giai đoạn III-IV(M0) bằng phối hợp
hóa xạ trị gia tốc ba chiều theo hình dạng khối u”,
Luận văn tiến sĩ y học- Ung thư học. Trường đại
học y Hà Nội.
7. Ngô Thanh Tùng (2001), “Nghiên cứu đặc điểm
lâm sàng, mô bệnh học và kết quả xạ trị ung thư biểu
mô vòm họng tại Bệnh viện K giai đoạn 1993- 1995” ,
Luận văn thạc sỹ Y học, Trường Đại học Y HN.
8. Đặng Huy Quốc Thịnh (2012). “Hóa-xạ trị đồng
thời carcinôm vòm hầu giai đoạn tiến xa tại chỗ-tại
vùng”, Luận án tiến sĩ y học, Trường Đại học Y
Dược Thành phố Hồ Chí Minh.
NGHIÊN CỨU ĐẶC ĐIỂM LÂM SÀNG, TỔN THƯƠNG CỦA TẮC
HOÀN TOÀN MẠN TÍNH MẠCH VÀNH VÀ KẾT QUẢ CAN THIỆP
MẠCH VÀNH QUA DA TẠI TRUNG TÂM TIM MẠCH, BỆNH VIỆN E
Phan Thảo Nguyên1, Nguyễn Oanh Oanh2, Lê Ngọc Thành1
TÓM TẮT9
Mục đích: Nghiên cứu đặc điểm lâm sàng, tổn
thương và kết quả can thiệp qua da của tắc hoàn toàn
mạn tính mạch vành từ tháng 1/2015 đến tháng
12/2018 có 75 bệnh nhân đủ tiêu chuẩn chẩn đoán
tắc hoàn toàn mạn tính mạch vành được điều trị can
thiệp qua da tại Trung tâm tim mạch – Bệnh Viện E.
Phương pháp và kết quả: tuổi trung bình của nhóm
nghiên cứu là 67,59 ± 8,67, độ tuổi thấp nhất là 42
năm tuổi, độ tuổi cao nhất là 83 tuổi, tỷ lệ mắc bệnh
nam/nữ > 3/1. Tăng huyết áp là 86,7%, tất cả các
bệnh nhân hút thuốc là nam giới chiếm70,7% và tiền
sử của nhồi máu cơ tim và đã được can thiệp chiếm
42,7%. Mức độ đau ngực theo CCS I, II, III, và đau
ngực IV là (13,3%, 49,3%, 28,0%, 9,3%). Mức độ
suy tim là theo NYHA I, II, III, IV (12,0%, 69,3%,
16,0% và 2,7%). Tỷ lệ phần trăm của từng vị trí tổn
thương tắc nghẽn mạn tính hoàn toàn LAD, LCx, RCA
(34,5%, 20,3% và 45,3%). Chiều dài vị trí CTO có tổn
thương trung bình LAD, LCx, RCA (15,87 ± 4,40 mm,
16,82 ± 4,02 mm, 17,81 ± 4,49 mm). Tổng điểm
trung bình mức độ phức tạp của J-CTO là 1,44 +/-0,
90. Thời gian can thiệp trung bình 124,37 ± 49,54
1Bệnh viện E
2Học viện Quân Y
Chịu trách nhiệm chính: Phan Thảo Nguyên
Email: bsphanthaonguyen@gmail.com
Ngày nhận bài: 4/3/2020
Ngày phản biện khoa học: 1/4/2020
Ngày duyệt bài: 14/4/2020
phút. Thời gian chiếu tia trung bình là 78,69 ± 32,27
phút. Liều thuốc cản quang trung bình là 305,85 ±
56,59 ml. Trong số 75 bệnh nhân được can thiệp có
84 tổn thương CTO trong đó có 76 vị trí tổn thương
CTO đã được tiến hành can thiệp chiếm tỷ lệ 90,5%.
Có 16 vị trí tổn thương được can thiệp ngược dòng, 60
vị trí tổn thương CTO đã được can thiệp xuôi dòng: tỷ
lệ thành công chung là 96%, tỷ lệ can thiệp thất bại là
4,0%. Kết luận: Tắc mạn tính hoàn toàn mạch vành
thường gặp ở các bệnh nhân có tiền sử nhồi máu cơ
tim hoặc bệnh mạch vành ổn định, với các mức độ
biểu hiện khác nhau triệu chứng lâm sàng. Điều trị tổn
thương CTO cho thấy một tỷ lệ thành công cao, các
biến chứng ít trầm trọng hơn so với phẫu thuật giúp
bệnh nhân cải thiện các triệu chứng, chất lượng cuộc
sống, chức năng thất trái ngay sau can thiệp.
Từ khóa:
Tắc mạch vành hoàn toàn mạn tính, can
thiệp mạch vành qua da.
SUMMARY
COMMENT THE CLINICAL SIGNS, LESIONS
OF CHRONIC TOTAL OCCUSIONS AND
PERCUTANEOUS CORONARY INTERVENTION
IN CARDIOVASCULAR CENTRE, E HOSPITAL
Objectives: We sought to investigate the clinical
and lesions characteristics as well as outcomes of
percutaneous coronary intervention (PCI) for patients
diagnosed with coronary chronic total occlusion (CTO)
from January 2015 to December 2018 at
Cardiovascular Centre, E Hospital. Methods and
results: A total of 75 patients were included. The
mean age of the study cohort was 67.59 ± 8.67


























