
Đ CHÍNH TH CỀ Ứ
S GIÁO D C VÀ ĐÀO T OỞ Ụ Ạ
QU NG NAMẢ
(Đ thi có 02 trang)ề
KI M TRA H C K I NĂM H C 2019-2020Ể Ọ Ỳ Ọ
Môn: Hoá h c – L p 10ọ ớ
Th i gian: 45 phút (ờkhông k th i gian giao để ờ ề)
MÃ Đ: 303Ề
Cho bi t nguyên t kh i: Ca= 40; Mg= 24; Be= 9; Ba=137; Fe= 56; Cr=52; O= 16; S=16; H=1.ế ử ố
H và tên h c sinh: ............................................................... L p: ................ọ ọ ớ
A/ TR C NGHI M: (5,0 đi m)Ắ Ệ ể
Câu 1: Nguyên t nào trong s các nguyên t :ố ố ố 8O, 9F, 15P, 16S có tính phi kim y u nh t?ế ấ
A. O. B. P. C. S. D. F.
Câu 2: Nguyên t c a nguyên t X có 19 electron. Nguyên t X ử ủ ố ố là
A. F. B. K. C. Ar. D. Ca.
Câu 3: S electron t i đa trong l p M làố ố ớ
A. 8. B. 32. C. 18. D. 2.
Câu 4: Nguyên t c a nguyên t X có t ng s h t p, n, e là 60. Trong h t nhân, s h t ử ủ ố ổ ố ạ ạ ố ạ
không mang đi n nhi u h n s h t mang đi n là 3. S kh i c a X làệ ề ơ ố ạ ệ ố ố ủ
A. 20. B. 41. C. 43. D. 29.
Câu 5: S oxi hóa c a nit trong Nố ủ ơ 2O là
A. -2. B. +4. C. +1. D. +2.
Câu 6: Oxit cao nh t c a m t nguyên t X thu c nhóm IIA ch a 40,0% oxi v kh i l ng.ấ ủ ộ ố ộ ứ ề ố ượ
Nguyên t X làố
A. Ca. B. Mg. C. Ba. D. Be.
Câu 7: Cation kali trong máu ng i có n ng đ vào kho ng 3,5 đn 4,5 mmol/l, đóng vai tròườ ồ ộ ả ế
quan tr ng trong ho t đng co c , d n truy n th n kinh, ... Kí hi u hóa h c c a cation này làọ ạ ộ ơ ẫ ề ầ ệ ọ ủ
A. Ka+.B. K+1.C. K+.D. K-.
Câu 8: Nguyên t c a nguyên t X có c u hình electron l p ngoài cùng là 3sử ủ ố ấ ớ 23p5. Phát bi uể
nào sau đây sai?
A. X chu kì 3, nhóm VIIA trong b ng HTTH.ở ả B. Liên k t c a X v i Na là c ng hóa ế ủ ớ ộ
tr . ị
C. Nguyên t ốX có tính phi kim. D. H p ch t khí v i hiđro c a X là HXợ ấ ớ ủ .
Câu 9: C u hình electron nguyên t c a nguyên t X là 1sấ ử ủ ố 22s22p4. Trong b ng h th ngả ệ ố
tu n hoàn, X thu c nhómầ ộ
A. IVA. B. IIA. C. VIA. D. VIIIA.
Câu 10: Các nguyên t x p chu kì 4 trong b ng tu n hoàn có s l p electron trong nguyênố ế ở ả ầ ố ớ
t làử
A. 8. B. 32. C. 6. D. 4.
Câu 11: Trong ph n ng Fe +ả ứ 2AgNO3
Fe(NO3)2 + 2Ag thì 1 mol Ag+ đã
A. nh ng 0,5 mol electron. ườ B. nh n 2 mol electron. ậ
C. nh ng 1 mol electron. ườ D. nh n 1 mol elecậtron.
Câu 12: S kh i c a nguyên t ố ố ủ ử
7
3
Li là
A. 3. B. 7. C. 4. D. 10.
Câu 13: Ph n ng hóa h c nào sau đây là ph n ng trao đi?ả ứ ọ ả ứ ổ
A. 2KClO3
o
t
2KCl + 3O2.B. AgNO3 + NaCl
AgCl + NaNO3.
C. Zn + 2HCl
ZnCl2 + H2.D. 4Na + O2
2Na2O.
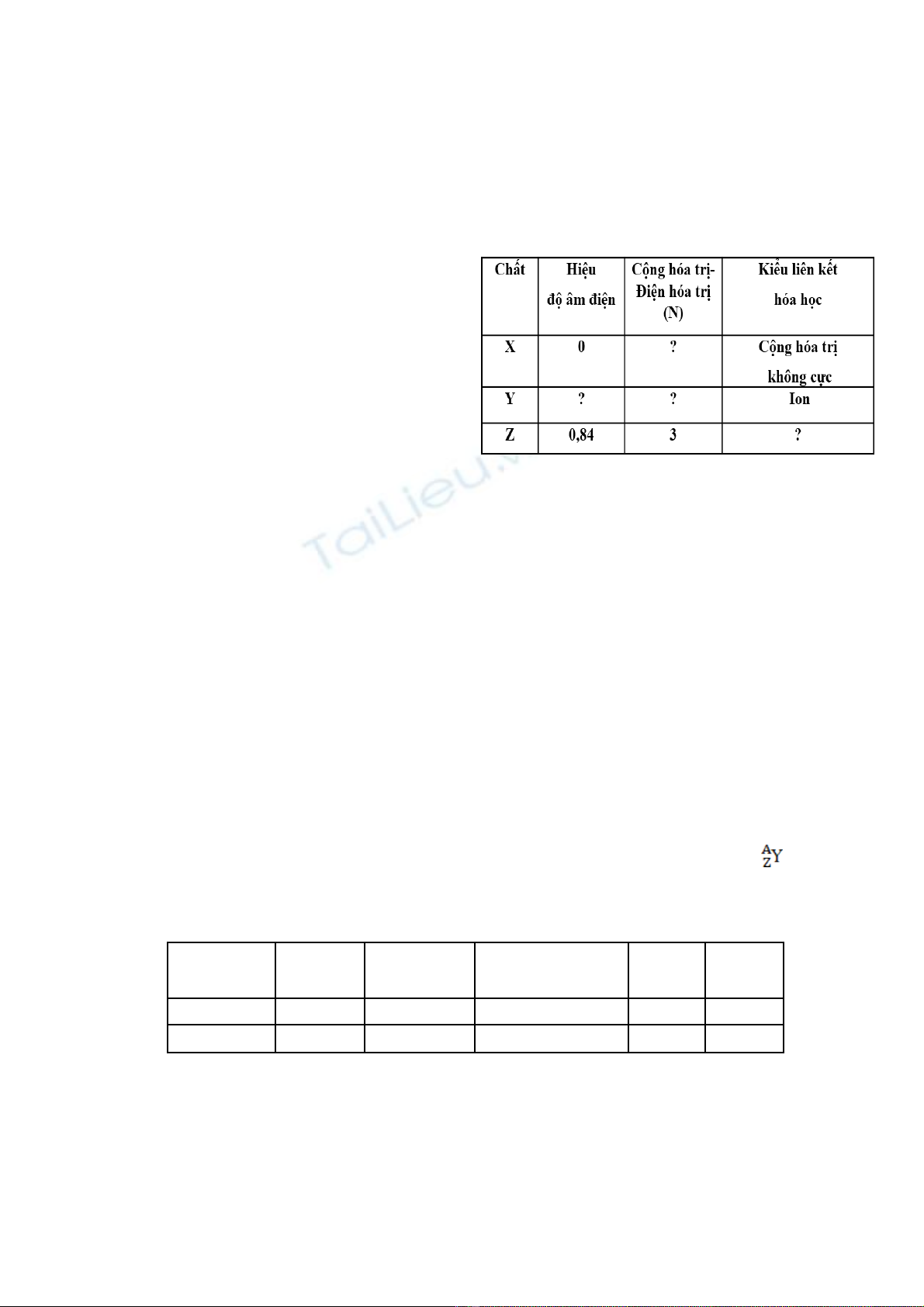
Câu 14: Cho X, Y, Z là các ch t khác nhau trong 3 ch t: Liấ ấ 3N, NH3, N2. Tính ch t c a chúngấ ủ
đc ghi trong b ng d i. Bi t đ âm đi n c a Li: 0,98; N: 3,04; H: 2,20.ượ ả ướ ế ộ ệ ủ
Cho các phát bi u sau:ể
(a) C ng hóa tr c a nguyên t N trong X là 3.ộ ị ủ ố
(b) Hi u đ âm đi n c a liên k t trong Y làệ ộ ệ ủ ế
0,1.
(c) Liên k t hóa h c trong Z là liên k t ion. ế ọ ế
(d) Đi n hóa tr c a nguyên t N trong Y là 3+.ệ ị ủ ố
S phát bi u đúng làố ể
A. 2. B. 3. C. 4. D. 1.
Câu 15: Các h p ch t có ch a Crợ ấ ứ +6 khi hi n di n trong n c th i gây ô nhi m môi tr ng, ệ ệ ướ ả ễ ườ
đe d a đn s c kh e và tính m ng con ng i. Có th x lý các h p ch t đó b ng ọ ế ứ ỏ ạ ườ ể ử ợ ấ ằ
FeSO4.7H2O theo c ch : ơ ế Fe+2 + Cr+6
Fe+3+ Cr+3.
Bi t r ng n ng đ Crế ằ ồ ộ +6 trong n c th i c a m t nhà máy m kim lo i là 0,005 mol/l.ướ ả ủ ộ ạ ạ
Kh i l ng FeSOố ượ 4.7H2O (kg) c n dùng đ x lí ầ ể ử 15 m3 n c th i này là ướ ả
A. 20,85. B. 34,2. C. 12,6. D. 62,55.
B/ T LU N: (5,0 đi m)Ự Ậ ể
Câu 1. (1,5 đi m)ể
Nguyên t c a nguyên t Y có s h t mang đi n tích âm bé h n s h t không mangử ủ ố ố ạ ệ ơ ố ạ
đi n tích là 1 h t. S h t mang đi n tích d ng c a nó là 17. ệ ạ ố ạ ệ ươ ủ
a. Hãy tính toán xác đnh tên nguyên t , s kh i và kí hi u nguyên t (d ng ị ố ố ố ệ ử ạ ) c a Y.ủ
b. Cho bi t Y là kim lo i, phi kim hay khí hi m. Vì sao?ế ạ ế
Câu 2. (2,25 đi m)ể
a. D a vào b ng HTTH, đi n thông tin còn thi u vào ô tr ng.ự ả ề ế ố
Tên
nguyên tốKí hi uệS hi uố ệ
nguyên tửC u hình e ấ
l p ngoài cùngớChu kìNhóm
Natri Na 11 3s13 IA
Iot 5 VIIA
b. Cho đ âm đi n (ộ ệ χ) c a các nguyên t : Rb (0,82), H (2,20), Cl (3,16). Bi t r ngủ ố ế ằ
trong s các ch t: RbCl, HCl, Clố ấ 2, ch t nào có liên k t càng phân c c (ấ ế ự Δχ càng l n) thì có đớ ộ
tan (S) trong n c (g/100ml n c, đi u ki n th ng) càng l n. Hãy tính ướ ướ ở ề ệ ườ ớ Δχ và ch ra ch tỉ ấ
nào trong 3 ch t trên có giá tr S l n nh t.ấ ị ớ ấ
c. Hãy nêu 2 lu n đi m đ ch ng t r ng b ng HTTH đang đc s d ng ph bi nậ ể ể ứ ỏ ằ ả ượ ử ụ ổ ế
ngày nay không ch là thành t u c a nhà bác h c Mendeleev.ỉ ự ủ ọ
Câu 3. (1,25 đi m)ể

a. Trong ph n ng th , s oxi hóa c a các nguyên t có thay đi hay không?ả ứ ế ố ủ ố ổ
b. Cân b ng ph n ng hóa h c sau b ng ph ng pháp thăng b ng electron (trình bày ằ ả ứ ọ ằ ươ ằ
đ 4 b c): ủ ướ Mg + HNO3 Mg(NO→3)2 + NO2 + H2O.
-----o0o-----
H c sinh đc s d ng b ng h th ng tu n hoàn các nguyên t hóa h c.ọ ượ ử ụ ả ệ ố ầ ố ọ
ĐÁP ÁN
CâuĐA CâuĐA CâuĐA
1B6B11 D
2B7C12 B
3C8B13 B
4B9C14 D
5C10 D15 D
N i dungộ CÁC Đ 303, 306, 309, 312, 315, 318, 321, 324ỀBi u đi mể ể
Câu 1 1,5
a. p = 17 = e, n = e +1 = 18.
X là Clo (Cl).
A= p + n= 35.
Kí hi u nguyên t : ệ ử
0,25
0,25
0,25
0,25
b. X là phi kim.
Vì c u hình Cl: 1sấ22s22p63s23p5 có 7 electron l p ngoài cùng.ở ớ 0,25
0,25
Câu 2 2,25
a.
Tên
nguyên tốKí hi uệS hi uố ệ
nguyên tửC u hình e ấ
l p ngoài cùngớChu kìNhóm
Natri Na 11 3s13 IA
Iot I 53 5s25p55 VIIA
0,75
(0,25x3)
b.
Ch tấRbCl HCl Cl2
Δχ2,34 0,96 0
RbCl có Δ l n nh t nên có giá tr S l n nh t.χớ ấ ị ớ ấ
0,50
0,50
c. H c sinh nêu đc 2 lu n đi m v vi c b ng HTTH đang đc s d ngọ ượ ậ ể ề ệ ả ượ ử ụ
ph bi n ngày nay không ch là thành t u c a nhà bác h c Mendeleev. Víổ ế ỉ ự ủ ọ
d :ụ
- Mendeleev s p x p các nguyên t theo chi u tăng d n M v i giá tr M doắ ế ố ề ầ ớ ị
các th h nhà bác h c tr c ông đã xác đnh.ế ệ ọ ướ ị
- Quy t c s p x p các nguyên t theo chi u tăng d n M ch a chính xác vàắ ắ ế ố ề ầ ư
0,50

đc các th h nhà bác h c sau này hoàn ch nh v i quy t c s p x p theoượ ế ệ ọ ỉ ớ ắ ắ ế
chi u tăng d n c a Z.ề ầ ủ
- B ng HTTH do Mendeleev công b còn thi u nhi u nguyên t v i nhi uả ố ế ề ố ớ ề
đi l ng ch a xác đnh đc, các nguyên t và đi l ng thi u đó đcạ ượ ư ị ượ ố ạ ượ ế ượ
các nhà bác h c sau ông xác đnh đ b sung, hoàn thi n thành b ng HTTHọ ị ể ổ ệ ả
nh ngày nay.ư
…
Câu 3. 1,25
a. Trong ph n ng th , s oxi hóa c a các nguyên t có thay đi.ả ứ ế ố ủ ố ổ 0,25
b. HS cân b ng đ 4 b c, m i b c 0,25đ.ằ ủ ướ ỗ ướ 1,0


























