Ngày so n:14/03/2011ạ
Ngày d y: 18/03/2011ạ
L p d y: 8Bớ ạ
Ti t 56 ế
Bài 37 : AXIT – BAZ - MU IƠ Ố (ti t 1ế)
**********
I. M C TIÊU:Ụ
1. Ki n th c:ế ứ
- H c sinh trình bày đc thành ph n, công th c hóa h c, phân lo i vàọ ượ ầ ứ ọ ạ
cách đc tên axit, baz .ọ ơ
- C ng c các ki n th c đã h c v đnh nghĩa, công th c hóa h c, tên g i,ủ ố ế ứ ọ ề ị ứ ọ ọ
phân lo i các oxit và m i liên quan c a các lo i oxit v i axit và baz t ngạ ố ủ ạ ớ ơ ươ
ng.ứ
2. K năngỹ :
- Rèn luy n k năng g i tên c a m t s h p ch t vô c khi bi t CTHH vàệ ỹ ọ ủ ộ ố ợ ấ ơ ế
ng c l i vi t đc CTHH khi bi t tên c a h p ch t.ượ ạ ế ượ ế ủ ợ ấ
3. Thái độ :
- Yêu thích môn h c.ọ
II. CHU N B C A GIÁO VIÊN VÀ H C SINHẨ Ị Ủ Ọ :
1. Giáo viên:
-Máy chi u.ế
-Phi u h c t p 1, 2ế ọ ậ
Phi u h c t p 1:ế ọ ậ
CTHH Thành
ph nầ
Hóa tr g c axitị ố
S nguyênố
t hidroử
G cố
axit
HCl
HBr
Page 1

H2S
HNO3
H2SO4
H2SO3
H2CO3
H3PO4
Phi u h c t p 2: ế ọ ậ
Tên axit CTH
H
Tên g c ố
HCl
HBr
H2S
HNO3
H2SO4
H2SO3
H2CO3
H3PO4
2. H c sinh:ọ
-H c bài cũ, chu n b bài m i.ọ ẩ ị ớ
III. TI N TRÌNH BÀY D Y:Ế Ạ
1. n đnh l p: ki m tra sĩ s .Ổ ị ớ ể ố
2. Ki m tra bài cũ: ể
Câu h i:ỏ
Hoàn thành các ph ng trình ph n ng sau:ươ ả ứ
K + H2O
Na2O + H2O
SO2 + H2O
Trong các s n ph m t o thành ph n ng trên, s n ph m nào là axit,ả ẩ ạ ở ả ứ ả ẩ
s n ph m nào là baz ?ả ẩ ơ
3. Gi ng bài m i:ả ớ
Page 2

a. M bàiở: Chúng ta đã làm quen v i m t s lo i h p ch t có tên là oxit.ớ ộ ố ạ ợ ấ
Trong các ch t vô c còn có các lo i ch t khác là axit, baz , mu i. Chúng làấ ơ ạ ấ ơ ố
nh ng h p ch t nh th nào? Có CTHH và tên g i ra sao ? Đc phân lo i thữ ợ ấ ư ế ọ ượ ạ ế
nào ? Đó là n i dung c a bài h c hôm nay.ộ ủ ọ
b. các ho t đng:ạ ộ
ho t đông 1: tìm hi u v axitạ ể ề .
M c tiêuụ: HS trình bày đc đnh nghĩa axit, phân lo i đc axit, cách g iượ ị ạ ượ ọ
tên axit, g c axit t ng ng.ố ươ ứ
Ph ng pháp gi ng d yươ ả ạ : Nêu v n đ, đàm tho i g i m , nghiên c u, th oẫ ề ạ ợ ở ứ ả
lu n nhóm.ậ
HO T ĐNG TH YẠ Ộ Ầ HO T ĐNG TRÒẠ Ộ N I DUNGỘ
Các em đã bi t nh ng axitế ữ
nào? CTHH ? Tên g i ?ọ
- S d ng b ng 1 : hãy ghiử ụ ả
s nguyên t hidro, g cố ử ố
axit và hóa tr g c axit vàoị ố
phi u h c t p s 1.ế ọ ậ ố
chi u b ng đáp ánế ả
chu n.YCHS so sánh v iẩ ớ
phi u h c t p c a nhómế ọ ậ ủ
mình.
- GV?: Có nh n xét gì vậ ề
thành ph n phân t c aầ ử ủ
các axit đó ? Nh n xét gìậ
v m i liên quan gi a sề ố ữ ố
nguyên t hidro và hóa trử ị
c a g c axit ?ủ ố
Nh n xét câu tr l iậ ả ờ
c a hs ủ: axit g m hidroồ
và g c axit, hóa tr c aố ị ủ
g c axit chính là số ố
- HS phát bi u: ểHCl,
H2SO4, HNO3….
- Hs th o lu n nhómả ậ
hoàn thành phi u h cế ọ
t p.ậ
- H nhóm th o lu n vàả ậ
phát bi u.ể
I. Axit :
Page 3

nguyên t hidro.ử
Nêu đnh nghĩa c a axitị ủ
theo nh n xét trên ?ậ
- Công th c hóa h c c aứ ọ ủ
axit g m 1 hay nhi uồ ề
nguyên t hidro và g cử ố
axit.
N u g i s nguyên tế ọ ố ử
hidro là n, g i chung g cọ ố
axit là A thì công th cứ
t ng quát c a axit s là:ổ ủ ẽ
HnA
G : nhìn vào phi u h cế ọ
t p 1, nhóm g m 3 axitậ ồ
đu tiên và nhóm g m cácầ ồ
axit còn l i có đi u gìạ ề
khác nhau v thành ph nề ầ
phân t ?ử
Có th chia thành 2 lo iể ạ
axit d a vào thành ph nự ầ
phân t axit có oxi và axitử
không có oxi
-GV thông báo cách g iọ
tên c a 2 lo i axit này.ủ ạ
L y ví d đc tên cho m iấ ụ ọ ỗ
lo i.ạ
-GV:Yêu c u HS th oầ ả
lu n nhóm làm phi u h cậ ế ọ
t p th 2. ậ ứ
- Hs phát bi u.ể
HS phát bi u: các axitể
đu có H và phi kimề
nh ng khác nhau vư ề
thành ph n oxi.ầ
HS nhóm trao đi vàổ
hoàn thành phi u h cế ọ
t p, báo cáo k t qu .ậ ế ả
1. Khái ni mệ : SGK
2. Công th c hóaứ
h cọ
HnA
3. Phân lo iạ :
G m: axit ch aồ ứ
OXI
Axit không
ch a OXI.ứ
4. Tên g iọ :
a) Axit không có oxi
axit+tên phi
kim+hidric
Tên g c: tên phi kimố
+ ua.
b) Axit có oxi :
Axit +phi kim +ic.
Axit có ít nguyên tử
oxi:
Page 4
GV chi u k t qu c a 1ế ế ả ủ
nhóm, nh n xét. Chi uậ ế
b ng chu n b ng 2 n uả ẩ ả ế
c n.ầ
Axit + phi kim +ơ
Tên g c axit: chuy nố ể
đuôi “ic” thành “at”,
“ơ” thành “it”
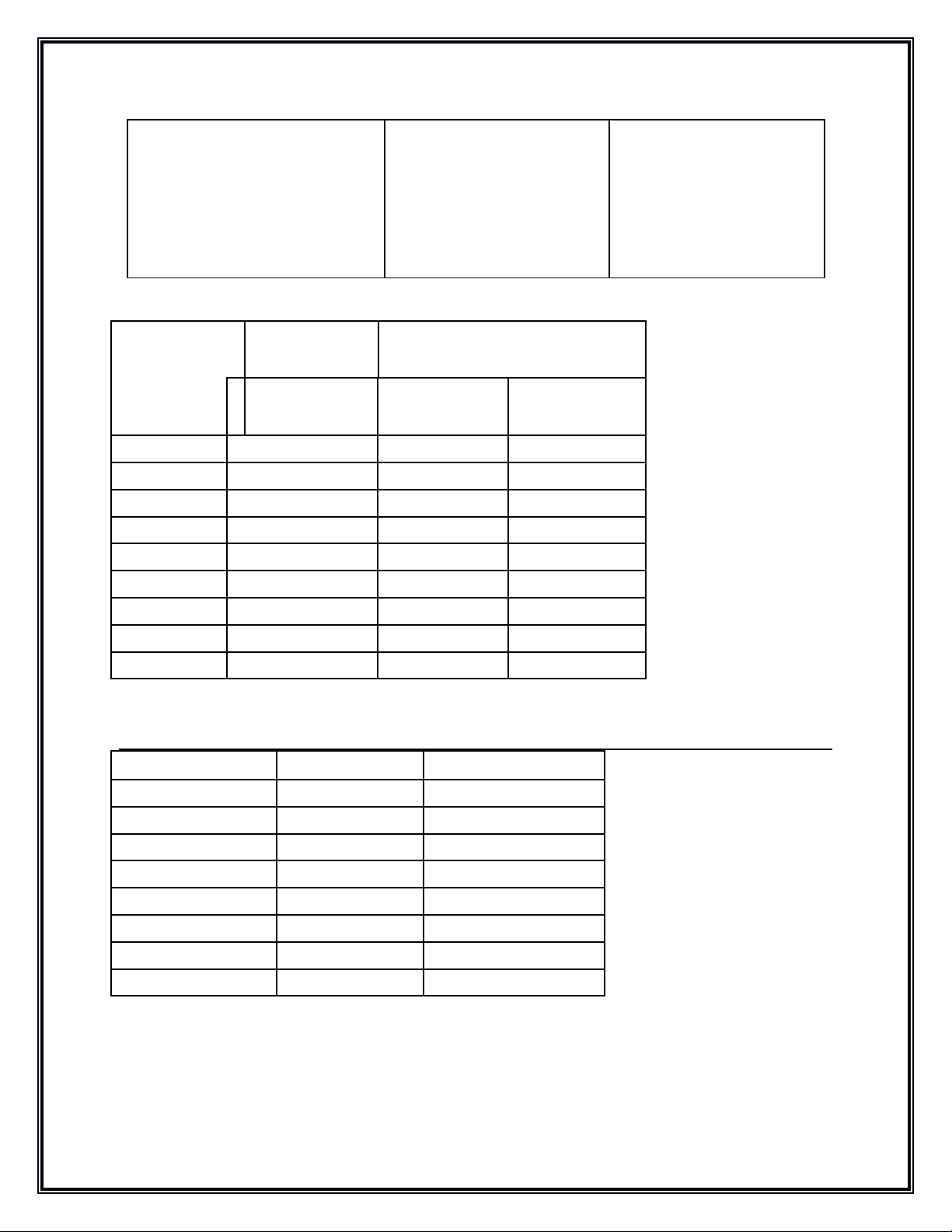
N i dung b n chu n 1:ộ ả ẩ
CTHH Thành
ph nầ
Hóa tr g c axitị ố
S nguyênố
t hidroử
G c axitố
HCl 1 -Cl 1
HBr 1 -Br 1
H2S 2 =S 2
HNO3 1 -NO31
H2SO4 2 =SO42
H2SO3 2 =SO32
H2CO3 2 =CO32
H3PO4 3 PO≡33
HnX n A
N i dung b n chu n b ng 2:ộ ả ẩ ả
Tên axit CTHH Tên g c ố
Axit clohiđric HCl Clorua
Axit bromhiđric HBr Bromua
Axit sunfuhiđric H2S Sunfua
Axit nitric HNO3Nitrat
Axit sunfuric H2SO4Sunfat
Axit sunfurơ H2SO3Sunfit
Axit cacbonic H2CO3cacbonat
Axit photphoric H3PO4photphat
Page 5


























