
HỘI THẢO KHOA HỌC UNG BƯỚU CẦN THƠ LẦN THỨ XIII – BỆNH VIỆN UNG BƯỚU THÀNH PHỐ CẦN THƠ
256
TỔNG QUÁT
LẬP KẾ HOẠCH XẠ TRỊ 3D-CRT
VÀ ĐẢM BẢO CHẤT LƯỢNG (QA) TRÊN MÁY COBALT-60
TẠI BỆNH VIÊN UNG BƯỚU THÀNH PHỐ CẦN THƠ
Lý Thế Hiển1, Nguyễn Thị Nhờ1,
Dương Tấn Phúc1, Trần Quang Khải1
TÓM TẮT33
Đặt vấn đề: Xạ trị sử dụng chùm tia photon
vẫn là một phương pháp phổ biến hiện nay trong
điều trị ung thư. Trong đó, kỹ thuật xạ trị ba
chiều theo hình dạng khối u (3D-CRT) được sử
dụng nhiều tại các bệnh viện và trung tâm xạ trị
hiện nay trong cả nước.
Đối tượng, phương pháp: Trong báo cáo
này, chúng tôi trình bày tổng quan quy trình xạ
trị, cụ thể là lập kế hoạch 3D-CRT bằng phần
mềm Eclipse và kiểm tra đảm bảo chất lượng
(QA) đo liều thực tế trên máy xạ Cobalt-60 bằng
phantom nước so với liều điểm tham chiếu của
kế hoạch xạ trị, độ chính xác của việc kiểm tra
liều dưới ± 5%.
Kết quả: Đánh giá trường hợp ung thư vùng
chậu và đầu cổ cho thấy liều vào bướu đạt liều
chỉ định và cơ quan lành nằm trong giới hạn liều
cho phép theo các tiêu chuẩn RTOG. Việc QA
liều của 4 trường hợp dữ liệu bệnh nhân cho thấy
việc tính toán liều thực tế so với liều trên hệ
thống lập kế hoạch xạ trị là gần tương đương
1Khoa Điều Trị Tia Xạ, Bệnh viện Ung Bướu
Thành phố Cần Thơ
Chịu trách nhiệm chính: Dương Tấn Phúc
SĐT: 0357120045
Email: tanphuc1012@gmail.com
Ngày nhận bài: 26/7/2024
Ngày phản biện: 29/7/2024
Ngày chấp nhận đăng: 31/7/2024
nhau với sai số trong khoảng 0-3%. Đảm bảo
thông số đầu ra của máy xạ Cobalt-60 chính xác,
tránh sai số hệ thống phần mềm có thể không
phát hiện trong khi vận hành và thực hành lâm
sàng.
Kết luận: Trong báo cáo này chúng tôi đã
tìm hiểu tổng quan được quy trình xạ trị theo kỹ
thuật 3D-CRT và cụ thể là quy trình lập kế hoạch
xạ trị trên phần mềm Eclipse tại bệnh viện Ung
Bướu Cần Thơ. Việc QA liều xạ cho những
trường chiếu được xem như một công cụ mạnh
mẽ cho việc kiểm tra QA trong khi vận hành hệ
thống lập kế hoạch điều trị.
Từ khóa: Xạ trị 3D-CRT, QA, phần mềm
Eclipse.
SUMMARY
RADIOTHERAPY PLANNING 3D-CRT
AND QUALITY ASSURANCE ON
COBALT-60 MACHINE AT CAN THO
ONCOLOGY HOSPITAL
Background: Photon beam radiotherapy is
still a popular method in cancer treatment today.
Of which, three-dimensional conformal radiation
therapy (3D-CRT) teachnique is widely used in
hospitals and radiation center nationwide today.
Methods: In this report, we present an
overview of the radiotherapy process,
specifically 3D-CRT planning using Eclipse
software and quality assurance (QA) checking of
actual dose measurement on the Cobalt-60

TẠP CHÍ Y HỌC VIỆT NAM TẬP 542 - THÁNG 9 - SỐ CHUYÊN ĐỀ - 2024
257
radiotherapy machine using a water phantom
compared with dose reference point of the
radiotherapy plan, the accuracy of the dose QA is
below ± 5%.
Results: Evaluation of the pelvic cancer;
head and neck cancer showed that the dose to the
tumor reached the prescribed dose; organs at risk
satisfy the tolerance doses according to
guidelines defined RTOG. Quality Assuarance
(QA) dose of four patients data showed that the
actual dose calculation compared to the dose on
the radiotherapy planning system was almost
equivalent with an error of about 0-3%. This
ensures that the output parameters of Cobalt-60
machine are accurate, avoiding errors that the
software system may not detect during operation
and clinical practice.
Conclusions: In this report, we have studied
the overview of the radiotherapy process using
3D-CRT technique; specifically the radiotherapy
planning process using Eclipse software at Can
Tho Oncology Hospital. The QA dose for
radiation fields is considered a powerful tool for
QA while operating the treatment planning
system.
Keywords: 3D-CRT radiotherapy, QA,
Eclipse software.
I. ĐẶT VẤN ĐỀ
Điều trị ung thư là điều trị đa mô thức
gồm xạ trị, phẫu thuật, hóa trị... Mỗi ca bệnh
đều được hội chẩn liên khoa để đưa ra phác
đồ hiệu quả nhất. Với những tiến bộ trong
lĩnh vực xạ trị (hệ thống máy móc đầy đủ)
chất lượng điều trị vượt trội hơn nhiều. Cụ
thể, tỷ lệ kiểm soát bệnh, kéo dài thời gian
sống của bệnh nhân tăng lên. Với ung thư
vòm họng, 20 năm trước, tỷ lệ sống thêm 5
năm chỉ đạt 33% nhưng nay đã tăng lên 65%.
Hay như ung thư phổi, trung bình trước đây
người bệnh chỉ sống thêm 1 năm, giờ đã lên
2 năm...[1].
Ngày nay, sự phát triển của các kỹ thuật
hiện đại và hệ thống máy tính giúp lập kế
hoạch xạ trị cho bệnh nhân trở nên chính xác
và hiệu quả cao như từ kỹ thuật 2D lên 3D-
CRT, IMRT, IGRT,… đã và đang ứng dụng
rộng rãi trong nước và trên thế giới.
Kỹ thuật xạ trị ba chiều theo hình dạng
khối u (3D-CRT) là một kỹ thuật được sử
dụng phổ biến hiện nay tại các trung tâm xạ
trị trong cả nước. Để hiểu rõ quy trình lập kế
hoạch xạ trị thực tế tại bệnh viện, báo cáo
này trình bày quy trình lập kế hoạch xạ trị
theo kỹ thuật 3D-CRT được tích hợp trong
phần mềm Eclipse phiên bản 8.9.21 (được hỗ
trợ từ bệnh viện Ung Bướu TP.Hồ Chí Minh
vào tháng 07 năm 2017) và được áp dụng
cho máy xạ trị ngoài sử dụng nguồn Cobalt-
60, hãng sản xuất Bhabhatron-II của Ấn Độ,
dùng chùm photon 1,25MeV, các nêm tĩnh
và tạo dạng trường chiếu với các khối chì để
xạ trị tại Khoa Điều trị Tia xạ, Bệnh viện
Ung Bướu Thành phố Cần Thơ.
II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
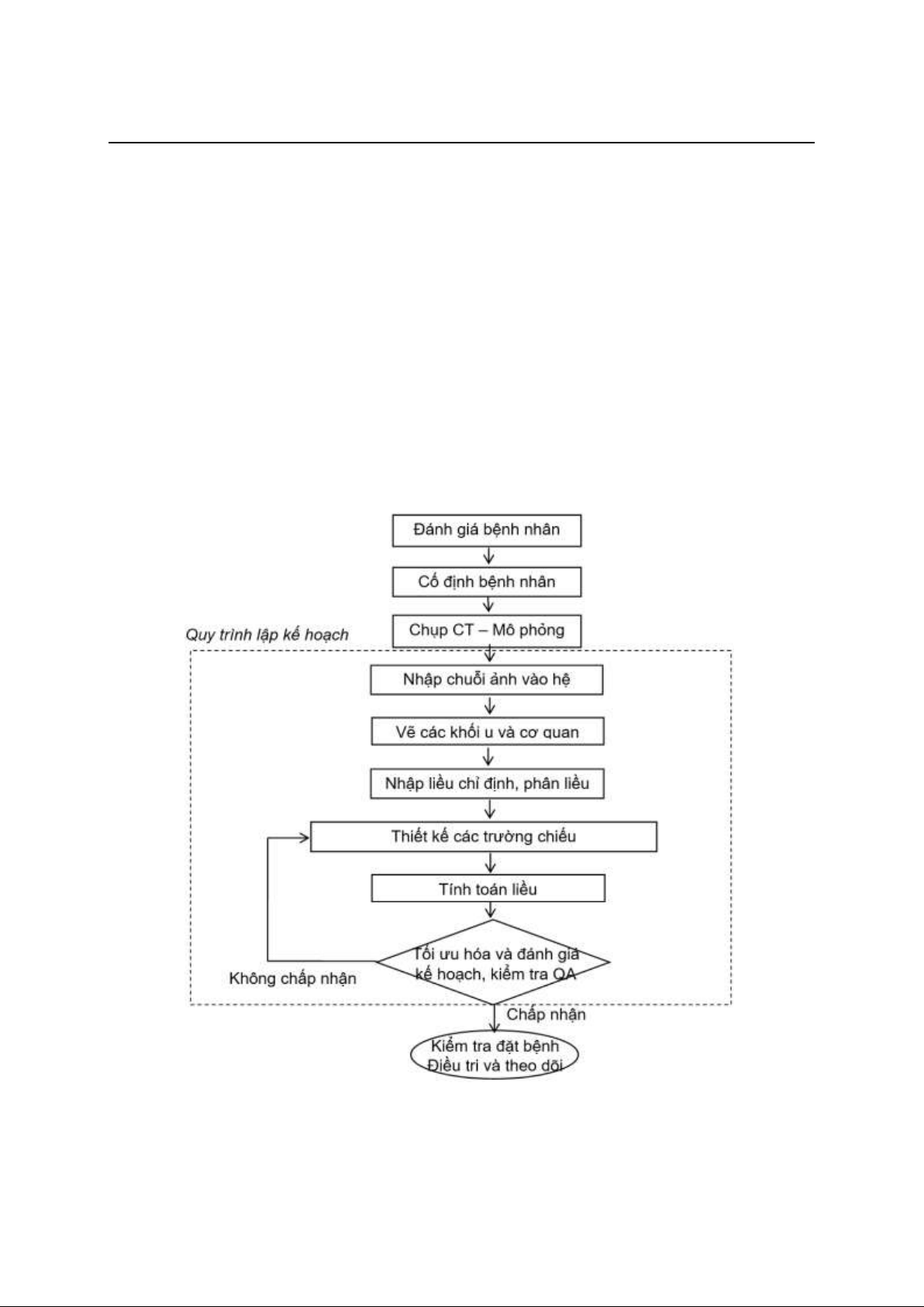
Sơ đồ tổng quát của quy trình xạ trị theo
phương pháp 3D-CRT được trình bày trong
Hình 1. Cụ thể, tìm hiểu quy trình lập kế
hoạch 3D-CRT tại Bệnh viện Ung bướu Cần
Thơ.
Sau khi đánh giá chỉ định liều xạ, bác sĩ
và kỹ sư vật lý sẽ phải tự xác định một mô
hình các trường chiếu phù hợp cho từng ca
bệnh cụ thể rồi cố định và chụp CT – Mô
phỏng bệnh nhân, toàn bộ dữ liệu hình ảnh
từng lát cắt của phim CT được đưa vào hệ
thống máy tính lập kế hoạch dựa trên phần
mềm Eclipse. Ta tiến hành lập kế hoạch xạ
trị, các bước của quy trình lập kế hoạch trên
phần mềm Eclipse được trình bày trong Hình
HỘI THẢO KHOA HỌC UNG BƯỚU CẦN THƠ LẦN THỨ XIII – BỆNH VIỆN UNG BƯỚU THÀNH PHỐ CẦN THƠ
258
1. Bác sĩ cần xác định các khối u và cơ quan
lành, vẽ thể tích lập kế hoạch PTV là mở
rộng từ CTV, vẽ các cơ quan lành gần đó để
khảo sát liều. Kỹ sư vật lý tạo trường chiếu,
chuẩn tâm chùm tia và đặt hay vẽ thiết bị phụ
trợ như nêm, chì cá nhân. Tạo trường chiếu
có thể sử dụng 2 chùm tia (đối song) thường
dùng cho các trường hợp ung thư đầu cổ khối
u nằm cạn. Sử dụng 3 chùm tia đối với khối
u nằm một bên và các chùm tia có thể không
đồng phẳng ở các hướng khác nhau để tránh
chùm tia đi trực tiếp qua các cơ quan lành,
hoặc 4 chùm tia đối với khối u nằm ở giữa và
sâu bên trong như trường hợp ung thư phổi,
trực tràng,…tùy thuộc vào vị trí của khối u,
hạch và yêu cầu của bác sĩ. Một số trường
hợp, số lượng lớn các trường chiếu được sử
dụng (lớn hơn 4) được tạo ra để đảm bảo cho
việc tối ưu liều tốt hơn.
Kỹ sư vật lý tiến hành tính toán liều, thu
được phân bố liều đến các cơ quan lành; khối
u và hạch, tối ưu hóa kế hoạch dựa vào quan
sát các đường đồng liều trên lát cắt, xem
đường liều chỉ định (thường là đường 95%)
có bao hết toàn bộ khối u chưa và đánh giá
biểu đồ phân bố liều – thể tích (Dose Volume
Histogram – DVH) có thỏa hai tiêu chí liều
vào khối u và liều vào cơ quan lành chưa.
Hình 1. Quy trình xạ trị theo kỹ thuật 3D-CRT

TẠP CHÍ Y HỌC VIỆT NAM TẬP 542 - THÁNG 9 - SỐ CHUYÊN ĐỀ - 2024
259
Đánh giá liều vào khối u quan tâm đến
bốn thông số sau: liều tối đa Dmax 107%
liều chỉ định, liều tối thiểu Dmin 95% liều
chỉ định, gần 100% thể tích khối u nhận được
95% liều chỉ định, yêu cầu đạt được 95% thể
tích khối u (càng gần 100% càng tốt) nhận
được 100% liều chỉ định [2]. Điều kiện đầu
tiên, liều tối đa vào khối u Dmax ≤ 107% liều
chỉ định nếu đạt được là tốt nhất, tuy nhiên
thông thường sau khi đặt các trường chiếu và
tối ưu hóa kế hoạch Dmax sẽ nằm vào khoảng
112% đến 117% liều chỉ định. Kỹ sư lập kế
hoạch sẽ phải cố gắng hạ Dmax xuống dưới
110% mà không làm ảnh hưởng quá lớn tới
liều Dmin của bướu và cơ quan lành xung
quang.
Đánh giá liều vào cơ quan lành trong xạ
trị là một phạm trù rộng lớn và các báo cáo
về giới hạn liều của cơ quan là rất nhiều
nhưng đề tài này sử dụng bảng giới hạn liều
chịu đựng cho các cơ quan lành của RTOG
[3]. Trong các cơ quan cần đánh giá, không
phải cơ quan nào cũng có tiêu chí đánh giá
như nhau mà tiêu chí đánh giá còn phụ thuộc
vào cấu trúc của cơ quan đó, chính là phụ
thuộc vào cách sắp xếp các FSU (Functional
Subunits). Một FSU như một ngăn chứa các
tế bào clonogenic của một cơ quan và thực
hiện một phần chức năng của cơ quan đó.
Trong một số mô, các FSU là rời rạc và cơ
quan vẫn có thể thực hiện chức năng của
mình khi một số FSU không thực hiện được
chức năng được nữa nên được goi là cơ quan
song song, khi đánh giá các cơ quan này ta
quan tâm đến liều trung bình (mean dose) tới
thể tích cơ quan. Trong một số mô khác, các
FSU không có ranh giới rõ ràng và có mối
quan hệ mật thiết với nhau, một phần nhỏ
trong cơ quan mất chức năng thì toàn bộ cơ
quan cũng không thực hiện chức năng mình
nữa nên được gọi là cơ quan chuỗi, khi đánh
giá cơ quan này ta quan tâm liều cực đại
(max dose) tới thể tích cơ quan [4].
Sau khi kế hoạch xạ trị được chấp nhận,
tiến hành lấy dấu kiểm tra các thông số xạ trị
và khuôn chì cá nhân của mỗi bệnh nhân phù
hợp thì tiến hành điều trị. Hệ thống máy tính
và phần mềm điều khiển máy xạ trị Cobalt-
60 phát tia điều trị mỗi ngày cho bệnh nhân.
Trong báo cáo này, chúng tôi thực hiện
một công đoạn nhỏ của công tác đảm bảo
chất lượng (QA) là tiến hành kiểm tra kết
quả liều của lập kế hoạch xạ trị thông qua đo
liều thực tế trên máy xạ Cobalt-60. Việc
đánh giá và so sánh kết quả liều trên các
phác đồ xạ trị được xem như là một phương
tiện để xác định sai số hệ thống lập kế hoạch
xạ trị (TPS). Nhằm loại trừ khả năng có xung
đột trong phần mềm, dẫn đến kết quả tính
của máy tính TPS bị sai lệch so với thực tế
xạ trị cho bệnh nhân. Chúng tôi thực hiện
kiểm tra lại kết quả liều lập kế hoạch thông
qua đo đạc liều thực tế trên phantom nước
bằng buồng ion hóa (PTW 30013-2321) và
máy ghi đo nC (Electrometer CDX2000B)
(Hình 2).

HỘI THẢO KHOA HỌC UNG BƯỚU CẦN THƠ LẦN THỨ XIII – BỆNH VIỆN UNG BƯỚU THÀNH PHỐ CẦN THƠ
260
Hình 2. Bố trí thí nghiệm đo sử dụng phantom nước, buồng ion hóa và máy ghi đo nC
Dữ liệu chụp CT-scaner phantom nước
được thiết lập trên phần mềm lập kế hoạch
Eclipse. Dựa trên kế hoạch xạ trị bệnh nhân
đã có sẵn, thực hiện chuyển đổi các kế hoạch
này trên phantom nước, tính toán liều trên hệ
thống lập kế hoạch điều trị xạ trị để có được
các giá trị liều tại điểm tham chiếu và thu
được thời gian (phút) mỗi trường chiếu xạ,
thực hiện đo liều trực tiếp trên máy xạ
Cobalt-60 để so sánh liều trên hệ thống lập
kế hoạch xạ trị, đo liều hiệu chuẩn (dựa trên
đơn vị điện tích nC) trong 2,94 phút/100cGy,
cho kích thước trường chiếu chuẩn 10x10cm,
nguồn da 75cm, độ sâu 5cm. Từ đó, tính toán
độ lệch tương đối giữa giá trị liều:
aX100%
X
−
=
(1), trong đó X là giá trị liều
theo đo thực tế và a là giá trị liều điểm tham
chiếu bằng phần mềm Eclipse. ICRU khuyến
nghị độ chính xác theo của việc kiểm tra liều
vào bướu là ± 5% [2],[6].


























