pha vµ x¸c ®Þnh nång ®é dung dÞch edta 0,05M
môc tiªu
1. Tr×nh bµy ®−îc nguyªn t¾c vµ ph¶n øng ®Þnh l−îng EDTA.
2. TÝnh ®−îc khèi l−îng kÏm ®Ó pha dung dÞch kÏm sulfat 0,05 M vµ pha ®−îc 100
mL dung dÞch kÏm sulfat 0,05 M.
3. X¸c ®Þnh ®−îc nång ®é dung dÞch EDTA 0,05 M.
1. dông cô - hãa chÊt
−
C©n ph©n tÝch
−
Buret
−
Pipet chÝnh x¸c dung tÝch 10 mL
−
B×nh nãn dung tÝch 100 mL
−
Cèc cã má
−
PhÔu thñy tinh
−
§òa thñy tinh
−
Cèc ch©n
−
èng ®ong dung tÝch 10 mL
−
ChÊt gèc kÏm (Zn)
−
Dung dÞch acid sufuric 10%
−
Dung dÞch ®Öm amoniac
−
Hçn hîp chØ thÞ ®en eriocrom T
2. pha dung dÞch complexon iii 0,05M
−
Complexon III (trilon B) lµ dinatri dihydro ethylen diamin
tetraacetat. Complexon III th−êng ë d¹ng ngËm n−íc vµ cã c«ng thøc
hãa häc lµ C10H14N2O8Na2.2H2O viÕt t¾t lµ EDTA. Complexon III cã
khèi l−îng ph©n tö lµ 372,2.
277

−
Complexon III ë d¹ng tinh thÓ kh«ng mµu, dÔ tan trong n−íc.
−
Complexon III kh«ng tháa m·n tiªu chuÈn chÊt gèc v×
C10H14N2O8Na2.2H2O dÔ mÊt n−íc kÕt tinh nªn thµnh phÇn kh«ng øng
®óng víi c«ng thøc. Ta chØ cã thÓ pha dung dÞch EDTA nång ®é xÊp xØ
0,05M tõ C10H14N2O8Na2.2H2O. Nång ®é dung dÞch EDTA sau khi pha,
®−îc x¸c ®Þnh b»ng mét dung dÞch chuÈn kh¸c ®· biÕt nång ®é.
−
L−îng C10H14N2O8Na2.2H2O cÇn thiÕt ®Ó pha 100 mL dung dÞch EDTA
cã nång ®é xÊp xØ 0,05M ®−îc tÝnh nh− sau:
−
Sè gam C10H14N2O8Na2.2H2O cÇn c©n lµ:
(g)1,861
1000
100372,20,05
1000
VMC
mM=
××
=
×
×
=
TiÕn hµnh pha dung dÞch EDTA 0,05M:
−
C©n kho¶ng 1,86 g C10H14N2O8Na2.2H2O trªn c©n kü thuËt vµ chuyÓn
vµo cèc ch©n.
−
Thªm vµo cèc ch©n kho¶ng 50 mL n−íc cÊt vµ dïng ®òa thñy tinh
khuÊy cho c¸c tinh thÓ tan hÕt.
−
Thªm n−íc cÊt vµo cèc ch©n võa ®ñ 100 mL. KhuÊy ®Òu.
3. nguyªn t¾c ®Þnh l−îng complexon
Dùa vµo ph¶n øng t¹o phøc gi÷a EDTA vµ kim lo¹i trong m«i tr−êng
®Öm pH 9. Lóc ®Çu dung dÞch cã mµu ®á vang do ph¶n øng cña Mg2+ víi chØ
thÞ (Hind2− ):
Zn2+ + Hind2− ZnInd− + H+
(§á vang )
Khi nhá EDTA (HY3− ) xuèng, Mg2+ tù do sÏ ph¶n øng tr−íc:
Zn2+ + HY3− ZnY2− + H+
Lóc Êy mµu cña dung dÞch vÉn kh«ng bÞ biÕn ®æi. GÇn ®iÓm t−¬ng
®−¬ng, ta cã sù c¹nh tranh t¹o phøc:
HY3− + ZnInd− ZnY2− + Hind2−
(§á vang ) (Xanh)
KÕt thóc chuÈn ®é khi mµu chuyÓn tõ tÝm sang xanh t−¬i hoµn toµn
(mµu cña chØ thÞ ë d¹ng tù do).
278

4. ®Þnh l−îng dung dÞch EDTA 0,05 M
4.1. Pha dung dÞch gèc kÏm sulfat 0,05 M
−
KÏm h¹t (Zn) tinh khiÕt tháa m·n yªu cÇu cña mét chÊt gèc.
−
Khèi l−îng ph©n tö l−îng cña Zn b»ng 65,37.
−
L−îng Zn cÇn thiÕt ®Ó pha 100 mL dung dÞch ZnSO4 cã nång ®é chÝnh
x¸c 0,05M lµ: (g)0,32685
1000
10065,370,05
1000
VMC
mM=
××
=
×
×
=
TiÕn hµnh pha 100 mL dung dÞch ZnSO4 0,05 M nh− sau:
−
C©n chÝnh x¸c kho¶ng 0,32 g Zn vµo cèc cã má.
−
Thªm vµo Zn trong cèc kho¶ng 5 mL dung dÞch H2SO4 10%. L¾c cho
tan hoµn toµn. Thªm vµo ®ã kho¶ng 20 mL n−íc cÊt.
−
ChuyÓn dung dÞch ë cèc cã má sang b×nh ®Þnh møc dung tÝch 100 mL
qua phÔu.
−
Tr¸ng cèc vµ phÔu nhiÒu lÇn b»ng n−íc cÊt (kho¶ng 50 mL). Bá phÔu ra.
−
Thªm n−íc võa ®ñ ®Õn v¹ch. L¾c ®Òu.
TÝnh nång ®é thùc (CM,th) cña dung dÞch ZnSO4 pha ®−îc:
0,05
m
m
C
LT
TH
tM, ×=
h
Trong ®ã:
- mTH lµ khèi l−îng, tÝnh b»ng g, cña Zn c©n ®−îc
- mLT lµ khèi l−îng, tÝnh b»ng g, cña Zn võa ®ñ ®Ó pha ®−îc 100,0 mL
dung dÞch ZnSO4 nång ®é chÝnh x¸c 0,05M (mLT = 0,32685 g).
4.2. TiÕn hµnh ®Þnh l−îng
−
LÊy chÝnh x¸c 10,00 mL dung dÞch ZnSO4 ®· pha cho vµo b×nh nãn
s¹ch. Thªm vµo ®ã 5 mL dung dÞch ®Öm amoniac, kho¶ng 0,1 g hçn
hîp chØ thÞ ®en eriocrom T vµ 30 mL n−íc cÊt. L¾c cho tan hÕt chØ thÞ.
−
Dïng phÔu rãt dung dÞch (tõ cèc cã má) kho¶ng 10 - 15 mL dung dÞch
EDTA lªn trªn buret ®Ó tr¸ng buret (lµm 2 lÇn). Cho ®Çy dung dÞch
EDTA lªn trªn buret vµ ®iÒu chØnh khãa buret ®−îc dung dÞch ®Õn
v¹ch 0.
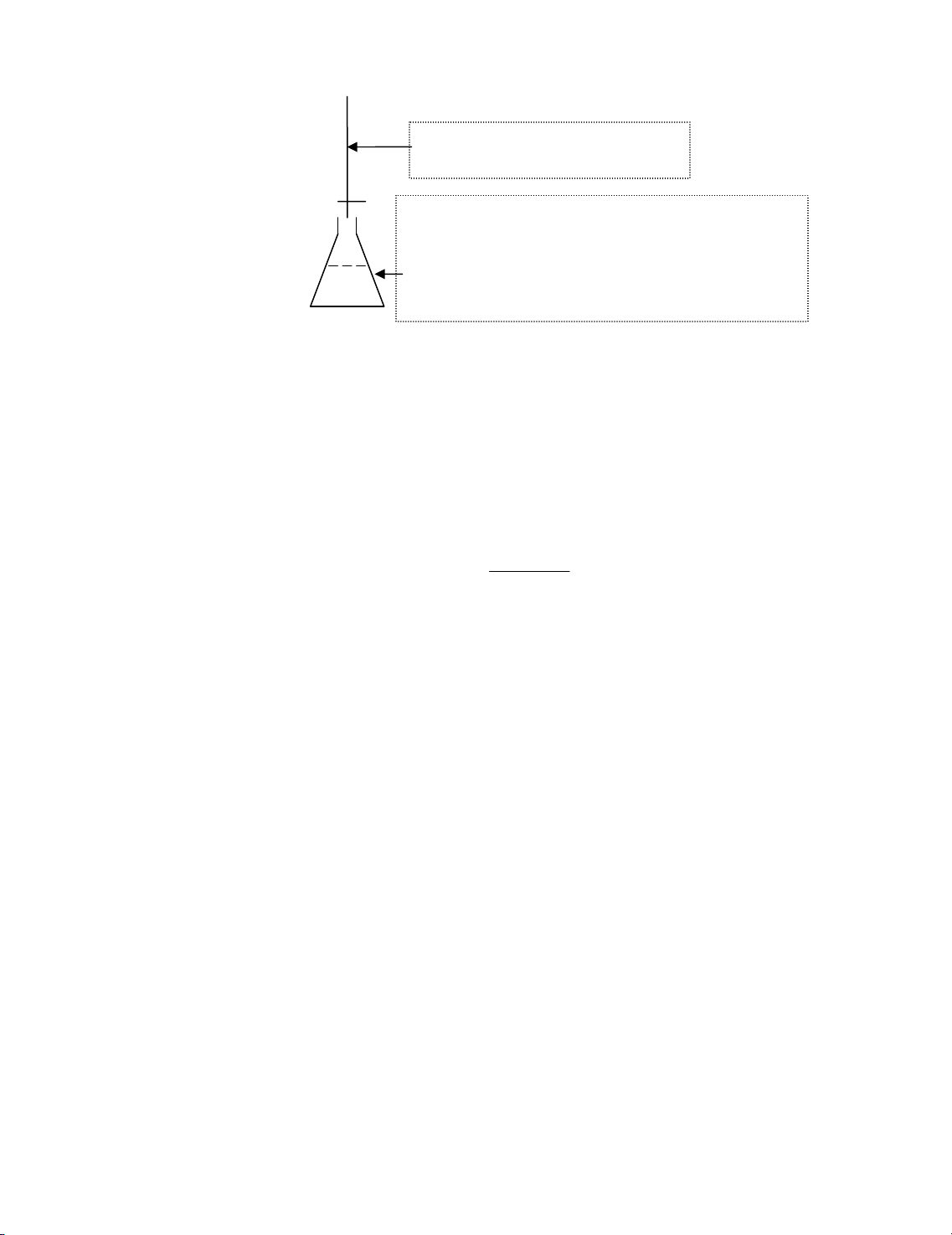
Bè trÝ thÝ nghiÖm ®−îc tr×nh bµy ë h×nh 13.1.
279
Error!
H×nh 13.1. Bè trÝ thÝ nghiÖm chuÈn ®é dung dÞch EDTA 0,05 M
Dung dÞch EDTA 0,05M
10,00 mL dung dÞch ZnSO4 ,
Dung dÞch ®Öm amoniac 5 mL ,
Hçn hîp chØ thÞ ®en eriocrom T 0,1g N−íc cÊt 30 mL
TiÕn hµnh chuÈn ®é: Mét tay ®iÒu chØnh khãa buret cho dung dÞch
EDTA tõ buret xuèng b×nh nãn, tay kia l¾c b×nh nãn. ChuÈn ®é tíi khi
dung dÞch ë b×nh nãn chuyÓn tõ mµu ®á vang sang mµu xanh t−¬i hoµn
toµn (kh«ng cßn ¸nh tÝm). Ghi thÓ tÝch dung dÞch EDTA ®· dïng.
4.3. TÝnh kÕt qu¶
Nång ®é mol/ L (CM,A) cña dung dÞch EDTA ®−îc tÝnh theo c«ng thøc sau:
A
BBM,
AM, V
VC
C
×
=
Trong ®ã:
−
VB lµ thÓ tÝch dung dÞch gèc ZnSO4, tÝnh b»ng mL, (VB = 10,00 mL)
−
CM,B lµ nång ®é mol/ L cña dung dÞch ZnSO4, (CM,B = CM,th)
−
VA lµ thÓ tÝch dung dÞch EDTA, tÝnh b»ng mL, ®· dïng chuÈn ®é.
Bµi tËp (bµi 13)
13.1. Pha ®óng kü thuËt 100 mL dung dÞch EDTA 0,05M vµ 100,0 mL
dung dÞch gèc ZnSO4 0,05M.
13.2. Tr×nh bµy nguyªn t¾c ®Þnh l−îng b»ng ph−¬ng ph¸p complexon.
13.3. Tr×nh bµy c¸ch tiÕn hµnh ®Þnh l−îng dung dÞch EDTA 0,05 M
dïng dung dÞch gèc ZnSO4 0,05 M.
13.4. ThiÕt lËp c«ng thøc tÝnh nång ®é mol/L (CM,A) cña dung dÞch EDTA.
13.5. M« t¶ sù chuyÓn mµu cña dung dÞch trong ®Þnh l−îng (b×nh nãn)
trong qu¸ tr×nh chuÈn ®é x¸c ®Þnh nång ®é dung dÞch EDTA ë
môc 4.2.
13.6. TÝnh nång ®é CM cña dung dÞch EDTA, biÕt khi chuÈn ®é
10,00 mL dung dÞch ZnSO4 0,0525 M trong m«i tr−êng ®Öm
amoniac hÕt 10,55 mL dung dÞch EDTA.
280

PhÇn phô lôc
Phô lôc 1. Dông cô th«ng th−êng b»ng sø, thuû tinh vµ mét
sè m¸y th«ng dông dïng trong ho¸ ph©n tÝch
H×nh 1. PipÐt ®iÖn tö H×nh 2. PipÐt ®Þnh møc H×nh 3
H×nh 4. C¸c lo¹i gi¸ ®ì PipÐt
H×nh 5. Qu¶ bãp cao su H×nh 6. C¸c lo¹i èng trong ®Þnh møc
dïng ®Ó nèi pipÐt
281













![Bài giảng Hoá kỹ thuật môi trường 2 - Đại học Xây dựng Miền Tây [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260512/hoatulip0906/135x160/59431778724718.jpg)










![Giáo trình Tài nguyên năng lượng và bảo vệ môi trường - Trường CĐ Cơ điện Hà Nội [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260323/lionelmessi01/135x160/8121774378783.jpg)
![Đề cương bài giảng Kỹ thuật xử lý môi trường - Trường Cao đẳng Cơ điện Hà Nội [Chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260323/lionelmessi01/135x160/75051774429892.jpg)
