SIÊU AXÍT & SIÊU BAZƠ
1 . SIÊU AXÍT có thể định nghĩa như một axít với độ axít lớn hơn của axít sulfuric nồng
độ 100%.
Một số siêu axít đơn giản bao gồm axít triflorometansulfonic (CF3SO3H), còn gọi là axít
triflic, và axít florosulfuric (FSO3H), cả hai axít này có độ axít hàng nghìn lần mạnh hơn
axít sulfuric. Trong nhiều trường hợp, siêu axít không phải là một hợp chất đơn, mà là
một hệ của nhiều hợp chất liên kết với nhau để tạo ra độ axít cao.
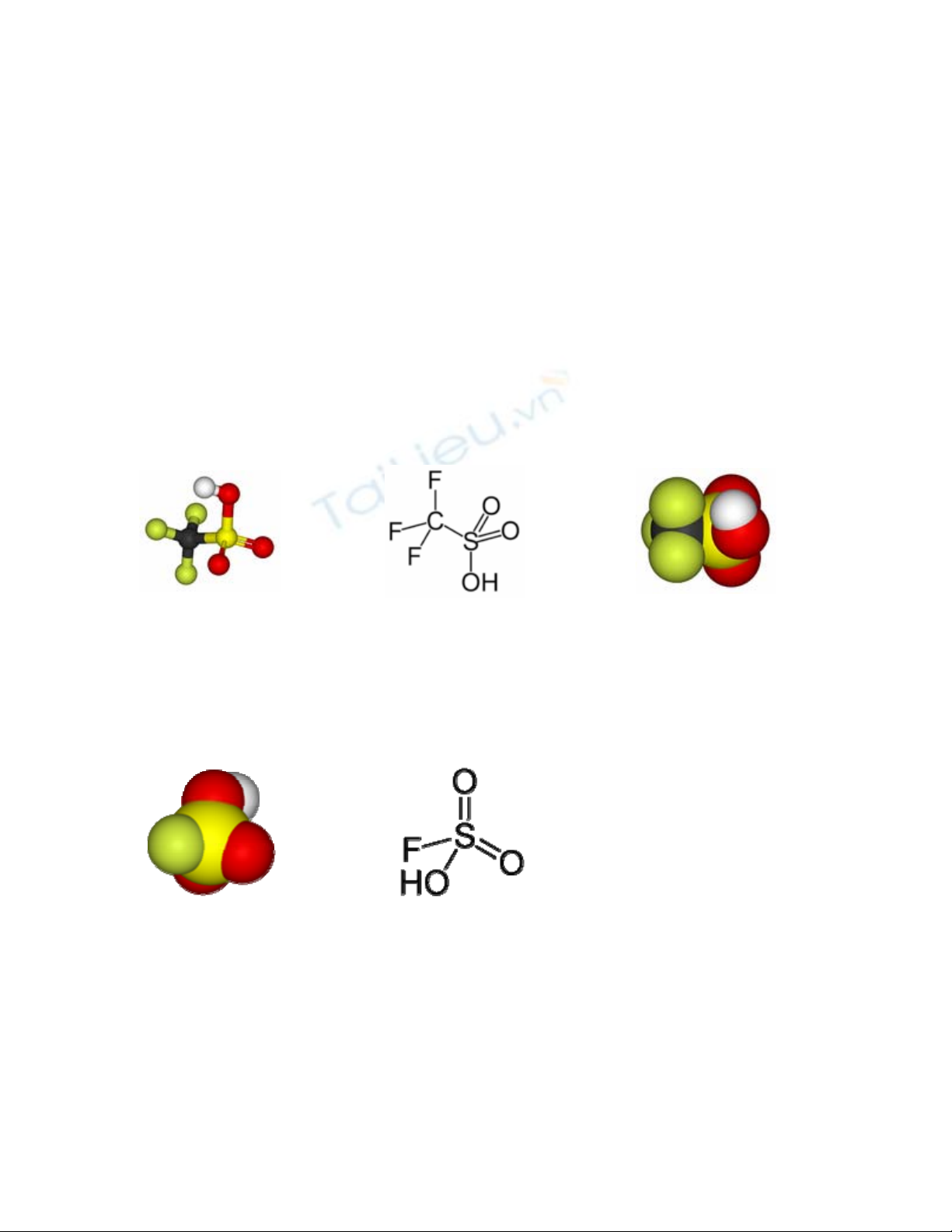
Cấu trúc phân tử axít
triflorometansulfonic
Công thức cấu tạo axít
triflorometansulfonic
axít
triflorometansulfonic
Cấu trúc phân tử axít florosulfuric
Công thức cấu tạo axít florosulfuric
Thuật ngữ "siêu axít" nguyên thủy được tạo ra bởi James Bryant Conant năm 1927 trong
phân loại các axít mà chúng mạnh hơn các axít vô cơ thông thường. George A. Olah đoạt

giải Nobel năm 1994 về hóa học [1] vì các nghiên cứu của ông về các siêu axít và công
dụng của chúng trong các theo dõi trực tiếp về cacbocation.
"Axít ma thuật" của Olah là tên gọi do khả năng kỳ diệu của chúng để hòa tan sáp nến.
Axít ma thuật là hỗn hợp của axít Lewis pentaflorua antimon (SbF5) và axít florosulfuric
(axít Bronsted). Hệ siêu axít mạnh nhất đã biết, gọi là axít floroantimonic, là hỗn hợp của
axít flohiđric và pentaflorua antimon. Trong hệ này, axít flohiđric giải phóng proton (H+),
và gốc bazơ liên hợp (F-) bị cô lập một cách có hiệu quả bằng cách tạo ra một liên kết
phối hợp rất mạnh với pentaflorua antimon. Kết quả của liên kết này là anion vô cơ lớn
(SbF6-), đây là một nucleophil rất yếu và là bazơ rất yếu.
2 . SIÊU BAZƠ
Trong hóa học, một siêu bazơ là một bazơ cực mạnh. Hiện nay vẫn chưa có tiêu chuẩn
được chấp nhận chung cho "mạnh hơn cái gì?" mặc dù phần lớn các nhà hóa học thường
xuyên coi hyđroxit natri như là bazơ 'điểm chuẩn' của họ giống như họ sử dụng axít
sulfuric làm axít 'điểm chuẩn' (xem siêu axít). Ion hyđroxit là một điểm chuẩn tốt, do nó
là bazơ mạnh nhất có thể tồn tại trong dung dịch nước; các bazơ mạnh hơn sẽ trung hòa
nước như là một axít bằng cách khử proton của nó, để sinh ra hyđroxit (và siêu bazơ
proton hóa). Một thói quen thông thường khác có thể định nghĩa siêu bazơ là khử α
proton lượng pháp của hợp chất cacbonyl thành dạng enol, một điều không thể thực hiện
được bằng các "bazơ thông thường". Mặc cho điều này, nhưng thuật ngữ vẫn chưa có
định nghĩa hóa học tiêu chuẩn, vì thế 1,8-Bis(dimetylamino)naphtalen có thể được gọi là
"siêu bazơ".
Proton Sponge 1,8-Bis(dimethylamino)naphthalene

Phân loại
Có ba lớp chính các siêu bazơ: hữu cơ, kim loại hữu cơ và vô cơ.
Trong tổng hợp hữu cơ, bazơ Lochmann-Schlosser, tổ hợp của n-butyl liti (C4H9Li) và
tert-butôxít kali ((CH3)3COK), nói chung được coi là một siêu bazơ. Trong tổ hợp này
của các tác nhân thì muối rượu bậc ba này của kali kết hợp mạnh với ion liti của tổ hợp,
giải phóng butyl (C4H9) ra khỏi sự kết hợp chặt chẽ của nó với ion kim loại (Li). Những
hệ thống như thế được gọi chung là các bazơ lao móc, do tác động của chúng tựa như các
lao móc trong thực tế.
Các siêu bazơ vô cơ thông thường là các muối với các ion âm nhỏ, điện tích cao, chẳng
hạn nitrua liti, có mật độ điện tích âm cực cao và vì thế nó thu hút rất mạnh các ion
hiđrôni (H3O+).


![Lý thuyết và bài tập Hóa học lớp 12 năm 2022 (KHXH) - Trường THPT Đào Sơn Tây [Tổng hợp]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230310/phuogchi205/135x160/2351678432530.jpg)

![Lý thuyết và bài tập Hóa học lớp 12 (KHTN) năm 2021 - Trường THPT Đào Sơn Tây [Đầy đủ]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230310/phuogchi205/135x160/491678432840.jpg)





















