
1
1
81
81
THUYEÁT LIEÂN KEÁT HOÙA TRÒ
Valence Bond Theory

2
2
82
82
Cấu trúc Lewis và mô hình VSEPR không giải thích
được sựhình thành nối.
Bằng cách nào để diễn tảhình dạng phân tửtheo các số
hạng của cơ học lượng tử?
Các vân đạo (orbital) có liên quan đến liên kết?
Sửdụng lý thuyết liên kết hóa trị(VB)
Liên kết được hình thành từsựxen phủ(overlap) của
các vân đạo hoá trịnguyên tửtham gia dùng chung
đôi electron.
Có 2 electron có spin ngược chiều nhau trong vân
đạo xen phủ.
Xen phủcàng nhiều, liên kết càng mạnh.
82
82
3
3
83
83
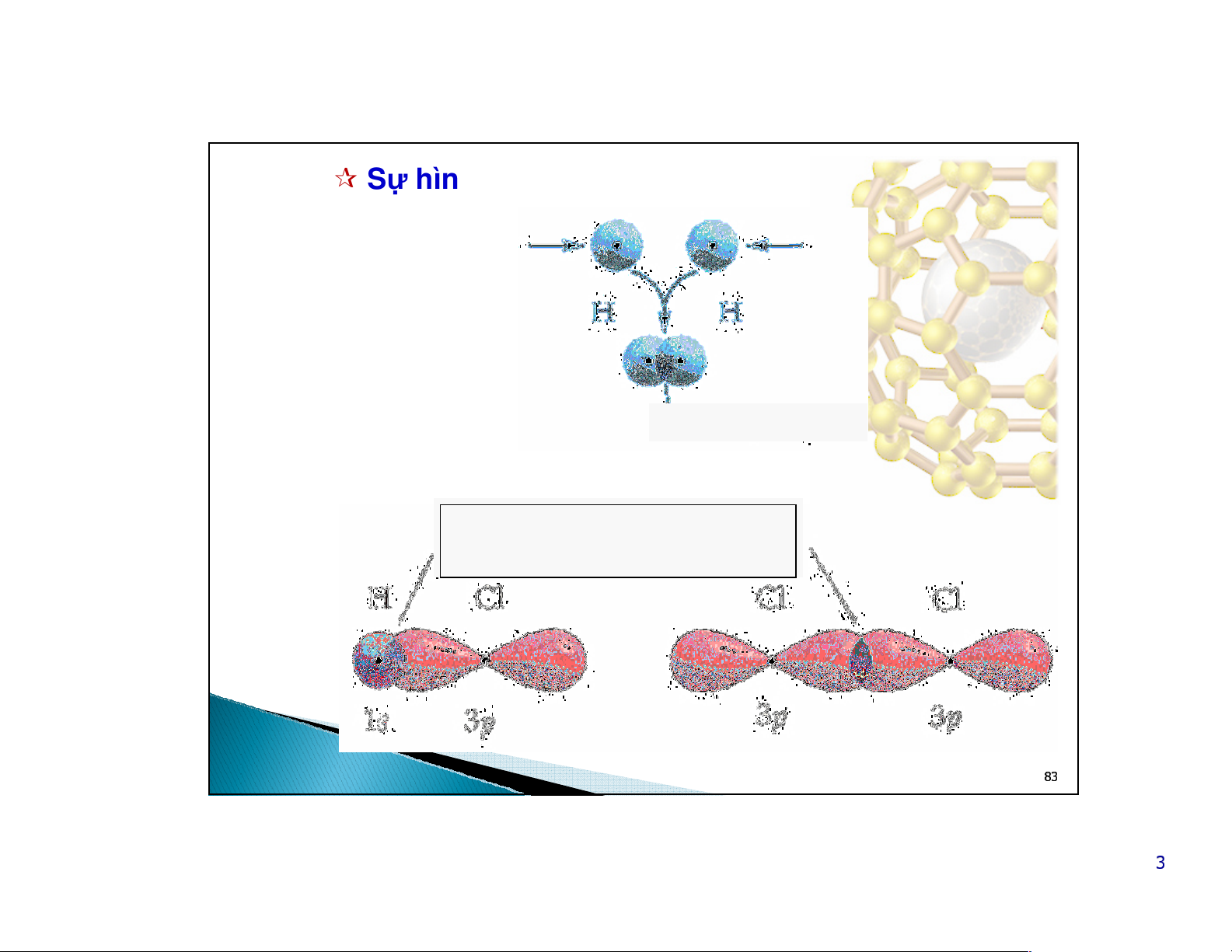
Sựhình thành phân tửH2
(1s1) (1s1)
Vùng xen phủ
Sựhình thành phân tửHCl và Cl2
Vùng xen phủ
83
83

4
4
84
84
Điều kiện tạo liên kết cộng hóa trịtheo VB
- 2 nguyên tửtạo liên kết phải ởkhá gần nhau sựxen phủcủa
các AO
- Có 2 electron trong vùng xen phủ
- Điều kiện để các AO xen phủnhau:
- Các AO phải có năng lượng xấp xỉ nhau (đồng năng)
- Các AO cùng dấu trong vùng xen phủ
- Hướng xen phủthích hợp xen phủcực đại

5
5
85
85
Caùc luaän ñieåm cô baûn cuûa thuyeát VB
Lieân keát coäng hoùa trò ñöôïc hình thaønh do söï gheùp
ñoâi 2 electron coù spin ñoái song khi coù söï xen phuû
cuûa 2 vaân ñaïo nguyeân töû.
Möùc ñoä xen phuû caøng lôùn thì lieân keát caøng beàn





![Tập bài giảng Hoá học đại cương 1 - Đăng Thị Thu Huyền [Full, Chi Tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260312/hoabattu2026/135x160/11351773633935.jpg)



![Bài giảng Hoá học đại cương Trường Đại học Nam Cần Thơ [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260310/hoaphuong0906/135x160/53091773287379.jpg)
















