
HồThịCẩm Hòai, PhD
htchoai@hcmus.edu.vn

Nhiệt động hóa học nghiên cứu những biến đổi vật lý và hóa
học của vật chất về phương diện trao đổi năng lượng.
NĐHH có thể giải quyết những vấn đề như:
Khi hóa chất được trộn chung lại, chúng có thể cho phản
ứng hóa học hay không?
Nếu có thì phản ứng sẽ kèm theo sự phóng thích hay thu
nhiệt?
Phản ứng xảy ra trọn vẹn hay chỉ có một phần. Nếu xảy ra
một phần thì thành phần hóa chất như thế nào khi phản ứng
có thể xem như ngừng lại.Thành phần ấy có thể thay đổi
trong điều kiện thí nghiệm nào?
Sự phát triển và duy trì cơ thể sống xảy ra được như thế
nào?
Nhắc lại một số định nghĩa cần thiết
Hệ thống: Bất cứ phần nào của vũ trụ có
giới hạn thường thấy được trong phạm vi
hóa học đang được khảo sát về phương
diện trao đổi năng lượng. Phần còn lại của
vũ trụ hợp thành môi trường ngòai đối với
hệ thống
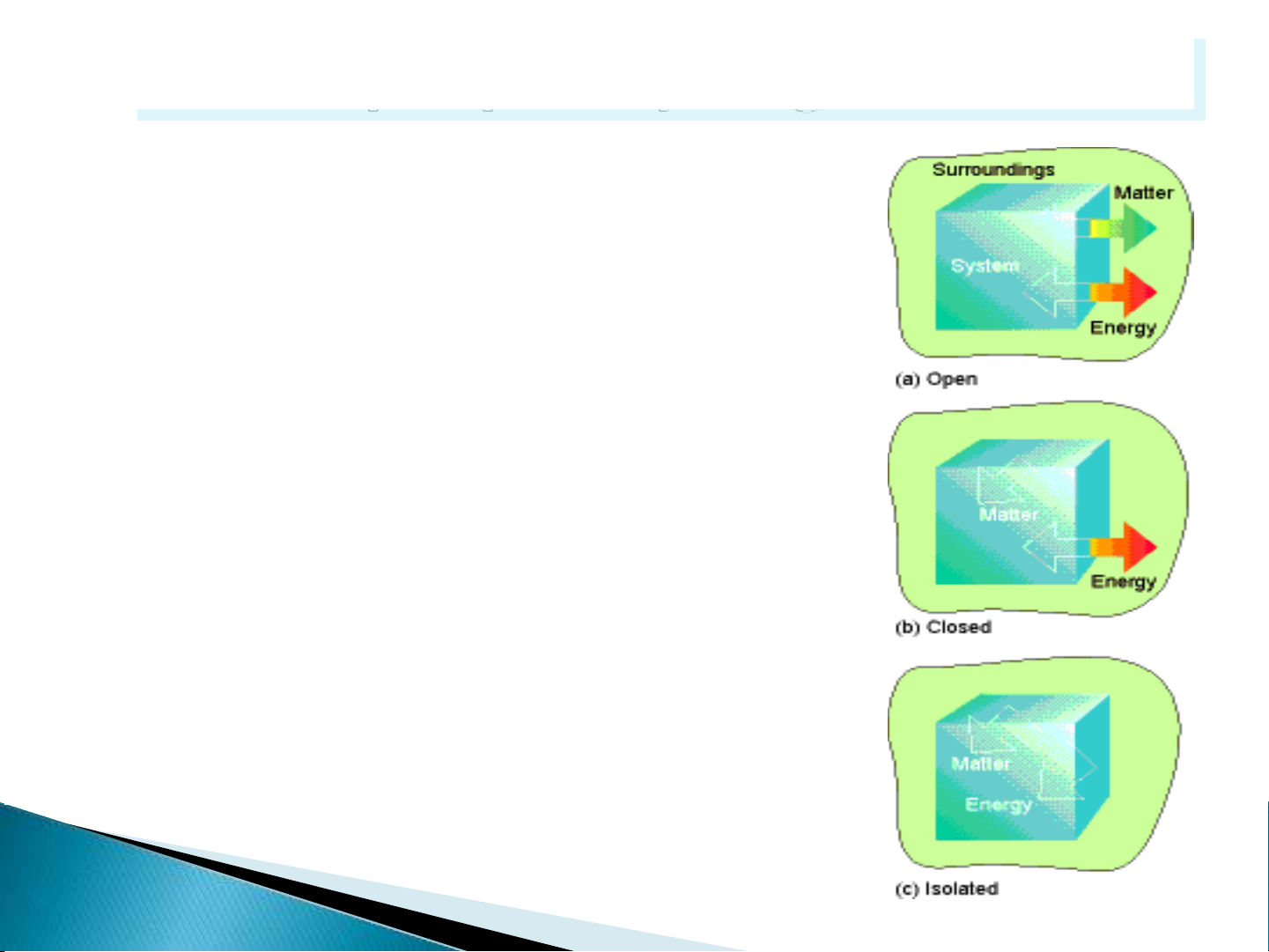
Hệ thống hở là hệ thống có thể trao đổi
vừa năng lượng vừa vật chất với môi
trường ngòai.
Hệ thống kín là hệ thống chỉ có thể trao
đổi năng lượng với môi trường ngòai.
Hệ thống cô lập không trao đổi năng
lượng cũng như vật chất với môi trường
ngòai.

Nhắc lại một số định nghĩa cần thiết
Trạng thái:
Nếu hệ thống cân bằng, bất cứ điểm nào trong hê thống đềucó đặc
tính giống nhau. Hê thống ấy có thể được xác định bằng một số
thuộc tính độc lập đối với nhau.
Ta nói một hệ thống có một trạng thái xác định.
Các thuộc tính độc lập để xác định một hệ thống là những biến số
trạng thái.
Những thuộc tính còn lại phụ thuộc vào các thuộc tính độc lập được
gọi là những hàm số trạng thái.
Trạng thái của một hệ thống có thể biến đổi và biến đổi ấy được xác
định nếu biết rõ trạng thái đầu và trạng thái cuối của hệ thống.
Đường biến đổi cũng được xác định nếu biết rõ trạng thái đầu và
trạng thái cuối và tất cả các những trạng thái trung gian mà hệ thống
trải qua.

Nhắc lại một số định nghĩa cần thiết
Biến đổi được gọi là thuận nghịch khi biến đổi ấy và biến đổi
ngược lại có thể thực hiện dễ dàng khi có sư thay đổi rất nhỏ điều
kiên thí nghiệm (nước đá nóng chảy ở zero độ C)
Biến đổi tự nhiên hay bất thuận nghịch chỉ có thể xảy ra theo 1
chiều, biến đổi ngược lại không thể thực hiện tự nhiên được (sự
truyền nhiệt từ đầu nóng đến đầu lạnh của một thanh kim lọai).
Biến đổi đẳng nhiệt (dT = 0)
Biến đổi đọan nhiệt (dq = 0)
Biến đổi đẳng áp (dp = 0)
Biến đổi đẳng tích (dV = 0)




![Bài giảng Hóa lý thực phẩm [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250716/kimphuong1001/135x160/849_bai-giang-hoa-ly-thuc-pham.jpg)
![Câu hỏi ôn tập Hóa lý [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250709/kimphuong1001/135x160/51111752043440.jpg)
![Bài giảng Hóa lý 1: Tổng hợp kiến thức [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250704/tiepnguyen438@gmail.com/135x160/6631751621117.jpg)




![Bài giảng Vật lý đại cương Chương 4 Học viện Kỹ thuật mật mã [Chuẩn SEO]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250925/kimphuong1001/135x160/46461758790667.jpg)














