
1
bé gi¸o dôc vµ ®µo t¹o
-------------------------
®Ò CHÝNH THøC
§¸p ¸n – thang ®iÓm
®Ò thi tuyÓn sinh §¹i häc, Cao ®¼ng n¨m 2004
----------------------------
M«n: hãa häc, Khèi b
(§¸p ¸n - Thang ®iÓm cã 6 trang)
C©u ý Néi dung §iÓm
I
1,50
1. CÊu h×nh electron vµ vÞ trÝ cña Ca vµ Cl (0,75 ®iÓm)
Cl (Z = 17): 1s22s22p63s23p5
Ca (Z = 20): 1s22s22p63s23p64s2
0,25
Cl : Chu kú 3, ph©n nhãm chÝnh, nhãm VII
Ca : Chu kú 4, ph©n nhãm chÝnh, nhãm II
0,25
Liªn kÕt trong CaCl2 thuéc lo¹i liªn kÕt ion.
V× Ca lµ kim lo¹i ®iÓn h×nh, Cl lµ phi kim ®iÓn h×nh
0,25
2. HiÖn t−îng vµ ph¶n øng gi÷a HCl vµ Na2CO3 (0,75 ®iÓm )
a. Lóc ®Çu kh«ng thÊy khÝ bay ra do chØ cã ph¶n øng:
HCl + Na2CO3 = NaHCO3 + NaCl
0,25
Sau ®ã thÊy cã bät khÝ tho¸t ra, v× toµn bé Na2CO3 ®· chuyÓn hÕt thµnh
NaHCO3 vµ cã ph¶n øng:
HCl + NaHCO3 = CO2↑ + H2O + NaCl
Cuèi cïng nÕu thªm tiÕp HCl th× kh«ng thÊy khÝ tho¸t ra, do NaHCO3 ®· ph¶n
øng hÕt.
0,25
b. V× HCl d− nªn cã ngay bät khÝ tho¸t ra tõ dung dÞch:
2 HCl + Na2CO3 = CO2↑+ H2O + 2NaCl
0,25
II 1,50
1. Ph¶n øng cña alanin (0,75 ®iÓm)
++H2O
+HCl
CH3CHCOOH
NH2
CH3CHCOONa
NH2
CH3CHCOOH
NH2
CH3CHCOOH
NH3Cl
NaOH
CH3CHCOOH
NH2
+CH3CHCOOCH3
NH2
+H2O
CH3OH
HCl
0,25
0,25
0,25
2. S¬ ®å biÕn hãa (0,75 ®iÓm)
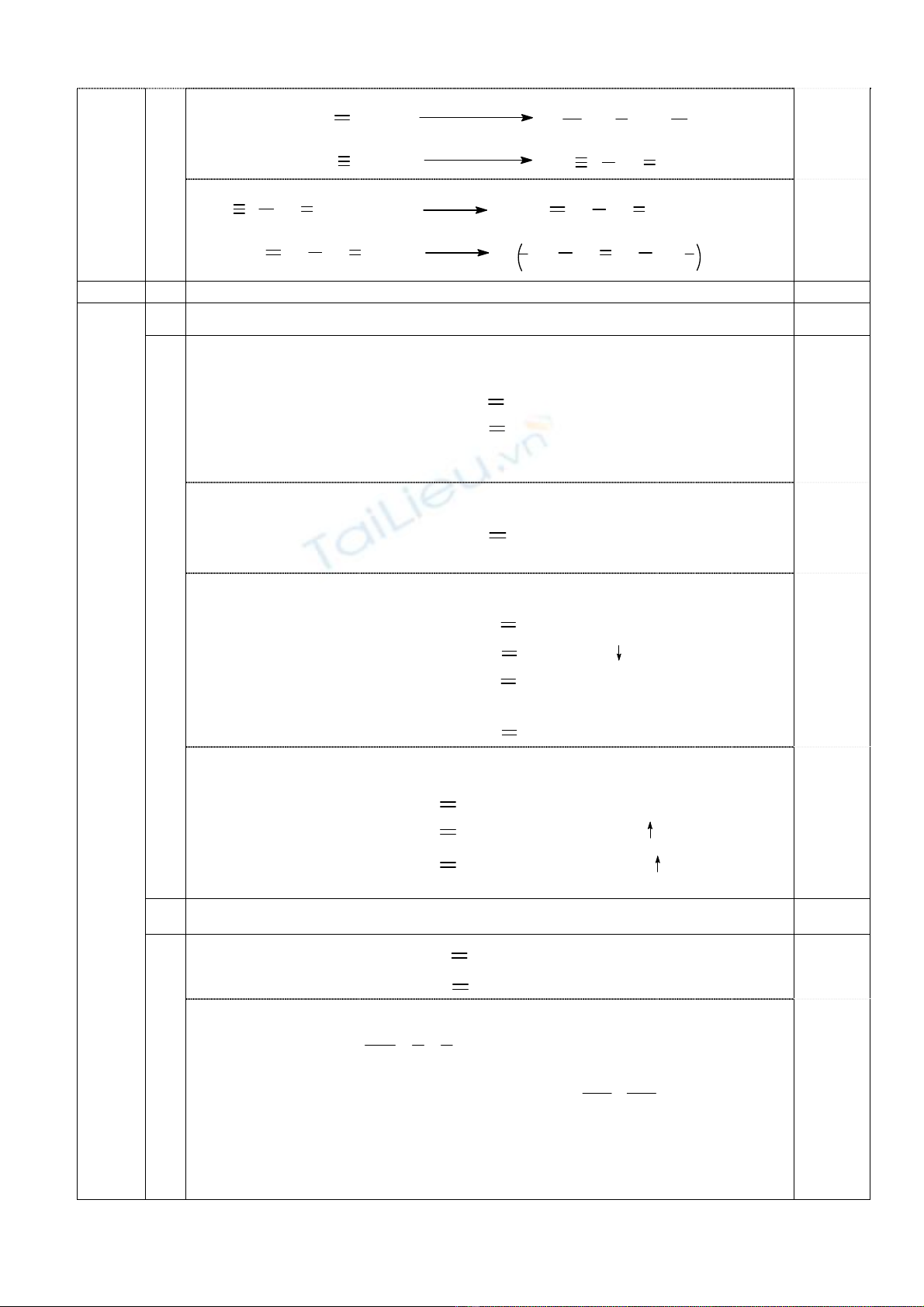
2 CH4
1500oCCH CH + 3 H2(1)
(2)
CH CH + HCl CH2CHCl
xt
0,25
2
(3
)
CH2CHCl
nto, p, xt (CH2CHCl )
(4)
CH CH
2CuCl, NH4Cl CH C CH CH2
n
0,25
(5)
CH C CH CH2+H2Pd CH2CH CH CH2
(6)
CH2CH CH CH2
nto , p, xt
, to
CH2CH CH CH2n
0,25
III 1,50
1. C¸c ph−¬ng tr×nh ph¶n øng (1,00 ®iÓm)
Cho CO qua A nung nãng:
Fe3O4+4 CO 3Fe 4 CO2
+
to
CuO +CO Cu CO2
+
to
⇒ ChÊt r¾n B: Al2O3, MgO, Fe, Cu.
0,25
ChÊt r¾n B + dung dÞch NaOH d−:
Al2O32NaOH 2NaAlO2H2O
++
⇒ Dung dÞch C: NaAlO2, NaOH d−; chÊt r¾n D: MgO, Fe, Cu
0,25
Dung dÞch C + dung dÞch HCl d−:
NaAlO2+++
++
HCl Al(OH)3NaCl
H2O
Al(OH)33HCl AlCl33H2O
++
NaOH HCl NaCl H2O
HoÆc:
NaAlO2+4HCl AlCl3+2H2O
NaCl +
0,25
ChÊt r¾n D + dung dÞch HNO3 lo·ng:
+
++
MgO 2HNO3Mg(NO3)2H2O
++
Fe 4HNO3Fe(NO3)32H2ONO
+++
3Cu 8HNO33Cu(NO3)24H2O2NO
0,25
2. §iÒu chÕ Ca(H2PO4)2 ( 0,50 ®iÓm)
(1
)
(2)
++
C
a3(
P
O4)23H2SO42H3
P
O43
C
aSO4
+3Ca(H2PO4)2
Ca3(PO4)24H3PO4
0,25
Theo (1) vµ (2):
Khèi l−îng H2SO4 = 98
2
3
3
4
234
468 ××× = 392 (kg)
Khèi l−îng dung dÞch H2SO470% cÇn dïng = 80
100
70
100
392 ×× = 700 (kg )
0,25
3
IV 1,50
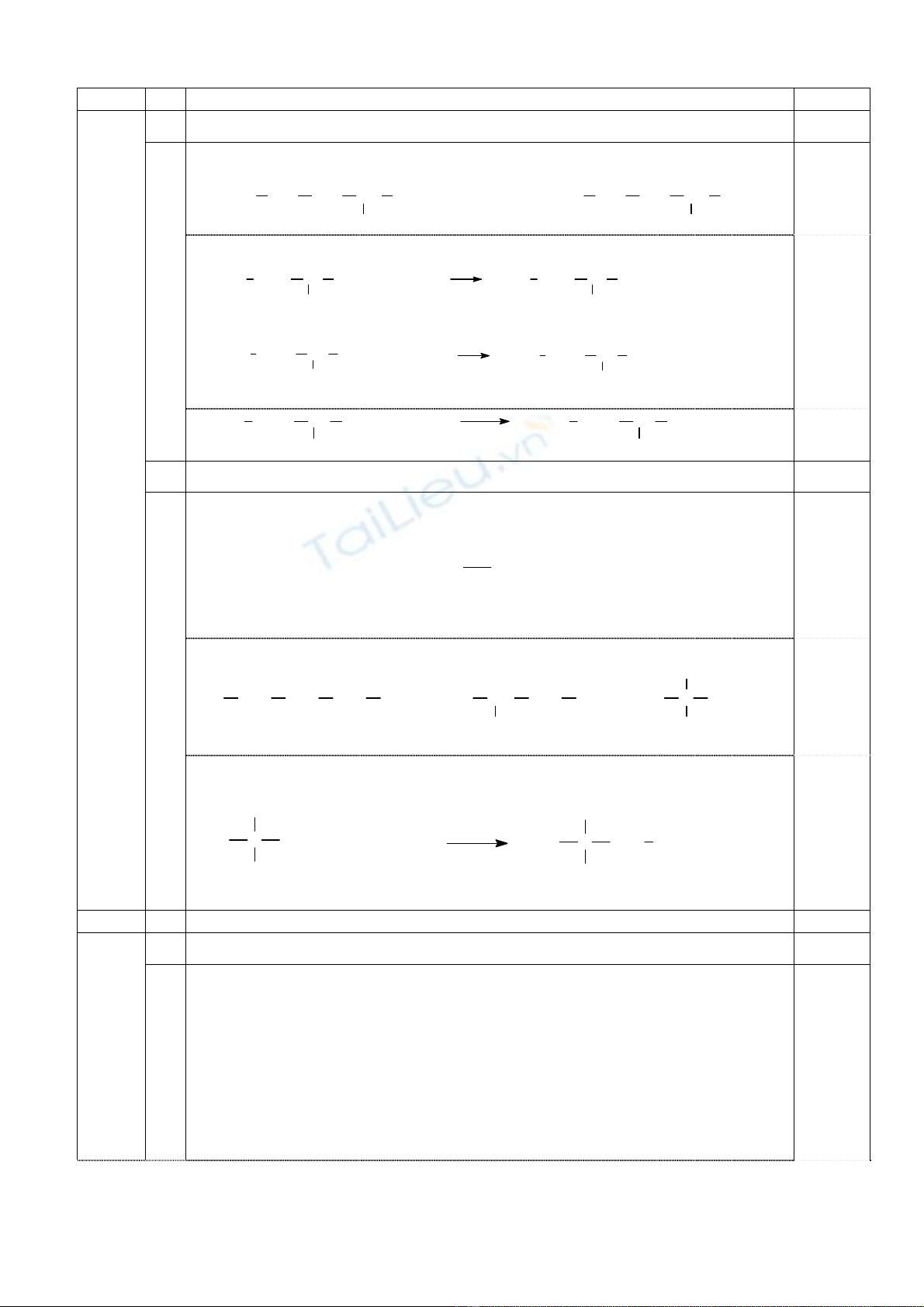
1. X¸c ®Þnh c«ng thøc cÊu t¹o cña hîp chÊt X (0,75 ®iÓm)
Theo ®iÒu kiÖn ®Ò bµi th× C8H15O4N cã hai c«ng thøc cÊu t¹o:
CH3OCO CH2CH2CH
NH2
COOC2H5C2H5OCO CH2CH2CH
NH2
COOCH3
hoÆc
0,25
C¸c ph−¬ng tr×nh ph¶n øng:
+++
2NaOH CH3OH C2H5OH
(CH2)2CH
NH2
COOC2H5
CH3OCO to
(CH2)2CH
NH2
COONa
NaOCO
HoÆc:
+++
2NaOH CH3OH C2H5OH
(CH2)2CH
NH2
COOCH3
C
2H5OCO to
(CH2)2CH
NH2
COONaNaOCO
0,25
++
(CH2)2CH
NH2
COONa
NaOCO 3HCl (CH2)2CH
NH3Cl
COOH
HOCO 2NaCl 0,25
2. X¸c ®Þnh c«ng thøc cña hi®rocacbon A ( 0,75 ®iÓm)
Ph©n tö khèi cña dÉn xuÊt brom = 15125,75 =×
Gäi c«ng thøc cña dÉn xuÊt brom lµ CxHyBrz.
12x + y + 80z = 151 ⇒ 80
151
z< mµ z nguyªn, d−¬ng ⇒ z = 1
Víi z = 1 ⇒ 12x + y + 80 = 151 ⇒ 12x + y =71 ⇒ x = 5 , y = 11.
C«ng thøc ph©n tö cña dÉn xuÊt chøa brom lµ C5H11Br.
0,25
VËy c«ng thøc ph©n tö cña hi®rocacbon A lµ C5H12, víi c¸c c«ng thøc cÊu t¹o:
CH3CH2CH2CH2CH3CH3CH CH2CH3
CH3
CH3CCH
3
CH3
CH3
,,
(1) (2) (3)
0,25
Do chØ thu ®−îc 1 dÉn xuÊt brom, nªn CTCT ®óng cña A lµ c«ng thøc (3).
CH3CCH
3
CH3
CH3
(3)
+Br
2CH3CCH
2
CH3
CH3
Br +HBr
askt
0,25
V 2,00
1 PhÇn tr¨m khèi l−îng cña hçn hîp A (1,25 ®iÓm)
Hçn hîp (Mg, Fe) + dung dÞch CuSO4:
Tr−íc hÕt, Mg ph¶n øng:
Mg + CuSO4 = MgSO4 + Cu↓ (1)
Khi Mg ph¶n øng hÕt th× Fe ph¶n øng:
Fe + CuSO4 = FeSO4 + Cu↓ (2)
V× trong dung dÞch cã 2 muèi nªn CuSO4 vµ Mg ph¶n øng hÕt, Fe ®· ph¶n
øng. Hai muèi trong dung dÞch lµ MgSO4 vµ FeSO4.
0,25

4
Dung dÞch C t¸c dông víi NaOH:
MgSO4 + 2NaOH = Mg(OH)2 ↓ + Na2SO4 (3)
FeSO4 + 2NaOH = Fe(OH)2 ↓ + Na2SO4 (4)
0,25
Nung kÕt tña:
+
to
Mg(OH)2MgO H2O
+
4 Fe(OH)2+O24 Fe(OH)3
2H2O
to
2 Fe(OH)3Fe2O3+3H
2O
Hay:
4 Fe(OH)2+O2
to
2 Fe2O3+4 H
2O
(5)
(6)
(7)
(8)
0,25
§Æt x, y, z lµ sè mol Mg, Fe ®· ph¶n øng vµ Fe cßn d− (z )0≥. Ta cã ph−¬ng
tr×nh:
m
A = 24x + 56(y+z) = 5,1 (9)
Theo c¸c ph¶n øng (1), (2): mB = 64(x+y) + 56z = 6,9 (10)
Theo c¸c ph¶n øng tõ (1) ®Õn (8):
m
D = 40x + 80y = 4,5 (11)
0,25
Gi¶i hÖ c¸c ph−¬ng tr×nh (9), (10), (11) ®−îc x = y = z = 0,0375 (mol)
Thµnh phÇn phÇn tr¨m cña c¸c kim lo¹i:
Mg: 100
1,5
240375,0 ×
× = 17,65 (%)
Fe: 100 − 17,65 = 82,35 (%)
0,25
2. Nång ®é mol/lÝt cña dung dÞch CuSO4 ( 0,25 ®iÓm)
3,0
25,0
0375,00375,0
25,0
yx
]CuSO[ 4=
+
=
+
= (mol/lÝt)
0,25
3. ThÓ tÝch khÝ SO2 ( 0,50 ®iÓm)
ChÊt r¾n B gåm Fe vµ Cu ph¶n øng víi dung dÞch H2SO4 ®Æc, nãng:
3SO2
2Fe +to
Fe2(SO4)3+6H2O
6H2SO4(®) +
0,0375 0375,0
2
3
SO2
Cu +to
CuSO4+2H2O
2H2SO4(®) +
0,075 0,075
0,25
)lÝt(94,24,22)075,00375,0
2
3
(V 2
SO =×+×= 0,25
VI 2,00
1. X¸c ®Þnh c«ng thøc c¸c chÊt cã trong hçn hîp A (1,50 ®iÓm)
Hai chÊt cã cïng mét lo¹i nhãm chøc + NaOH → 1 r−îu ®¬n chøc + 2 muèi
cña 2 axÝt ®¬n chøc, kÕ tiÕp ⇒ Hçn hîp A gåm 2 este ®¬n chøc ®−îc t¹o bëi
cïng mét r−îu ®¬n chøc vµ 2 axit ®¬n chøc ®ång ®¼ng kÕ tiÕp.
0,25

5
Gäi c«ng thøc chung cña hai este trªn lµ CxHyO2 víi sè mol hçn hîp b»ng a.
Ph−¬ng tr×nh ph¶n øng ch¸y:
CxHyO2 + )1
4
y
x( −+ O2 → xCO2 + 2
y H2O
a )1
4
y
x( −+ a ax a 2
y
Theo ®Ò bµi:
4,22
096,12
n2
O= = 0,54 (mol)
, 4,22
304,10
n2
CO = = 0,46 (mol)
0,25
Theo ®Þnh luËt b¶o toµn khèi l−îng:
OHCOOA 222 mmmm +=+
⇒ 222 COOAOH mmmm −+=
)g(48,64446,03254,044,9m OH2
=×−×+= ⇒ 18
48,6
nOH2
= = 0,36 (mol)
0,25
Theo ph¶n øng ch¸y ta cã :
46,0axn 2
CO == (1)
36,0
2
y
an OH2
== (2)
54,0)1
4
y
x(an 2
O=−+= (3)
Tõ (1), (2), (3) ⇒ a = 0,1 (mol)
Khèi l−îng mol ph©n tö trung b×nh cña A 1,0
44,9
= = 94,4 (g) ⇒ MA = 94,4 ®v.C
0,25
§Æt c«ng thøc chung cña hai este lµ RRCOO ′.
Khi cho 5,0
4,94
2,47 =(mol) hçn hîp A t¸c dông víi NaOH :
RRCOO ′ + NaOH → RCOONa + OHR′
0,5 0,5
Khèi l−îng mol ph©n tö trung b×nh cña muèi (Mmuèi):
Mmuèi = 5,0
2,38 = 76,4 (g) ⇒ R = 76,4 − 67 = 9,4
Gèc < 9,4 lµ H ⇒ gèc kÕ tiÕp lµ CH3
Hai muèi tháa m·n lµ HCOONa vµ CH3COONa.
0,25
Khèi l−îng ph©n tö trung b×nh cña hai este: MA = 94,4 = 9,4 + 44 + R'
⇒ R' = 41 lµ C3H5.
VËy c«ng thøc ph©n tö cña hai este lµ C4H6O2 vµ C5H8O2.
C«ng thøc cÊu t¹o t−¬ng øng cña hai este:
HCOOCH2CH = CH2 ; CH3COOCH2CH = CH2
0,25






















![Đề thi Tiếng Anh có đáp án [kèm lời giải chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250810/duykpmg/135x160/64731754886819.jpg)



