
Ngày nhận bài: 31-10-2024 / Ngày chấp nhận đăng bài: 31-12-2024 / Ngày đăng bài: 28-01-2025
*Tác giả liên hệ: Nguyễn Đức Tuấn. Khoa Dược, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam.
E-mail: ductuan@ump.edu.vn
© 2025 Bản quyền thuộc về Tạp chí Y học Thành phố Hồ Chí Minh.
8 https://www.duoc.tapchiyhoctphcm.vn
ISSN : 1859-1779
Nghiên cứu Dược học
Tạp chí Y học Thành phố Hồ Chí Minh - Dược học;28(1):08-21
https://doi.org/10.32895/hcjm.p.2025.01.02
Xây dựng qui trình định lượng đồng thời allopurinol
và chất chuyển hóa oxypurinol trong huyết tương người
bằng kỹ thuật HPLC-DAD
Lê Thị Thu Cúc1, Ngô Thị Minh Tâm2, Lê Minh Tài2, Nguyễn Quang3, Lương Bắc An4,
Lê Hoàng Gia Linh4, Đỗ Đức Minh4, Nguyễn Đức Tuấn5,*
1Khoa Dược-Trường Đại Học Nguyễn Tất Thành, Thành phố Hồ Chí Minh, Việt Nam
2Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam
3Trung tâm nghiên cứu bệnh gout và mạn tính Việt Pháp, Thành phố Hồ Chí Minh, Việt Nam
4Trung tâm Y sinh học phân tử, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam
5Khoa Dược, Đại học Y Dược Thành phố Hồ Chí Minh, Thành phố Hồ Chí Minh, Việt Nam
Tóm tắt
Đặt vấn đề: Allopurinol (ALO) là thuốc thuộc nhóm ức chế tổng hợp acid uric, sau khi hấp thu vào cơ thể được chuyển
hóa phần lớn thành chất chuyển hóa có hoạt tính là oxypurinol (OXY).
Mục tiêu nghiên cứu: Xây dựng quy trình định lượng đồng thời ALO và chất chuyển hóa OXY trong huyết tương người
bằng HPLC-DAD.
Đối tượng và phương pháp nghiên cứu: Đối tượng nghiên cứu là các mẫu huyết tương người giả lập chứa ALO và
OXY. Mẫu huyết tương được xử lý bằng phương pháp tủa protein và tiến hành định lượng đồng thời ALO và OXY
bằng HPLC-DAD
Kết quả: Mẫu huyết tương người chứa ALO và OXY và chuẩn nội acyclovir đã được tủa protein bằng acid percloric
10%, hiệu suất chiết ổn định trên 90% với CV < 15%. Điều kiện sắc ký: cột Gemini NX C18 (150 × 4,6 mm; 5,0 µm);
thể tích tiêm mẫu 40 µL; pha động là dung dịch acid formic 0,1%; tốc độ dòng 0,7 mL/phút; bước sóng phát hiện
254 nm. Khoảng tuyến tính: 0,10 - 20 μg/mL (ALO) và 0,09 – 18 μg/mL (OXY). Giới hạn định lượng dưới (LLOQ) là 0,10 μg/mL
(ALO) và 0,09 μg/mL (OXY). Quy trình thẩm định đã được áp dụng để phân tích một số mẫu huyết tương người bệnh
gút đang được điều trị bằng ALO.
Kết luận: Quy trình định lượng đồng thời ALO và chất chuyển hóa OXY trong huyết tương người bằng kỹ thuật
HPLC-PDA có độ nhạy, độ đặc hiệu, độ chính xác, độ đúng cao. Quy trình có thể được ứng dụng để định lượng ALO và
OXY trong huyết tương người trong các nghiên cứu dược động học và tương đương sinh học.
Từ khóa: Allopurinol; oxypurinol; huyết tương người; HPLC-DAD

Tạp chí Y học Thành phố Hồ Chí Minh - Dược học * Tập 28 * Số 1* 2025
https://doi.org/10.32895/hcjm.p.2025.01.02 https://www.duoc.tapchiyhoctphcm.vn | 9
Abstract
DEVELOPMENT OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHIC
METHOD FOR SIMULTANEOUS DETERMINATION OF ALLOPURINOL
AND OXYPURINOL METABOLITE IN HUMAN PLASMA
Le Thi Thu Cuc, Ngo Thi Minh Tam, Le Minh Tai, Nguyen Quang, Luong Bac An,
Le Hoang Gia Linh, Do Đuc Minh, Nguyen Duc Tuan
Background: Allopurinol (ALO) is a drug in the uric acid synthesis inhibitor group. After absorption into the blood, ALO
is extensively metabolized to the active metabolite oxypurinol
Objectives: Development of high-performance liquid chromatographic photodiode array detection (HPLC – DAD)
method for simultaneous determination of ALO and OXY metabolite in human plasma.
Methods: The subject of this study was simulated human plasma containing ALO and OXY. Human plasma samples
were treated by protein precipitation and ALO and OXY were simultaneously quantified by HPLC-DAD.
Results: Human plasma samples containing ALO and OXY and the internal standard acyclovir were protein precipitated
with 10% perchloric acid. The extraction efficiency was stable at over 90% with CV < 15%. Chromatographic conditions:
Gemini NX C18 column (150 × 4.6 mm; 5.0 µm); injection volume 40 µL; mobile phase 0.1% formic acid solution; flow
rate 0.7 mL/min; detection wavelength 254 nm. Linearity range: 0.10 - 20 μg/mL (ALO) and 0.09 - 18 μg/mL (OXY). LLOQ
were 0.10 μg/mL (ALO) and 0.09 μg/mL (OXY). The validation method was applied on analysis of plasma samples of
gout patients being treated with ALO.
Conclusion: A sensitive, specific, precise, and accurate HPLC-DAD method for simultaneous determination of ALO and
OXY in human plasma was successfully developed and validated. The method can be applied for quantification of these
compounds in human plasma for in vivo pharmacokinetic and bioequivalence studies.
Keywords: Allopurinol; oxypurinol; human plasma; HPLC-DAD
1. ĐẶT VẤN ĐỀ
Allopurinol (ALO) là thuốc thuộc nhóm ức chế tổng hợp
acid uric, được khuyến cáo lựa chọn đầu tiên trong điều trị
gút [1-3]. Hiện nay, thị trường Việt Nam đang lưu hành thuốc
generic ALO với giá thành thấp hơn nhiều so với thuốc gốc.
Tuy nhiên, các chế phẩm này chưa được đánh giá tương
đương sinh học so với thuốc gốc. ALO sau khi hấp thu vào
cơ thể được chuyển hóa phần lớn thành chất chuyển hóa có
hoạt tính là ALO.
Ngoài ra, hiện nay, đã bắt đầu có nghiên cứu tại Việt Nam
nhằm xác định các biến thể gen ABCG2 ở người bình thường
so với bệnh nhân gout có khác biệt hay không, biến thể nào
trên gen ABCG2 sẽ đóng vai trò là yếu tố nguy cơ gây bệnh
và dự đoán đáp ứng với các liệu pháp điều trị giảm acid uric
máu, từ đây yêu cầu một phương pháp định lượng ALO và
chất chuyển hóa có hoạt tính của nó là oxypurinol trong
huyết tương người bệnh gút trong các nghiên cứu này.
Trong huyết tương người đặc biệt là người bệnh có nền
mẫu phức tạp, nồng độ ALO và OXY thấp nên đòi hỏi
phương pháp định lượng phải có độ nhạy, độ đặc hiệu
và độ chính xác phù hợp. Việc định lượng ALO và
OXY bằng phương pháp các phương pháp HPLC-DAD,
LC-MS/MS đã được công bố trên nhiều tạp chí quốc tế
tuy nhiên tại Việt Nam, cho đến nay chưa có công trình
định lượng đồng thời ALO và OXY trong huyết tương
người được công bố. Nhóm nghiên cứu hướng tới
phương pháp HPLC-DAD với thiết bị phân tích phổ
biến, sẵn có sau khi xem xét giới hạn định lượng dưới
của phương pháp HPLC-DAD với ALO và OXY là
khoảng 0,1 μg/mL (tức là bằng khoảng 5 % so với
Cmax của ALO và khoảng 2 % so với Cmax của OXY
theo các tài liệu về dược động học).
Tạp chí Y học Thành phố Hồ Chí Minh - Dược học * Tập 28 * Số 1* 2025
10 | https://www.duoc.tapchiyhoctphcm.vn https://doi.org/10.32895/hcjm.p.2025.01.02
Vì vậy, đề tài này được thực hiện với mục tiêu xây dựng
quy trình định lượng đồng thời ALO và chất chuyển hóa
OXY trong huyết tương người bằng kỹ thuật HPLC-DAD,
góp phần vào việc đánh giá tương đương sinh học của các
chế phẩm chứa ALO trên thị trường và nghiên cứu dược
động học của ALO trên người bệnh gút tại Việt Nam.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP
NGHIÊN CỨU
2.1. Đối tượng nghiên cứu
Các mẫu huyết tương người tự tạo chứa hỗn hợp ALO và
OXY và các mẫu huyết tương trắng. 6 lô huyết tương trắng
sử dụng trong nghiên cứu được mua tại Bệnh viện Truyền
máu và Huyết học Thành phố Hồ Chí Minh và được bảo
quản ≤ -25 oC.
2.2. Chất đối chiếu
Danh mục các chất đối chiếu được trình bày ở Bảng 1.
Bảng 1. Các chất đối chiếu
Chất đối
chiếu
Hàm lượng
(tính theo
nguyên trạng)
Số lô Nguồn gốc/Nơi
cung cấp
Allopurinol 99,7% QT269
020520
Viện Kiểm nghiệ
m
thuốc TP.HCM
Oxypurinol 91,6% 1-SCZ-89-1
Toronto Canada
Acyclovir 94,1% QT149
070320
Viện Kiểm nghiệ
m
thuốc TP.HCM
2.3. Trang thiết bị
Máy sắc ký lỏng hiệu năng cao SHIMADZU prominence LC
30AD, Detector Diod Array SPD-M20A. Cân phân tích điện tử
Mettler Toledo AT200, bể siêu âm Hwashin, máy đo pH Mettler
Toledo, máy ly tâm lạnh effpendorf, tủ đông -20 oC (Alaska-
Mỹ), tủ đông -70 oC (Froilabo – Pháp), micropipett, bình định
mức, pipet chính xác, ống đong, cốc có mỏ,...
Các thiết bị phân tích và dụng cụ phân tích đã được hiệu
chuẩn đạt quy định theo GLP và ISO/IEC 17025.
2.4. Dung môi và hóa chất
Acetonitril và methanol đạt tiêu chuẩn dùng cho sắc ký
lỏng. Acid percloric, acid formic (FA) (Merck), natri acetat
và natri hydroxyd đạt tiêu chuẩn dùng cho phân tích.
2.5. Phương pháp nghiên cứu
ALO được chuyển hóa nhanh chóng bởi xanthine oxidase
thành chất chuyển hóa có hoạt tính chính là OXY [2]. Sau
khi uống, khoảng 80 - 90% liều uống được hấp thu nhanh
qua đường tiêu hóa. Nồng độ đỉnh trong huyết tương đạt
được sau 2 - 6 giờ ở liều thường dùng. Sau khi uống một liều
300 mg, nồng độ cao nhất trong huyết tương của ALO
khoảng 2 - 3 microgam/ml và của oxipurinol khoảng 5 - 6,5
microgam [1].
Tham khảo các công trình nghiên cứu [4-6-8] và dựa theo
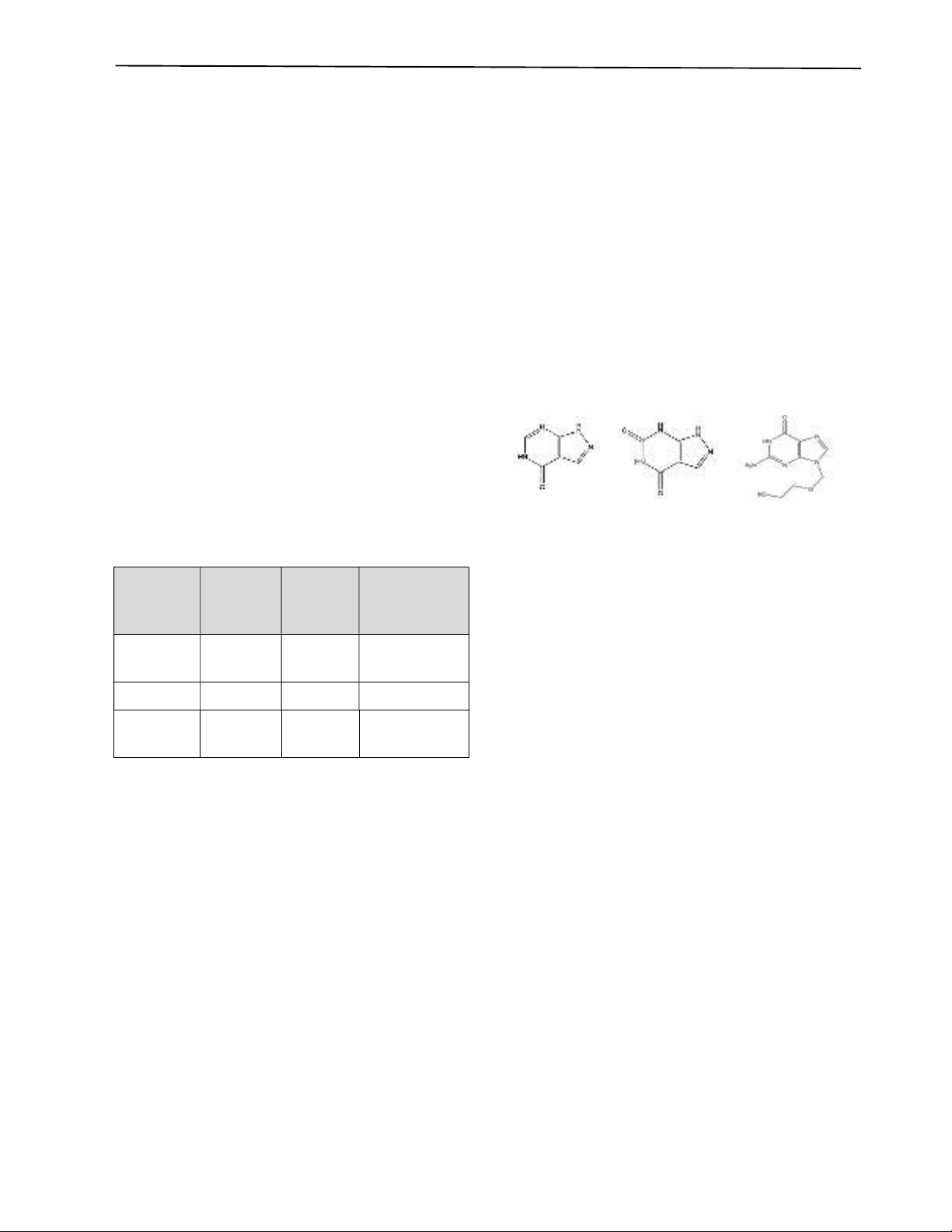
cấu trúc hóa học của các chất phân tích (Hình 1), phương
pháp được lựa chọn là phương pháp tủa protein (PPT) với
việc sử dụng acyclovir làm nội chuẩn (IS).
Allopurinol Oxypurinol Acyclovir
Hình 1. Cấu trúc của ALO, OXY và acyclovir (nội chuẩn)
2.5.1. Điều kiện sắc ký
Cột Gemini C18 NX (150 × 4,6 mm; 5 µm). Pha động:
acid formic 0,1% trong nước (tt/tt). Tốc độ dòng 0,7 mL/phút.
Bước sóng phát hiện 254 nm. Thể tích tiêm 40 µL. Nhiệt độ
cột 40 oC và nhiệt độ buồng tiêm mẫu 10 oC.
2.5.2. Chuẩn bị dung dịch chuẩn gốc, đường
chuẩn và mẫu QC (quality control)
Dung dịch chuẩn nội gốc
Cân chính xác khoảng 20 mg acyclovir, cho vào bình định
mức 100 mL, hòa tan trong 5 mL dung dịch NaOH 0,1 N,
sau đó điền đầy đến vạch bằng dung môi pha mẫu acetonitril
- nước (1:1, tt/tt). Từ dung dịch chuẩn nội gốc pha loãng với
dung môi pha mẫu acetonitril - nước (1:1, tt/tt) để thu được
dung dịch chuẩn nội có nồng độ 40 µg/mL (dung dịch IS).
Dung dịch chuẩn gốc ALO và OXY 1000 µg/mL
Cân chính xác khoảng 25 mg lượng chất chuẩn, cho vào
các bình định mức riêng biệt có dung tích 25 ml, hòa tan bằng
dung dịch NaOH 0,1 N sau đó điền đầy đến vạch bằng dung
môi pha mẫu acetonitril - nước (1:1, tt/tt) để thu được các
dung dịch chuẩn gốc có nồng độ tương ứng với từng chất

Tạp chí Y học Thành phố Hồ Chí Minh - Dược học * Tập 28 * Số 1 * 2025
https://doi.org/10.32895/hcjm.p.2025.01.02
https://www.duoc.tapchiyhoctphcm.vn
|
11
khoảng 1000 µg/mL, bảo quản ở nhiệt độ 2 -8 oC, để ở nhiệt
độ phòng trước khi sử dụng.
Dung dịch chuẩn hỗn hợp
Hút 20 mL dung dịch chuẩn gốc ALO, 20 mL dung dịch
chuẩn gốc OXY vào bình định mức 50 mL, pha loãng đến
vạch bằng dung môi pha mẫu được dung dịch L10.
Dung dịch chuẩn
Từ dung dịch chuẩn gốc ALO và OXY, tiến hành pha các
dung dịch chuẩn trong dung môi pha mẫu như Bảng 2.
Bảng 2. Cách pha dãy dung dịch chuẩn trong dung môi pha mẫu
Dung
dịch
Hút
(mL)
Từ dung
dịch
Bình định
mức (mL)
Nồng độ
Trong
DMPM
Trong huyết
tương
L10 1 L10 1 400 20,0
L9 20 L10 25 320 16,0
L8 5 L10 10 200 10,0
L7 10 L9 20 160 8,0
L6 3 L10 10 120 6,0
L5 5 L10 20 100 5,0
L4 3 L10 20 60 3,0
L3 5 L10 50 40 2,0
L2 3 L3 20 6 0,3
L1 1 L3 20 2 0,1
Từ các dung dịch chuẩn L1 -L10 tiến hành thêm vào huyết
tương trắng với tỷ lệ 5%: hút 1 mL dung dịch chuẩn trong
dung môi vào bình định mức 20 mL, điền đầy đến vạch bằng
huyết tương trắng thu được các mẫu giả lập đường chuẩn và
mẫu kiểm chứng (mẫu QC).
2.5.3. Xử lý mẫu
Lấy chính xác 500 µL huyết tương chứa các chất chuẩn
ALO, OXY (mẫu giả lập) cho vào ống nghiệm, thêm 50 μL
dung dịch IS; lắc xoáy 10 giây; thêm 250 μL acid percloric
10%; lắc xoáy 1 phút, ly tâm 17000 vòng/phút ở 20 oC trong
10 phút, lọc qua màng lọc Milipore 0,22 μm.
2.5.4. Thẩm định quy trình phân tích
Quy trình định lượng các chất ALO và OXY bằng phương
pháp HPLC được thẩm định dựa theo những quy định và yêu
cầu trong hướng dẫn của US-FDA và EMA [7].
Tính phù hợp của hệ thống
Tiêm lặp lại 6 lần một mẫu huyết tương giả lập có chứa
hỗn hợp ALO, OXY và chuẩn nội ở mức nồng độ MQC đã
qua xử lý. Yêu cầu: Các thông số sắc ký khảo sát có độ lệch
chuẩn tương đối (CV) 5,0%.
Tính đặc hiệu
Tiến hành sắc ký mẫu huyết tương trắng, mẫu giả lập thêm
chuẩn nội ở mức nồng độ giới hạn định lượng dưới của phạm
vi định lượng (LLOQ). Yêu cầu: mẫu huyết tương trắng cho
tín hiệu phân tích nằm trong giới hạn cho phép (≤ 20% diện
tích pic đối với các chất phân tích và ≤ 5% đối với chuẩn nội
trong dung dịch ở mức nồng độ giới hạn định lượng dưới).
Sau khi khảo sát giá trị LLOQ của ALO và OXI theo yêu cầu
thỏa mãn điều kiện tín hiệu đáp ứng của chất phân tích so với
tín hiệu đáp ứng của mẫu huyết tương trắng ít nhất bằng 5
lần và cho độ chính xác trong khoảng ± 20% và độ đúng
80 - 120% , giá trị LLOQ của ALO là 0,10 μg/mL và LLOQ
của OXI là 0,09 μg/mL
Giới hạn định lượng dưới (LLOQ)
Tiến hành xác định nồng độ thấp nhất sao cho thỏa mãn
điều kiện tín hiệu đáp ứng của chất phân tích so với tín hiệu
đáp ứng của mẫu huyết tương trắng ít nhất bằng 5 lần và cho
độ chính xác trong khoảng ± 20% và độ đúng 80 -120%. Tiến
hành sắc ký trên 6 lô mẫu huyết tương trắng và 6 mẫu huyết
tương chứa OXY, ALO (nồng độ LLOQ). Ghi nhận S/N
của các chất phân tích và đánh giá độ đúng, độ chính xác
trên 6 mẫu LLOQ.
Đường chuẩn và khoảng tuyến tính
Chuẩn bị các hỗn hợp chuẩn với nồng độ trong phạm vi
định lượng. Thêm các hỗn hợp chuẩn này vào trong huyết
tương trắng (với tỷ lệ 5% thể tích so với nền mẫu), thêm tiếp
chuẩn nội và tiến hành xử lý mẫu để thu được giai mẫu chuẩn
có nồng độ trong phạm vi định lượng. Xác định sự tương
quan giữa nồng độ và tỷ số diện tích pic của chất phân tích
và diện tích của pic chuẩn nội. Vẽ đường biểu diễn sự tương
quan giữa giá trị nồng độ và tỷ số diện tích pic theo hàm giá
trị đã xây dựng được.
Khoảng tuyến tính của ALO và OXY thiết lập gồm 10
nồng độ cho mỗi chất đi từ giới hạn định lượng dưới (LLOQ)
đến giới hạn định lượng trên (ULOQ). Nồng độ thấp nhất từ
LLOQ thỏa mãn điều kiện tín hiệu đáp ứng của chất phân

Tạp chí Y học Thành phố Hồ Chí Minh - Dược học * Tập 28 * Số 1* 2025
12 | https://www.duoc.tapchiyhoctphcm.vn https://doi.org/10.32895/hcjm.p.2025.01.02
tích so với tín hiệu đáp ứng của mẫu huyết tương trắng ít nhất
bằng 5 lần và cho độ chính xác trong khoảng ± 20% và độ
đúng 80 - 120%, trong nghiên cứu này giá trị LLOQ của
ALO là 0,10 μg/mL và LLOQ của OXI là 0,09 μg/mL. Mức
giá trị ULOQ của ALO là khoảng 20 μg/mL và ULOQ của
OXI khoảng 18 μg/mL (tương ứng 200 % so với LLOQ)
Các giá trị cụ thể 10 điểm trong đường chuẩn khoảng tuyến
tính được trình bày ở Bảng 3.
Độ đúng và độ chính xác trong ngày và giữa
các ngày
Độ đúng và độ chính xác trong ngày được xác định
cùng lúc trên các mẫu huyết tương người có chứa chất
cần phân tích tại 4 mức nồng độ LLOQ, LQC, MQC,
HQC. Mỗi mức nồng độ được chuẩn bị 6 mẫu. Tiến
hành xử lý mẫu và sắc ký trong một ngày. Đánh giá độ
chính xác và độ đúng giữa các ngày bằng cách tiếp tục
thực hiện thêm ít nhất 02 ngày.
Tỷ lệ phục hồi (Hiệu suất chiết)
Chuẩn bị các mẫu có chứa ALO, OXY trong huyết
tương người và trong dung môi pha mẫu ở các mức
nồng độ LQC, MQC và HQC, mỗi nồng độ 6 mẫu. Tiến
hành xử lý mẫu. Xác định tỷ lệ phục hồi bằng cách so sánh
đáp ứng của chất phân tích được chiết từ mẫu giả lập thêm
chuẩn nội ở 3 mức nồng độ LQC, MQC và HQC với đáp
ứng của mẫu chuẩn có cùng nồng độ tương ứng được
pha trong dung môi.
Độ ổn định trong huyết tương
Pha 5 lô mẫu, mỗi lô chứa ALO, OXY trong huyết
tương người ở mức nồng độ LQC, HQC, mỗi nồng độ
6 mẫu. Phân tích 1 lô theo phương pháp đã xây dựng.
Độ ổn định ngắn hạn ở nhiệt độ phòng sau 6 giờ: Lô
thứ 2 để ở nhiệt độ phòng trong 6 giờ rồi phân tích. Độ
ổn định của mẫu sau 3 chu kỳ đông - rã đông: Lô thứ 3
bảo quản ở -20 oC, lấy ra để yên ở nhiệt độ phòng cho đến
khi rã đông, lặp lại chu trình thêm 2 lần. Phân tích mẫu
sau 3 chu trình đông - rã đông. Độ ổn định của mẫu trong
buồng tiêm mẫu sau khi xử lý mẫu 24 giờ: Tiêm lại lô mẫu
ở mức nồng độ LQC, HQC, mỗi nồng độ 6 mẫu, sau 24
giờ xử lý và bảo quản trong buồng tiêm mẫu ở 10 oC. Độ
ổn định dài hạn ở -20 ºC sau 30 và 90 ngày: Các lô còn
lại bảo quản ở nhiệt độ 20 oC và phân tích sau thời gian
sau 30, 90 ngày.
Độ ổn định trong dung dịch gốc
Pha 3 lô mẫu, mỗi lô chứa ALO và OXY trong dung môi
ở mức nồng độ MQC, mỗi lô 6 mẫu. Phân tích 1 lô theo
phương pháp đã xây dựng. Độ ổn định ngắn hạn ở nhiệt độ
phòng sau 6 giờ: Lô thứ 2 để ở nhiệt độ phòng trong 6 giờ
rồi phân tích. Độ ổn định dài hạn ở 2-8 oC sau 15 ngày: Lô
còn lại bảo quản ở nhiệt độ 2-8 oC và phân tích trong thời
gian sau 15 ngày.
Độ ổn định của dung dịch IS
Pha 3 lô mẫu chứa IS trong dung môi, mỗi lô 6 mẫu. Phân
tích 1 lô theo phương pháp đã xây dựng. Độ ổn định ngắn
hạn ở nhiệt độ phòng sau 6 giờ: Lô thứ 2 để ở nhiệt
độ phòng trong 6 giờ rồi phân tích. Độ ổn định dài hạn
ở 2-8 oC sau 15 ngày: Lô còn lại bảo quản nhiệt độ 2-8 oC
và phân tích trong thời gian sau 15 ngày.
Mẫu được xem là ổn định nếu như giá trị tìm lại của từng
hoạt chất nằm trong khoảng từ 85 -115 % của nồng độ ban
đầu ở từng mức nồng độ.
Ảnh hưởng của nền mẫu (MF)
Chuẩn bị 6 lô huyết tương người khác nhau, mỗi lô 3 mẫu,
tiến hành phân tích mẫu theo quy trình xử lý mẫu, mẫu sau
khi xử lý được thêm chất phân tích ở 2 mức nồng độ LQC,
HQC và chuẩn nội vào 2 mẫu mỗi lô. Tiến hành phân tích
mẫu song song với mẫu LQC và HQC có chuẩn nội trong
pha động để tính ảnh hưởng của nền mẫu. MF được tính theo
công thứ sau:
MFAS = Area MAS / Area MPAS
MFIS = Area MIS / Area MPIS
MF = MFAS / MFIS
Trong đó: Area MAS (IS): diện tích pic của chất phân tích
(hoặc chuẩn nội) trong huyết tương người; Area MPAS (IS):
diện tích pic của chất phân tích (hoặc chuẩn nội) trong pha
động. Yêu cầu: CV của MF < 15%.
Ảnh hưởng của lượng mẫu tồn dư (Carryover)
Tiến hành tiêm mẫu có nồng độ cao nhất trong huyết
tương người (ULOQ) sau xử lý vào hệ thống sắc ký,
sau khi phân tích xong, tiêm ngay mẫu huyết tương
trắng (Blank) đã xử lý vào hệ thống. Thực hiện quy
trình trên 6 lần. Tiêm 6 lần mẫu ở mức nồng độ LLOQ
trong huyết tương người sau xử lý để đánh giá kết quả.









![Các thông số dược động học ứng dụng trong lâm sàng [chuẩn SEO]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250328/quyvanphi/135x160/5981743096622.jpg)
















