
TNU Journal of Science and Technology
230(05): 436 - 441
http://jst.tnu.edu.vn 436 Email: jst@tnu.edu.vn
PHENOLIC COMPOUNDS FROM THE LEAVES OF CITRUS SINENSIS
AT HAM YEN, TUYEN QUANG
Tran Duc Dai*, Nguyen Thi Tuyet
Tan Trao University
ARTICLE INFO
ABSTRACT
Received:
23/6/2023
The genus Citrus belongs to the family Rutaceae, This genus is
the most important fruit tree crop in the world. Citrus sinensis
(L.) Osbeck is one of the extensively studied plants. Citrus
sinensis has been used traditional with preparations derived from
peels, young fruit, mature fruit, flower, and other tissues. It is
known for numerous activities such as colic, tuberculosis,
diarrhea, cough, cold, menstrual disorder, obesity, angina,
antidiabetic, hypertension, antiosteoporosis, cramps, bronchitis,
and stress, etc. due to the presence of phenolic acids, flavonoids,
and essential oil components. In this study, column
chromatography was used to ethyl acetat extract of Citrus sinensis
leaves (Moraceae) led to isolation of three phenolic compounds:
Sinensetin, Nobiletin, Tangeritin. Their chemical structures were
elucidated by spectroscopic methods (1H-NMR, 13C-NMR, DEPT,
HSQC, HMBC) and by comparison with data reported in the
literatures.
Revised:
06/02/2025
Published:
07/02/2025
KEYWORDS
Cam sanh
Citrus sinensis
Ham Yen
Tuyen Quang
Phenolic
n-hexan
Ethyl acetat
CÁC HỢP CHẤT FLAVONOID TỪ LÁ CAM SÀNH (CITRUS SINENSIS)
TẠI HÀM YÊN, TUYÊN QUANG
Trần Đức Đại*, Nguyễn Thị Tuyết
Trường Đại học Tân Trào
THÔNG TIN BÀI BÁO
TÓM TẮT
Ngày nhận bài:
23/6/2023
Cây cam sành (Citrus sinensis) thuộc nhóm cây có múi (Citrus) thuộc
họ Rutaceae, chi này là một trong những cây ăn quả có múi quan
trọng nhất trên thế giới. Cây cam sành là một trong những loài thực
vật được nghiên cứu nhiều. Cây cam đã được người dân sử dụng làm
thuốc với nhiều thành phần khác nhau như vỏ, quả non, quả chín, hoa
và các thành phần khác. Nó được biết đến như một vị thuốc chữa đau
bụng, bệnh lao, tiêu chảy, ho, cảm lạnh, rối loạn kinh nguyệt, béo
phì, đau thắt ngực, chống tiểu đường, tăng huyết áp, chống loãng
xương, chuột rút, viêm phế quản và căng thẳng, v.v. do trong thành
phần hóa học của cây cam có các hợp chất phenolic, flavonoid và các
thành phần tinh dầu. Trong nghiên cứu này, phương pháp sắc ký cột
đã được sử dụng để tách các hợp chất hóa học từ cao etyl axetat của
lá cam kết quả đã phân lập ba hợp chất phenolic: Sinensetin,
Nobiletin, Tangeritin. Cấu trúc hóa học của 3 hợp chất được xác định
bằng các phương pháp quang phổ (1H-NMR, 13C-NMR, DEPT,
HSQC, HMBC) và bằng cách so sánh với dữ liệu được báo cáo trong
các tài liệu.
Ngày hoàn thiện:
06/02/2025
Ngày đăng:
07/02/2025
TỪ KHÓA
Cam sành
Citrus sinensis
Hàm Yên
Tuyên Quang
Phenolic
n-hexan
Ethyl acetat
DOI: https://doi.org/10.34238/tnu-jst.8200
* Corresponding author: Email: ducdaitq@gmail.com

TNU Journal of Science and Technology
230(05): 436 - 441
http://jst.tnu.edu.vn 437 Email: jst@tnu.edu.vn
1. Giới thiệu
Cây cam có tên khoa học là Citrus sinensis, đại diện cho các nhóm cây có múi được trồng
nhiều nơi trên thế giới, chiếm khoảng 70% tổng sản lượng hàng năm của các loài Cam quýt [1].
Các nghiên cứu chỉ ra một số loại hợp chất hóa học đã được xác định trong trái cây, vỏ, lá, nước
ép và rễ của cây cam (C. sinensis), bao gồm các nhóm sau: flavonoid, steroid, hydroxyamit,
ankan, axit béo, coumarin, peptit, carbohydrate, carbamat, alkylamine, carotenoid, các hợp chất
dễ bay hơi và các nguyên tố vi lượng như kali, magie, canxi, natri… [2], [3].
Hoạt tính kháng khuẩn của tinh dầu, dịch chiết xuất thô từ vỏ cam, cho thấy các vùng ức chế
Escherichia coli, S.aureus và P.aeruginosa, L. monocytogenes, S.typhimurium, L.plantarum và B.
cereus [2], [4], kháng viêm, chống oxy hóa [5], [6], hạ đường huyết [7]. Trong tinh dầu vỏ quả
cam sành Hàm Yên chứa các hợp chất như cis-Ocimene 2,4,6-Trimethyl-1-nonene, L-Limonene,
δ-3-Carene, δ-cadinene, β-Pinene, Camphene, α-Thujene, α-Bergamotene, Gettysolve B,
Camphene, Octyl alcohol, α-Copaene-11-ol, n-Butan-1-ol, α-Terpineol, Terpinene-4-ol, Nerol,
trans-Geraniol, β-Elemol, Linalool, cis-Geraniol [8]-[10].
Các hợp chất hóa học tự nhiên của cây cam (lá, thân, rễ, quả) có tiềm năng sử dụng làm chất
bảo vệ thực vật tự nhiên thân thiện với môi trường, các nghiên cứu về thành phần hóa học của lá
cam sành tại Hàm Yên, Tuyên Quang chưa nhiều, do đó việc nghiên cứu thành phần hóa học và
hoạt tính sinh học các cao chiết lá cam sành tại Hàm Yên Tuyên Quang là cần thiết làm cơ sở
khoa học cho việc nghiên cứu các sản phẩm bảo vệ sức khỏe, thực phẩm chức năng.
2. Phương pháp nghiên cứu
2.1. Đối tượng nghiên cứu
Hình 1. Cây cam sành chụp tại Hàm Yên, Tuyên Quang tháng 11 năm 2022
Mẫu nghiên cứu lá cam sành thu hái tại Hàm Yên, Tuyên Quang, thời gian thu mẫu vào tháng
12/2022. Mẫu nghiên cứu được TS. Đỗ Công Ba, giảng viên Khoa Y Dược, Trường Đại học Tân
Trào xác định tên khoa học Citrus sinensis. Mẫu lá cam sành Hàm Yên được lưu tại Phòng thực
hành Hóa – Trường Đại học Tân Trào.
2.2. Phương pháp nghiên cứu
2.2.1. Phương pháp tạo cao chiết từ lá cam
TNU Journal of Science and Technology
230(05): 436 - 441
http://jst.tnu.edu.vn 438 Email: jst@tnu.edu.vn
Mẫu tươi 6 kg lá cam tươi được thái nhỏ, sấy ở nhiệt độ 45oC đến khô (2 kg), mẫu khô nghiền
nhỏ, cho vào bình ngâm chiết với ethanol (5 lần x 10 lít), nhiệt độ thường khoảng 24oC, dùng
máy siêu âm phá mẫu, nhiệt máy siêu âm khoảng 50oC thu được dịch chiết tổng.
Dịch chiết tổng được lọc qua giấy lọc, sau đó tiến hành loại dung môi bằng thiết bị cất quay
chân không (to < 52oC), dưới áp suất giảm, thu được cao chiết tổng dưới dạng siro (500 g). Hòa
tan cao chiết tổng với 0,5 lít (H2O), sau đó đem chiết phân đoạn lần lượt bằng các loại dung môi
có độ phân cực tăng dần (n-hexane, ethyl acetate, butanol), đuổi kiệt dung môi thu được các cặn
tương ứng lần lượt là cặn n–hexane (CSH 200 g), ethyl acetate (CSE 40 g), buthanol (CSB 85 g)
và dịch nước. Các cao chiết dùng để phân tích thành phần hóa học.
2.2.2. Phương pháp phân lập các hợp chất từ lá cam
Phân đoạn ethyl acetat tiếp tục được tách thành các đoạn nhỏ khác nhau bằng các phương
pháp sắc ký. Sự có mặt của các chất trong các phân đoạn được đánh giá bằng sắc ký lớp mỏng
(Thin layer chromatography - TLC) pha thường và pha đảo sử dụng dung dịch hiện màu là acid
sulfuric 10% phun đều lên bản mỏng và hơ nóng từ từ đến khi các vệt chất hiện rõ.
Sử dụng kết quả hiển thị vệt chất trên TLC để tiến hành gom và chia các phân đoạn đã được
sắc ký. Các phân đoạn thu được tiếp tục được kiểm tra bằng TLC để lựa chọn phương pháp sắc
ký phù hợp để tiếp tục phân tách thành các phân đoạn nhỏ hơn.
Lặp lại các công việc như trên, cuối cùng sẽ thu được các hợp chất sạch, đủ lượng để tiến
hành đo các phổ và xác định cấu trúc.
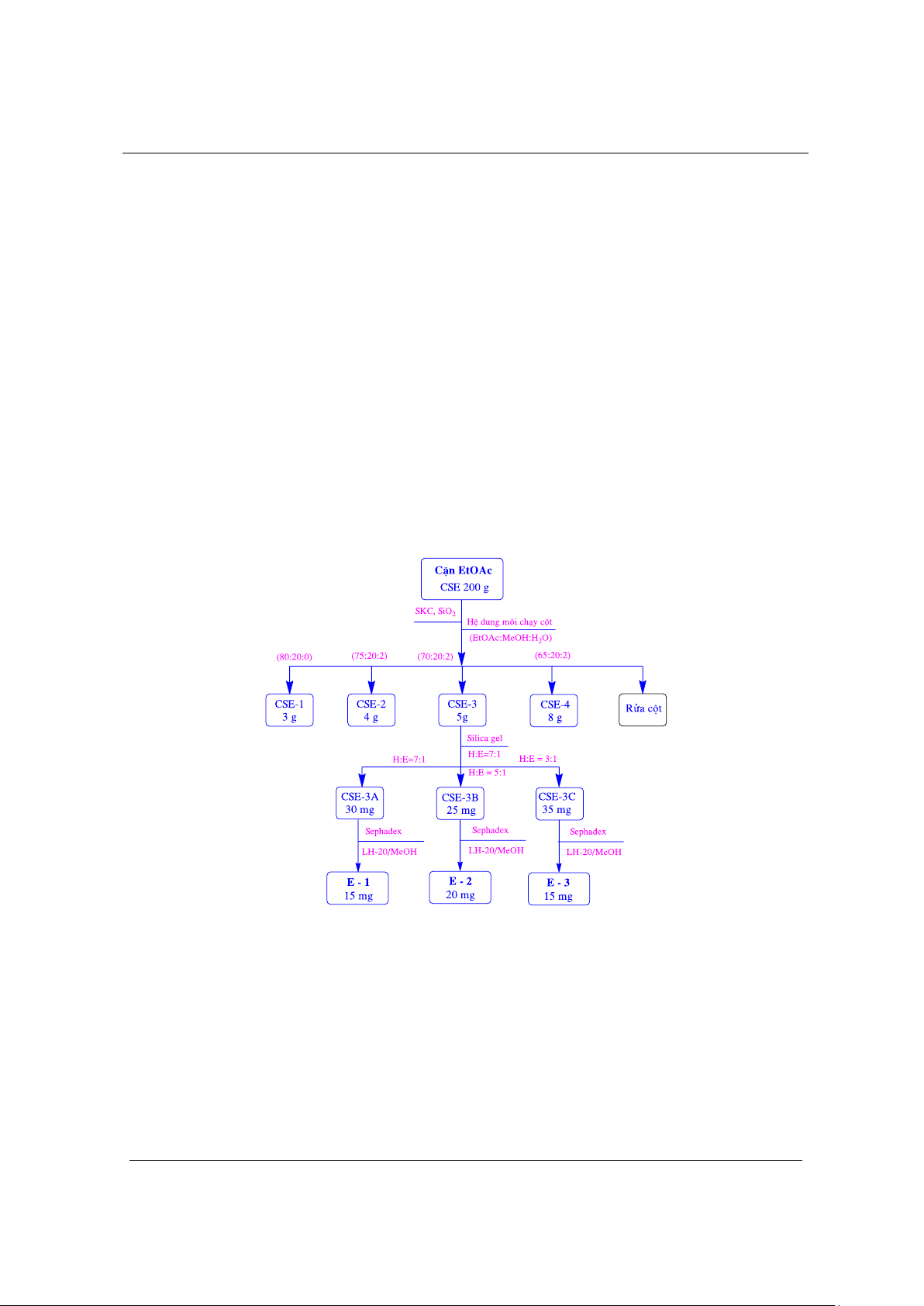
Hình 2. Sơ đồ phân lập các hợp chất từ cao ethylacetat (EtOAc) lá cam
Hợp chất E1 (Sinensetin) tách được từ cao chiết ethyl acetat lá cam có dạng tinh thể hình
kim, có khối lượng 15 mg. Dùng phương pháp sắc ký bản mỏng với hệ dung môi sắc ký (H:E =
7:1), Rf = 0,6, vệt chất của E-1 trên TLC hiện vệt tròn khi sử dụng thuốc thử H2SO4 10% và hơ
nóng từ từ. Đo phổ proton (1H-NMR) bằng máy cộng hưởng từ hạt nhân, công suất máy 500
MHz, dung môi pha mẫu CD3OD số liệu phổ như sau: 1H-NMR (500 MHz, CD3OD): δH 7.62
(1H, dd, J = 8.5, 2.0 Hz, H-6′), 7.50 (1H, d, J = 2.0 Hz, H-2′), 7.12 (1H, H-8), 7.11 (1H, d, J = 8.5
Hz, H-5′), 6.65 (1H, s, H-3). 4.03 (3H, s, OCH3), 3.96 (3H, s, OCH3), 3.94 (3H, s, OCH3), 3.93
(3H, s, OCH3), 3.88 (3H, s, OCH3). 13C-NMR (125 MHz, CD3OD): δC 179.59 (C-4), 163.74 (C-
2), 159.99 (C-7), 156.13 (C-9), 153.85 (C-4′), 153.32 (C-5), 150.89 (C-3′), 141.80 (C-6), 124.85
(C-1′), 121.22 (C-6′), 113.10 (C-10), 112.78 (C-5′), 110.49 (C-2′), 107.11 (C-3), 97.98 (C-8),
62.61, 61.80, 57.05, 56.74, 56.51 (6xOCH3).
TNU Journal of Science and Technology
230(05): 436 - 441
http://jst.tnu.edu.vn 439 Email: jst@tnu.edu.vn
Hợp chất E2 (Nobiletin) tách được từ cao chiết ethyl acetat lá cam có dạng tinh thể hình kim,
có khối lượng 20 mg. Dùng phương pháp sắc ký bản mỏng với hệ dung môi sắc ký (H:E = 7:1),
Rf = 0,6, vệt chất của E-2 trên TLC hiện vệt tròn khi sử dụng thuốc thử H2SO4 10% và hơ nóng từ
từ. Đo phổ proton (1H-NMR) bằng máy cộng hưởng từ hạt nhân, công suất máy 500 MHz, dung
môi pha mẫu CD3OD số liệu phổ như sau: 1H-NMR (500 MHz, CD3OD): δH 7.64 (1H, dd, J =
7.0, 1.5 Hz, H-6′), 7.53 (1H, d, J = 1.5 Hz, H-2′), 7.12 (1H, d, J = 7.0 Hz, H-5′), 6.68 (1H, s, H-3).
4.12 (3H, s, OCH3), 4.04 (3H, s, OCH3), 3.95 (3H, s, OCH3), 3.94 (3H, s, OCH3), 3.93 (3H, s,
OCH3), 3.91 (3H, s, OCH3).
Hợp chất E3 (Tangeritin) tách được từ cao chiết ethyl acetat lá cam có dạng tinh thể hình
kim, có khối lượng 15 mg. Dùng phương pháp sắc ký bản mỏng với hệ dung môi sắc ký (H:E =
7:1), Rf = 0,6, vệt chất của E-3 trên TLC hiện vệt tròn khi sử dụng thuốc thử H2SO4 10% và hơ
nóng từ từ. Đo phổ proton (1H-NMR) bằng máy cộng hưởng từ hạt nhân, công suất máy 500
MHz, dung môi pha mẫu CD3OD số liệu phổ như sau: 1H-NMR (500 MHz, CD3OD): δH 7.99
(1H, d, J = 7.0 Hz, H-2′&6′), 7.12 (1H, d, J = 7.0 Hz, H-3′&5′), 6.68 (1H, s, H-3). 4.12 (3H, s, 7-
OCH3), 4.04 (3H, s, 6-OCH3), 3.94 (3H, s, 5-OCH3), 3.92 (3H, s, 4′-OCH3), 3.91 (3H, s, 8-
OCH3). 13C-NMR (125 MHz, CD3OD): δC 179.45 (C-4), 166.16 (C-4′), 164.36 (C-2), 153.37 (C-
7), 149.36 (C-8), 149.19 (C-9), 144.93 (C-5), 139.70 (C-6), 129.12 (C-2′&6′), 124.52 (C-1′),
115.72 (C-10, 3′&5′), 106.73 (C-3), 62.67, 62.63 (C-6&C-8), 62.23, 62.18 (C-5&C-7), 56.54 (4′-
OCH3).
3. Kết quả và bàn luận
Từ 6 kg lá cam tươi tách các hợp chất sạch bằng các phương pháp tách chiết, kết tinh lại, xác
định cấu trúc hóa học các hợp chất bằng phương pháp phổ cộng hưởng từ hạt nhân, ổ 1H-NMR,
13C-NMR và DEPT, các phổ cộng hưởng từ hạt nhân hai chiều (HSQC, HMBC, COSY, NOESY và
ROESY), phổ hồng ngoại và dựa trên các số liệu phổ của các chất đã biết cấu trúc đã phân lập
được 3 hợp chất phenolic bao gồm: E-1 (Sinensetin); E-2 (Nobiletin); E-3 (Tangeritin) cụ thể
như sau:
Phổ proton 1H-NMR của hợp chất E-1 có 1 proton thơm vòng A cộng hưởng tại δH 7.12 ppm
(1H, s, H-8); do đó có 3 vị trí bị thế H tại vòng A. Phổ của vòng B của hợp chất E-1 cho thấy có
bộ 3 tín hiệu proton thơm thuộc loại vòng ABX. Tín hiệu proton tại δH 6.65 ppm (1H, s) cho tín
hiệu 1 proton gán cho H-3 [11], [12]. Có tín hiệu proton đơn tại δH 4.03 (3H, s, OCH3) đính vào
carbon C-5, tại 3.93 (3H, s, OCH3) đính vào carbon C-6, tại 3.94 (3H, s, OCH3) đính vào carbon
C-7, tại 3.96 (3H, s, OCH3) đính vào carbon C-3′, tại 3.88 (3H, s, OCH3) đính vào carbon C-4′
[11], [12], phổ các bon 13C-NMR cho thấy có 20 tín hiệu carbon, trong đó tín hiệu tại δC 179.59
ppm ứng với nhóm các bonyl (> C = O) tương ứng với carbon C-4, có 5 tín hiệu các bon tại δC
62.61, 61.80, 57.05, 56.74, 56.51 ứng với 5 nhóm -OCH3. Các tín hiệu carbon tương đồng với
các tín hiệu carbon của công bố [11]. Phổ HSQC có 5 tín hiệu các bon (màu đỏ) ứng với các
nguyên tử carbon có số nguyên tử H lẻ (HC). Từ kết quả phân tích trên, so sánh số liệu phổ của
hợp chất E-1 với số liệu của hợp chất sinensetin đã được công bố trong tài liệu [12] là trùng
khớp; do đó cấu trúc của hợp chất E-1 được xác định là sinensetin tên IUPAC là 3′,4′,5,6,7-
Pentamethoxyflavone.
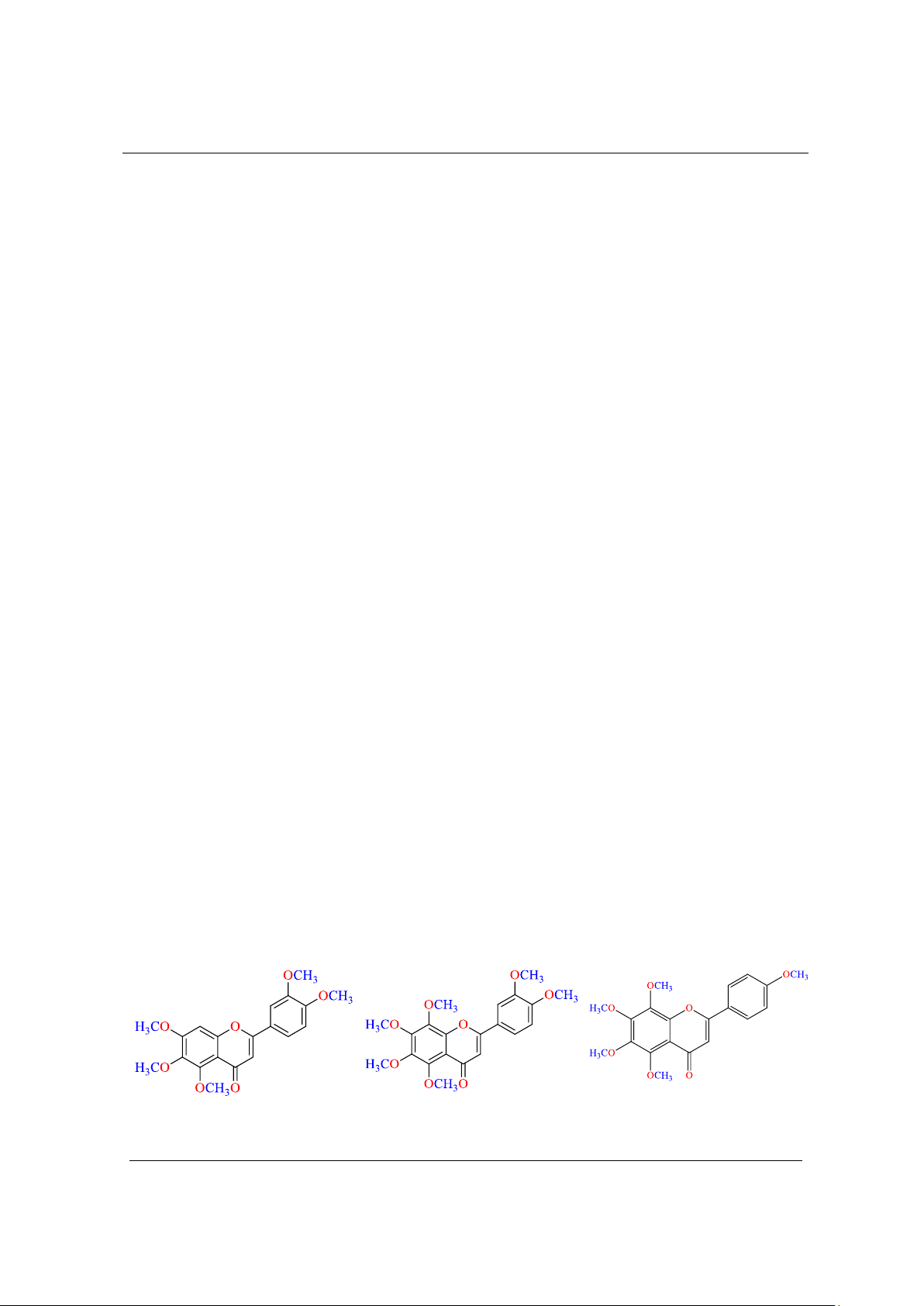
Hình 3. Cấu trúc hóa học của hợp chất E-1, E-2, E-3

TNU Journal of Science and Technology
230(05): 436 - 441
http://jst.tnu.edu.vn 440 Email: jst@tnu.edu.vn
Phổ proton 1H-NMR của hợp chất E-2 cho thấy có bộ 3 tín hiệu proton thơm thuộc loại vòng
ABX ứng với δH 7.65 (1H, dd, J = 7.0, 1.5 Hz, H-6′), 7.53 (1H, d, J = 1.5 Hz, H-2′), 7.12 (1H, d,
J = 7.0 Hz, H-5′). Tín hiệu proton tại δH 6.68 ppm (1H, s) cho tín hiệu 1 proton gán cho H-3 [11],
[12]. Có 6 tín hiệu proton đơn tại δH 4.12 (3H, s, OCH3) đính vào carbon C-5, tại 4.04 (3H, s,
OCH3) đính vào carbon C-6, tại 3.95 (3H, s, OCH3) đính vào carbon C-7, tại 3.94 (3H, s) đính
vào carbon C-8, tại 3.93 (3H, s, OCH3) đính vào carbon C-3′, tại 3.91 (3H, s, OCH3) đính vào
carbon C-4′ [11], [12]. Phổ các bon 13C-NMR cho thấy có 20 tín hiệu carbon, trong đó tín hiệu tại
δC 179.58 ppm ứng với nhóm các bonyl (>C=O) tại carbon C-4. Có 6 tín hiệu các bon tại δC
62.66, 62.60, 62.22, 62.18, 56.58, 56.52 ứng với 6 nhóm -OCH3. Các tín hiệu carbon của hợp
chất E-2 tương đồng với các tín hiệu carbon của hợp chất Nobiletin đã công bố [11]. Phổ HSQC
có 4 tín hiệu các bon có số nguyên tử H lẻ (-CH=) C-3, C-2′, C-5′, C-6′ và có 6 tín hiệu màu đỏ ứng
với 6 nhóm OCH3. Từ kết quả phân tích trên, so sánh số liệu phổ của hợp chất E-2 với số liệu phổ
của hợp chất Nobiletin đã được công bố trong tài liệu [12] là trùng khớp, do đó khẳng định hợp
chất E-2 được xác định là Nobiletin tên IUPAC là 3′,4′,5,6,7,8-Hexamethoxyflavone.
Phổ proton 1H-NMR của hợp chất E-3 cho thấy có bộ 4 tín hiệu proton thơm thuộc loại vòng
ABX ứng với δH 7.99 (1H, d, J = 7.0 Hz, H-2′&6′), 7.12 (1H, d, J = 7.0 Hz, H-3′&5′) và tín hiệu
proton tại δH 6.68 ppm (1H, s) của 1 proton gán cho H-3 [13]. Có 5 tín hiệu proton đơn tại δH 4.12
(3H, s, OCH3) đính vào carbon C-7, tại 4.04 (3H, s, OCH3) đính vào carbon C-6, tại 3.94 (3H, s,
OCH3) đính vào carbon C-5, tại 3.92 (3H, s) đính vào carbon C-4′, tại 3.91 (3H, s, OCH3) đính
vào carbon C-8 [13]. Phổ các bon 13C-NMR cho thấy có 20 tín hiệu carbon, trong đó tín hiệu
tại δC 179.45 ppm ứng với nhóm các bonyl (>C=O) tại carbon C-4. Có 5 tín hiệu các bon
tại δC 62.67, 62.63 (C-6&C-8), 62.23, 62.18 (C-5&C-7), 56.54 (4′-OCH3) ứng với 6 nhóm -
OCH3. Các tín hiệu carbon của hợp chất E-3 tương đồng với các tín hiệu carbon của hợp
chất Tangeritin đã công bố [13]. Phổ HSQC có 10 tín hiệu các bon (màu đỏ) ứng với 10 nguyên
tử carbon có số nguyên tử H lẻ (-CH=) C-3, C-2′, C-5′, C-6′ và có 5 tín hiệu màu đỏ ứng với 5
nhóm OCH3. Từ kết quả phân tích trên, so sánh số liệu phổ của hợp chất E-3 với số liệu phổ của
hợp chất Tangeritin đã được công bố trong tài liệu [13] là trùng khớp, do đó khẳng định hợp chất
E-3 được xác định là Tangeritin tên IUPA là 4′,5,6,7,8-Pentamethoxyflavone.
4. Kết luận
Từ 6 kg lá cam sành tươi tách được 3 hợp chất sạch, bằng các phương pháp tách chiết, kết tinh
lại, phương pháp phổ cộng hưởng từ hạt nhân, phổ proton (1H-NMR), phổ các bon 13 (13C-NMR)
và phổ DEPT, các phổ cộng hưởng từ hạt nhân hai chiều (HSQC, HMBC) và so sánh với các số liệu
phổ của các chất đã biết cấu trúc, nhóm nghiên cứu đã xác định cấu trúc hóa học của 3 hợp chất
phenolic bao gồm: E-1 (Sinensetin); E-2 (Nobiletin); E-3 (Tangeritin).
TÀI LIỆU THAM KHẢO/ REFERENCES
[1] K. N. Sheetal, M. S. Vala, and B. B. Maitreya, “A review: Phytochemical constituents, medicinal uses
and economical value of orange peels (Citrus sinensis L Osbeck),” International Journal of Creative
Research Thoughts, vol. 8, no. 5, pp. 1340-1354, 2020.
[2] J. J. Manuel, Favela-Hernández, O. González-Santiago, A. Mónica, Ramírez-Cabrera, C. Patricia,
Esquivel-Ferriño, and M. del R. Camacho-Corona, “Chemistry and Pharmacology of Citrus sinensis,”
Molecules, vol. 21, 2016, Art. no. 247.
[3] M. Yovo, G. A. Alitonou, P. Sessou, L. Dedome, F. Tchobo, F. Avléssi, C. Menut, and D,
Sohounhloué, “Phytochemistry and Antibacterial Activity of Citrus sinensis Extracts against Three
Pathogenic Bacteria in Benin,” Research Journal of Pharmaceutical, Biological and Chemical
Sciences, vol.7, no. 6, pp. 1344-1352, 2016.
[4 The Royal Society & The Royal Academy of Engineering, Nanoscience and nanotechnologies:
opportunities and uncertainties, London, 2004.
[5] S. S. Liew, W. Y. Ho, S. K. Yeap, and S. A. B. Sharifudin, “Phytochemical composition and in vitro
antioxidant activities of Citrus sinensis peel extracts,” PeerJ, vol. 6, pp. 1-26, 2018, Art. no. e5331.


























