
BƯỚC TIẾN MỚI TRONG DỰ PHÒNG
BIẾN CỐ TIM MẠCH KHI STATIN
ĐƠN ĐỘC CHƯA ĐỦ HIỆU QUẢ
Bs Nguyễn Thanh Hiền

Nội dung
1. LDL-C: Nỗ lực ĐT và thách thức
2. Xu hướng phối hợp thuốc với cơ chế ức chế kép sinh tổng
hợp và hấp thu cholesterol
3. Bằng chứng cải thiện tốt hơn kết cục tim mạch của phối hợp
Ezetimibe+Statin khi giảm thêm LDL-C –NC IMPROVE IT
4. Cập nhật các khuyến cáo mới với sự chấp nhận vai trò của
các NON-STATINS
5. Kết luận
PHÂN TÍCH HỒI QUI ĐA BIẾN ĐỂ ƯỚC LƯỢNG TẦN SUẤT BỊ
NMCT VÀ BỊ ĐMV TÙY THEO CÁC BIẾN SỐ NC KHÁC NHAU
Biến số Nguy cơ mạch máu tương đối
NMCT (n= 107)Bệnh ĐMV (n=74)
Chỉ số khối cơ thể (BMI)
Huyết áp
Đường huyết
Hút thuốc lá
Có tiền sử gia đình
Cholesterol
LDL
TG
VLDL
HDL
.30 kg/m2
160/95mmHg
>150mg/dl
>240 mg/dl
>190mg/dl
>200mg/dl
>30mg/dl
<35mg/dl
1.5
1.9*
3.1**
2.1**
4.2**
4.6**
7.4**
2.8**
2.2**
3.1***
1.5
2.0*
1.9*
1.6
1.9
2.1
3.4***
1.4
1.2
1.5
( Theo Cremer P, nagel D, Seidel D: Gottingen Risk, Incidence and Prevalence Study (GRIPS) 1990)
*p<0.05 **p<0.01 ***p<0.001
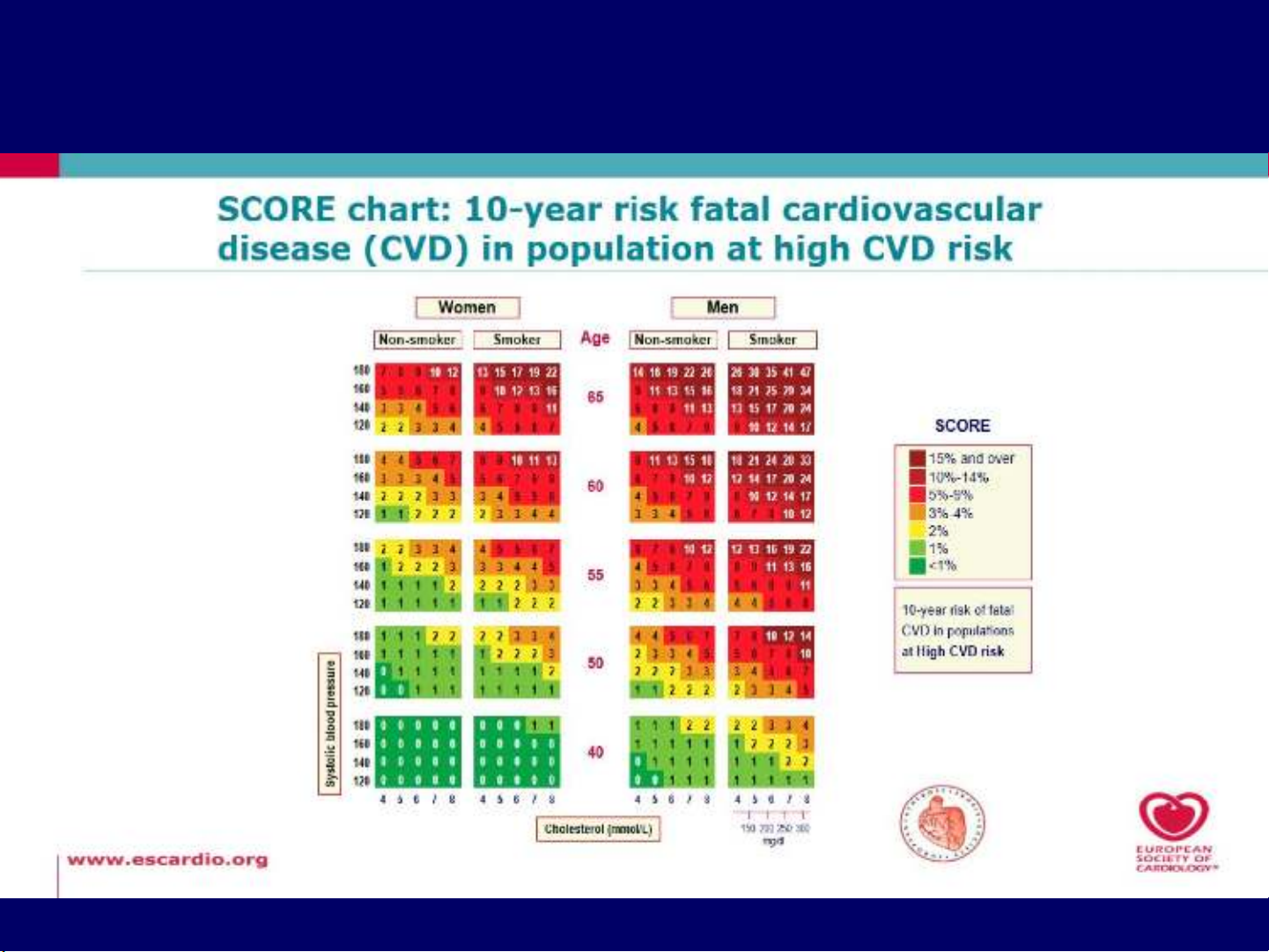
PHÂN TẦNG NGUY CƠ TỬ VONG TIM MẠCH THEO
THANG ĐIỂM SCORE

Nguy
cơ rất
cao
Có
bất kỳ vấn đề sau đây:
Đã được ghi nhận có BMV trên lâm sàng hoặc hình ảnh học rõ
ràng.
BMV lâm sàng bao gồm NMCT cũ,hc MVC, đã làm thủ thuật tái
thông
động mạch vành và các động mạch khác, ĐQ và cơn TIA, phình
ĐMC
và bệnh mạch máu ngoại biên. Ghi nhận BMV trên hình ảnh học
bao
gồm xơ vữa đáng kể trên hình CMV hoặc SA ĐM CẢNH.
Nhưng
KHÔNG bao gồm việc tăng các thông số trên xét nghiệm hình
ảnh
như tăng độ dầy thành động mạch cảnh.
Tiểu đường với tổn thương cơ quan đích bao gồm tiểu đạm hoặc
đi
cùng với các yếu tố nguy cơ chính như hút thuốc lá hoặc
tăng
cholesterol máu hoặc tăng huyết áp.
Bệnh thận mạn nặng (GFR < 30mL/phút/1.73m2)
Điểm SCORE ≥10%.
Nguy cơ cao
Các
đối tượng có vấn đề sau đây:
Tăng đáng kể một yếu tố nguy cơ bao gồm rối loạn lipid
máu
có yếu tố gia đình và tăng huyết áp nặng.
Hầu hết bệnh nhân tiểu đường (một số bệnh nhân trẻ có
tiểu
đường típ 1 có thể ở mức nguy cơ thấp hoặc trung bình).
Điểm SCORE ≥5 % và <10% cho nguy cơ tử vong 10 năm
đối
với BMV.
Nguy cơ trung
bình
Những
đối tượng được xem là nguy cơ trung bình khi SCORE
10
năm
≥1% và < 5 %. Nhiều bệnh nhân độ tuổi trung niên nằm
trong
nhóm
nguy cơ này.
Nguy cơ thấp
Nhóm
nguy cơ thấp dành cho những người có điểm SCORE < 1%
PHÂN TẦNG NGUY CƠ TỬ VONG TIM MẠCH THEO
THANG ĐIỂM SCORE











![Bài ôn tập Giải phẫu răng [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20251005/tuyetnhitk1305@gmail.com/135x160/78741759715471.jpg)





![Bài giảng Glass Ionomer Vương Lam Linh: Tổng hợp kiến thức [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250908/dangkhoa5304@gmail.com/135x160/90151757385750.jpg)





