189
Chương 16
QUANG SINH HỌC
16.1. CƠ CHẾ HẤP THỤ ÁNH SÁNG VÀ PHÁT SÁNG
16.1.1. Định luật hấp thụ ánh sáng
Chiếu một chùm ánh sáng đơn sắc, song
song tới đập vuông góc vào một lớp môi
trường giới hạn bởi hai mặt phẳng song song,
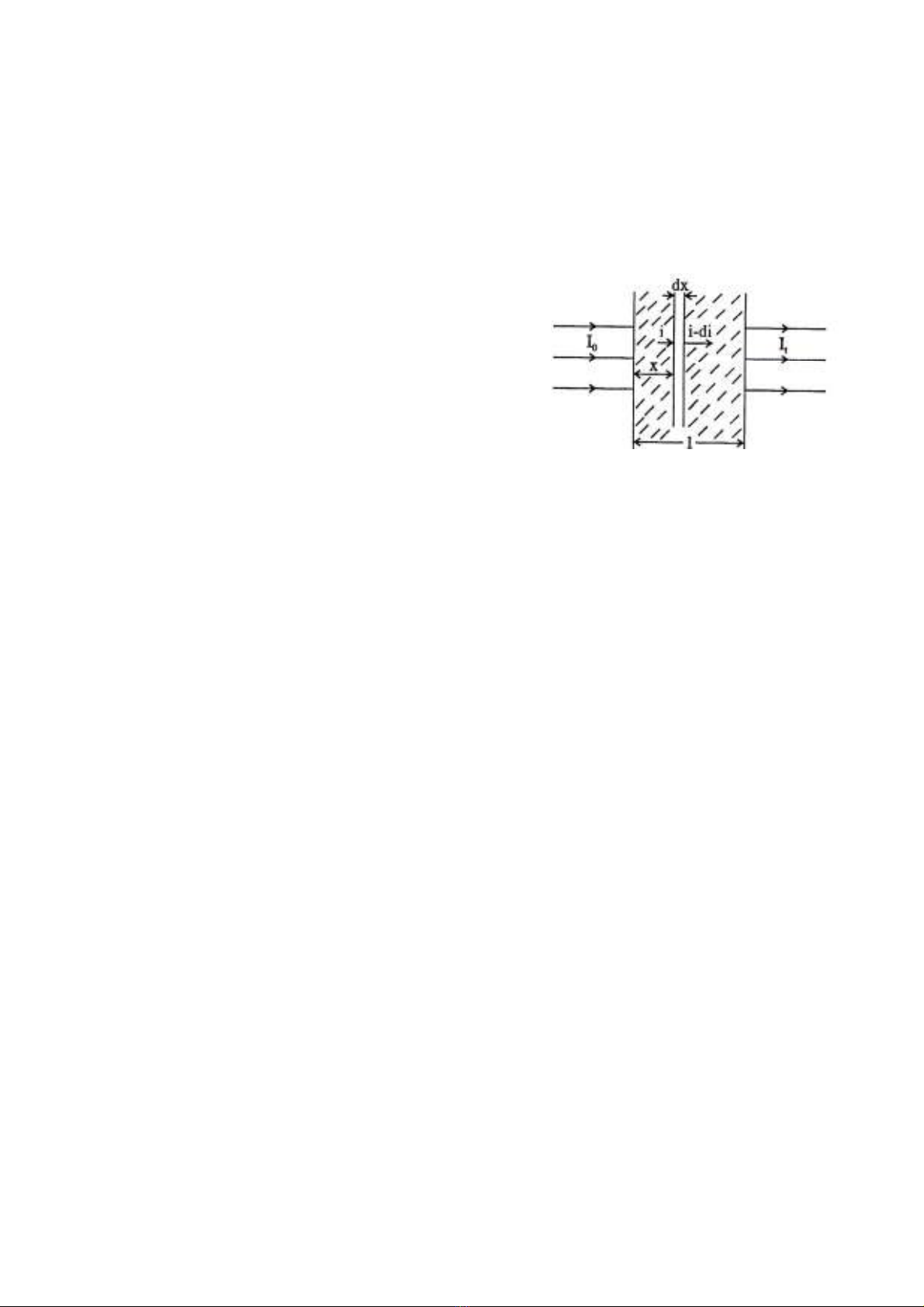
có bề dày l (Hình 16.1)
Gọi cường độ chùm sáng chiếu tới mặt
trước là I0, phần ánh sáng bị phản xạ khi đi tới
mặt phân cách giữa hai môi trường là If, phần ánh sáng bị tán xạ trong môi trường Ix,
phần ánh sáng bị các phân tử hấp thụ là Ih, phần còn lại truyền qua khối môi trường
là It. Theo định luật bảo toàn năng lượng, ta có:
I0 = If + Ix + Ih + It (16.1)
Giả sử mặt ngăn cách của môi trường rất nhẵn, phẳng và các tia sáng tới đập
vuông góc với mặt nên xem như phần ánh sáng phản xạ If không đáng kể.
Môi trường trong suốt va đồng nhất thì ánh sáng bị tán xạ cũng có thể bỏ qua.
Như vậy chỉ còn:
I0 = Ih + It (16.2)
Để xác định trực tiếp phần năng lượng ánh sáng bị phân tử môi trường hấp
thụ thì rất khó, tuy vậy có thể xác định Ih gián tiếp qua việc đo I0 và It. Định luật
Bugơ - Lambe - Bia (Bouguer - Lambert - Bear) cho ta mối liên quan giữa I0 và It.
Giả sử ta xét một lớp môi trường có bề dày dx, cách mặt trước của môi
trường là x. Gọi i là cường độ chùm sáng khi đi tới mặt dx, (i-di) là cường độ chùm
sáng khi đi ra khỏi lớp dx. Như vậy, khi đi qua lớp đơn xin, cường độ chùm sáng đã
giảm đi một lượng là - di. Độ giảm -di của cường độ chùm sáng tỷ lệ với i và độ dày
dx, ta có:
- di ~ i, dx
Vậy: - di = k.i.dx (16.3)
Hình 16.1

190
Trong đó k là một hệ số tỉ lệ, gọi là hệ số hấp thụ của môi trường, k phụ
thuộc vào bản chất, mật độ môi trường, vào bước sóng ánh sáng.
Giải phương trình vi phân (16.3):
It = I0.e-kl (16.4)
Biểu thức (4) chính là biểu thức toán học của định luật Bugơ - Lambe.
Khi chuyển từ cơ số tự nhiên (e) sang cơ số thập phân (10) thì biểu thức (4)
trở thành:
It = I0.10-k'l (16.5)
Trong đó k' gọi là hệ số tắt, k' = 0.43k.
Nếu x
0
I1
=
I10
thì k' = x
1, vậy hệ số tắt có giá trị bằng nghịch đảo bề dày mà với
nó cường độ ánh sáng yếu đi 10 lần.
Trong trường hợp môi trường hấp thụ ánh sáng là dung dịch loãng nồng độ
bằng C, ta thấy hệ số tắt k' tỷ lệ thuận với C.
k' = C.
ε
(16.6)
ε
là hệ số tắt của dung dịch. Hệ số
ε
không phụ thuộc vào nồng độ, chỉ phụ
thuộc vào bản chất của chất tan, vào bước sóng (
λ
) của ánh sáng chiếu vào dung dịch.
Phối hợp các biểu thức (16.5) và (16.6) ta được phương trình biểu diễn định
luật cơ bản của sự hấp thụ ánh sáng, định luật Bugơ- Lambe- Bia:
It = I0.10 lC..
ε
− (16.7)
Định luật này chứng tỏ hệ số hấp thụ của một chất tỷ lệ thuận với khối lượng
lớp môi trường mà ánh sáng đi qua, tức là tỷ lệ thuận với số phân tử chất hấp thụ
trên một đơn vị độ dài của đường truyền sáng. Ý nghĩa vật lý của định luật là khả
năng hấp thụ ánh sáng của một phân tử nào đó không phụ thuộc vào sự có mặt cảu
các phân tử khác ở xung quanh nó. Rõ ràng điều này chỉ đúng với các dung dịch
loãng. Khi nồng độ dung dịch tăng, khoảng cách giữa các phân tử giảm, tương tác
giữa các phân tử không đáng kể, ta thấy có nhiều sai khác so với định luật Bugơ -
Lambe - Bia. Ngoài ra, trong nhiều trường hợp
ε
không chỉ phụ thuộc vào chất tan
mà còn phụ thuộc vào dung môi. Điều này chứng tỏ sự tương tác giữa các phân tử
chất tan và các phân tử dung môi cũng ảnh hưởng đến sự hấp thụ dung dịch.
Vậy điều kiện để áp dụng định luật hấp thụ ánh sáng là:

191
- Chùm sáng phải đơn sắc.
- Dung dịch đo phải loãng (nằm trong khoảng nồng độ thich hợp).
- Dung dịch phải trong suốt (trừ chuẩn độ đo quang).
- Chất thử phải bền trong dung dịch và bền dưới tác dụng của ánh sáng UV-VIS.
* Một số đại lượng thông dụng
- Độ truyền qua (T-Transmittance)
Độ truyền qua (hay còn gọi là độ thấu quang) đặc trưng cho độ trong suốt (về
mặt quang học) của dung dịch, được định nghĩa:
T= -ε.C.l
t
0
I=10
I (16.8)
Thường T tính ra phần trăm (%). Một chất cho T=1 (hay 100%), nghĩa là
hoàn toàn không hấp thụ ánh sáng, người ta nói chất đó trong suốt hoàn toàn.
- Độ hấp thụ
Độ hấp thụ (hay còn gọi là mật độ quang D - Density, hoặc độ tắt E -
Extinction) được định nghĩa:
A(D,E) = lg lC
T..
1
ε
= (16.9)
Đối với một chất xác định (có
ε
xác định), thường đo trên một loại cốc đo (có
bề dày thông thường l =1 cm) như vậy độ hấp thụ tỷ lệ thuận với nồng độ dung dịch:
A = K.C (K=
ε
.l) (16.10)
Đây chính là cơ sở lý thuyết của phương pháp định lượng bằng quang phổ
hấp thụ.
- Hệ số hấp thụ phần trăm (E cm1
%1 )
Theo công thức A =
ε
.C.l, nếu l = 1cm, C=1% thì
A =
ε
= E cm1
%1 ( thường viết tắt là E11)
Vậy E11 chính là độ hấp thụ của dung dịch có nồng độ 1%, dùng cốc đo có bề
dày 1 cm. Với một chất tan xác định, tại một
λ
xác định, E11 là một hằng số.
- Hệ số hấp thụ phân tử (
μ
ε
)
Hệ số hấp thụ phân tử, hay còn gọi là hệ số tắt mol, là độ hấp thụ của dung
dịch có nồng độ 1 M/l, dùng cốc đo có đọ dày 1cm.

192
Cũng như E11, với một chất xác định, trong những điều kiện đo xác định (
λ
,
dung môi, nhiệt độ ....),
μ
ε
là một hằng số.
Giữa E11 và
μ
ε
có mối liên hệ:
1
1
μ
E
ε=.M
10 (16.11)
Ở đây M là phân tử gam của chất tan.
16.1.2. Ứng dụng quang phổ hấp thụ phân tử
Đa số các chất trong suốt có hệ số hấp thụ k (cũng có nghĩa là độ hấp thụ A)
thay đổi theo bước sóng (
λ
). Những chất đó gọi là các chất hấp thụ lọc lựa. Đường
cong biểu diễn sự phụ thuộc của độ hấp thụ (A) của một chất vào bước sóng ánh
sáng chiếu vào nó, gọi là phổ hấp thụ của chất đó.
(k,
ε
, A, D) = f(
λ
) (16.12)
Phổ hấp thụ của mỗi chất được đặc trưng bỏi hình dạng đường cong hấp thụ,
số lượng, vị trí và cường độ của các cực đại.
Ngày nay phương pháp quang phổ hấp thụ phân tử (bao gồm phổ tử ngoại,
khả kiến, hồng ngoại - UV, VIS, IR) đã trở thành một phương pháp phân tích thông
dụng trong các phòng thí nghiệm ở các cơ sở nghiên cứu, trường học, trạm kiểm
nghiệm, xí nghiệp sản xuất dược phẩm…Sở dĩ như vậy vì phương pháp này có
những ưu điểm chính sau:
1. Độ chính xác (precision), độ lặp lại (reproducibility) của phương pháp khá cao.
2. Sai số tương đối của phương pháp (UV-VIS) nhỏ, thường vào khoảng 0,5-1%.
3. Độ nhạy cao của phương pháp giúp có thể phân tích được các dung dịch
loãng cỡ 10-4
μ
g/l (cỡ cài chục
μ
g/ml) rất thích hợp cho các phép phân tích vết
(phân tích độc chất)
4. Thời gian phân tích nhanh chóng, chỉ cần 5-10 phút có thể cho biết ngay
kết quả.
5. Kỹ thuật thao tác đơn giản, máy móc ngày càng hoàn thiện, gon nhẹ, trình
độ tự động hoá, tin học hoá cao.
Dưới đây chỉ giới thiệu một cách ngắn gọn một số lĩnh vực áp dụng của phổ
hấp thụ phân tử trong ngành Dược.
16.1.2.1. Phân tích định tính

193
Cơ sở lý luận của phương pháp phân tích quang phổ hấp thụ phân tử là sự
phụ thuộc giữa phổ của một chất vào cấu trúc hoá học của nó (cụ thể là cấu trúc của
lớp vỏ phân tử, của các mối liên kết, của các nhóm chức và của cấu hình không gian
của phân tử…).Vì thế, nếu có hai chất được đo trong những điều kiện hoàn toàn như
nhau mà cho phổ (đặc biệt là phổ IR) hoàn toàn giống nhau thì có thể xem hai chất
đó có cấu trúc hoá học như nhau.
Để phân tích phổ, người ta dựa vào các chỉ tiêu:
- Bước sóng hấp thụ cực đại:
λ
max (với phổ IR thường dùng đại lượng là số
sóng: 1
ν
λ
= (cm-1). Ví dụ, phổ của dung dịch vitamin B12 (cyanocobalamin) trong
nước có các
λ
max = 278; 361; 548 nm. Phổ của dung dịch vitamin B2 (riboflavn)
trong nước có
λ
max = 223; 267; 375 và 444 nm.
- Dựa vào tỷ số độ hấp thụ tại các cực đại hoặc tại cực đại với cực tiểu hấp
thụ. Thí dụ, với vitamin B12 ta có tỷ số A278/A361 = 0.57; A548/A361 = 0.30.
Trong thực tế thường tiến hành so sánh phổ của chất khảo sát với phổ của
chất chuẩn được đo trong những điều kiện như nhau, hoặc so sánh với phổ đã được
công bố trong các tài liệu nghiên cứu (catalogue chuyên đề …). Hiện nay việc dùng
phổ hấp thụ hồng ngoại để phân tích có nhiều ưu việt hơn dùng phổ tử ngoại, khả
biến, vì phổ IR cho lượng thông tin nhiều hơn (phổ IR của một chất thường có vài
chục đỉnh hấp thụ cực đại, trong khi phổ UV và VIS thường chỉ có một và
λ
max).
Phân tích cấu trúc của một chất không thể thiếu được phương pháp phổ IR.
16.1.2.2. Phân tích định lượng
Định lượng là lĩnh vực ứng dụng chủ yếu của phương pháp phổ UV và VIS.
Nhiều chuyên luận trong Dược điển đã dùng phương pháp này để định lượng các
hoạt chất.
Cơ sở của phương pháp là dựa vào công thức:
A =
ε
.C.l
Có nhiều kỹ thuật định lượng bằng phổ UV và VIS:
- Phương pháp đo trực tiếp
- Phương pháp so sánh.


![Giáo trình Thực hành Vật lý đại cương Phần 2: [Mô tả chi tiết nội dung/chủ đề]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260306/hoaphuong0906/135x160/84291773037096.jpg)
![Giáo trình Thực hành Vật lý đại cương Phần 1: [Mô tả/Định tính Thêm Nếu Cần]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260306/hoaphuong0906/135x160/48081773037097.jpg)
![Vật Lý Đại Cương 2: Tổng hợp lý thuyết, công thức, bài tập trắc nghiệm và tự luận [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250212/tuetuebinhan666/135x160/740265305.jpg)
![Giáo trình thực hành Vật lý đại cương Trường ĐH Thủ Dầu Một [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230629/chankora09/135x160/1801688034123.jpg)
![Bài giảng Vật lý đại cương: Phần 2 - Trường ĐH Võ Trường Toản [Tài liệu chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230606/loivokiet/135x160/476896379.jpg)















![Đề thi học kì 2 môn Vật lí 1 năm 2023-2024 có đáp án [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/64291778553454.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2023-2024 có đáp án [Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/1381778553461.jpg)
![Đề thi học kì 2 Vật lí 1 năm 2022-2023 có đáp án [kèm PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260507/hoahongxanh0906/135x160/21778553462.jpg)

