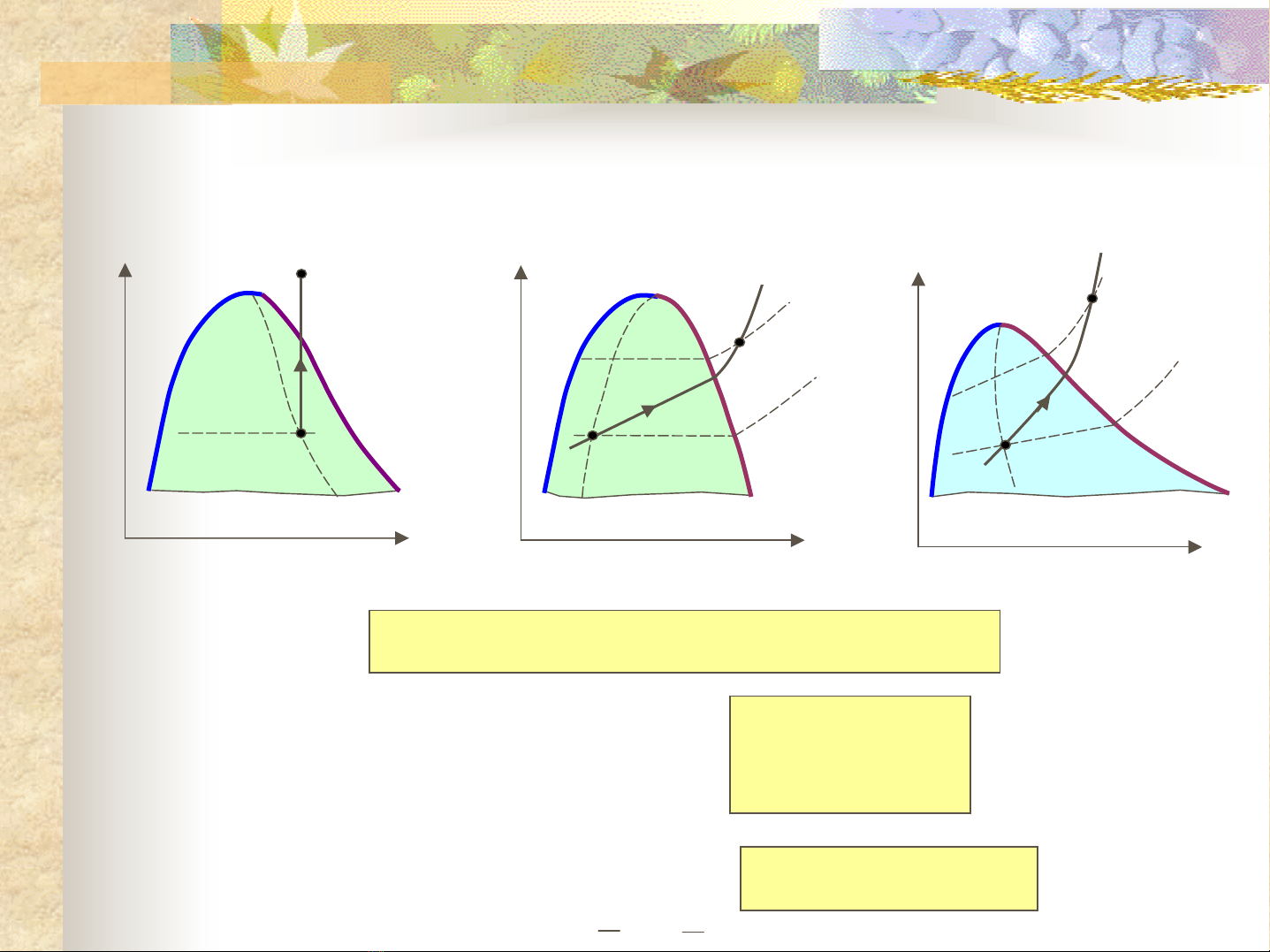
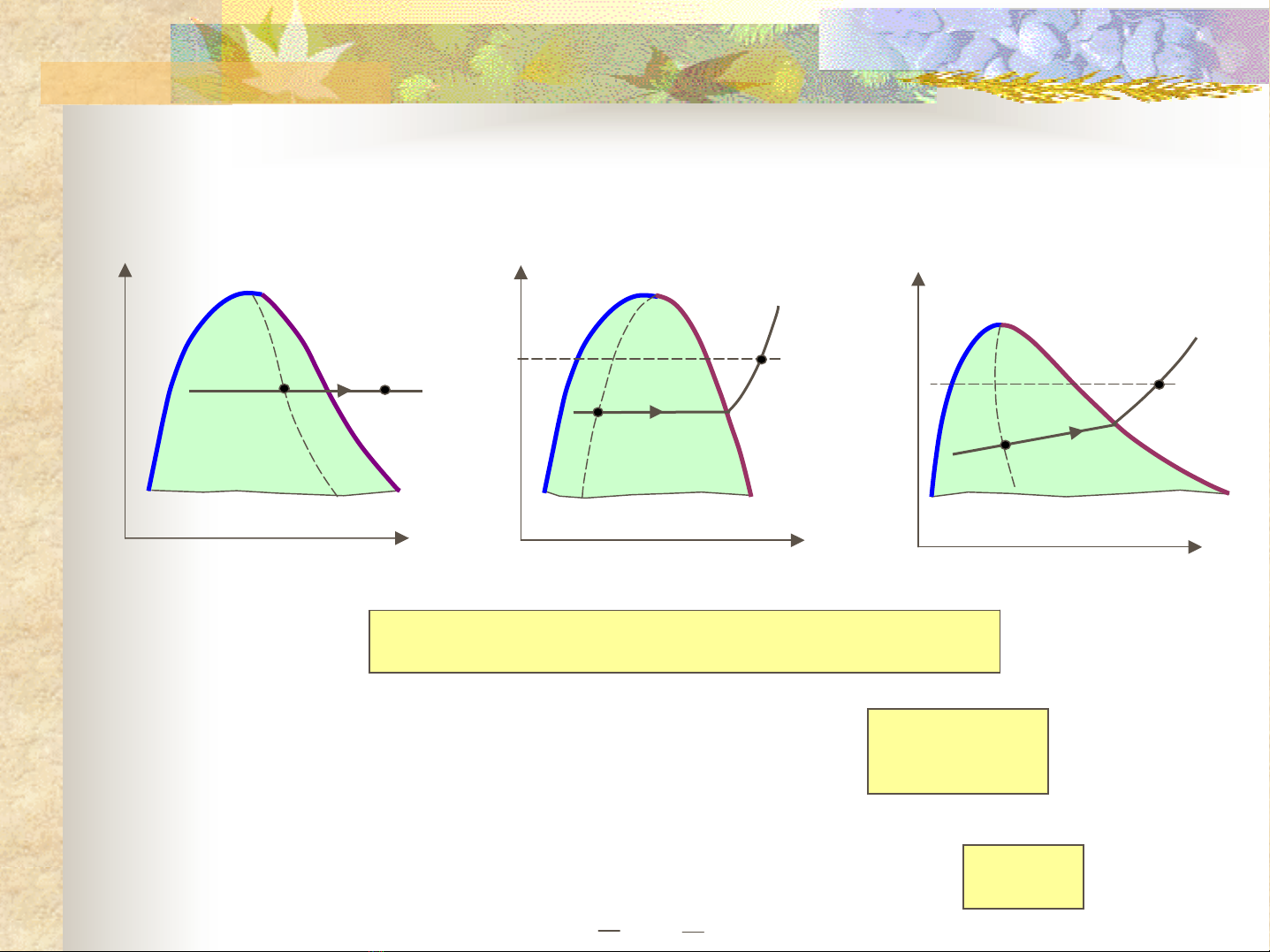
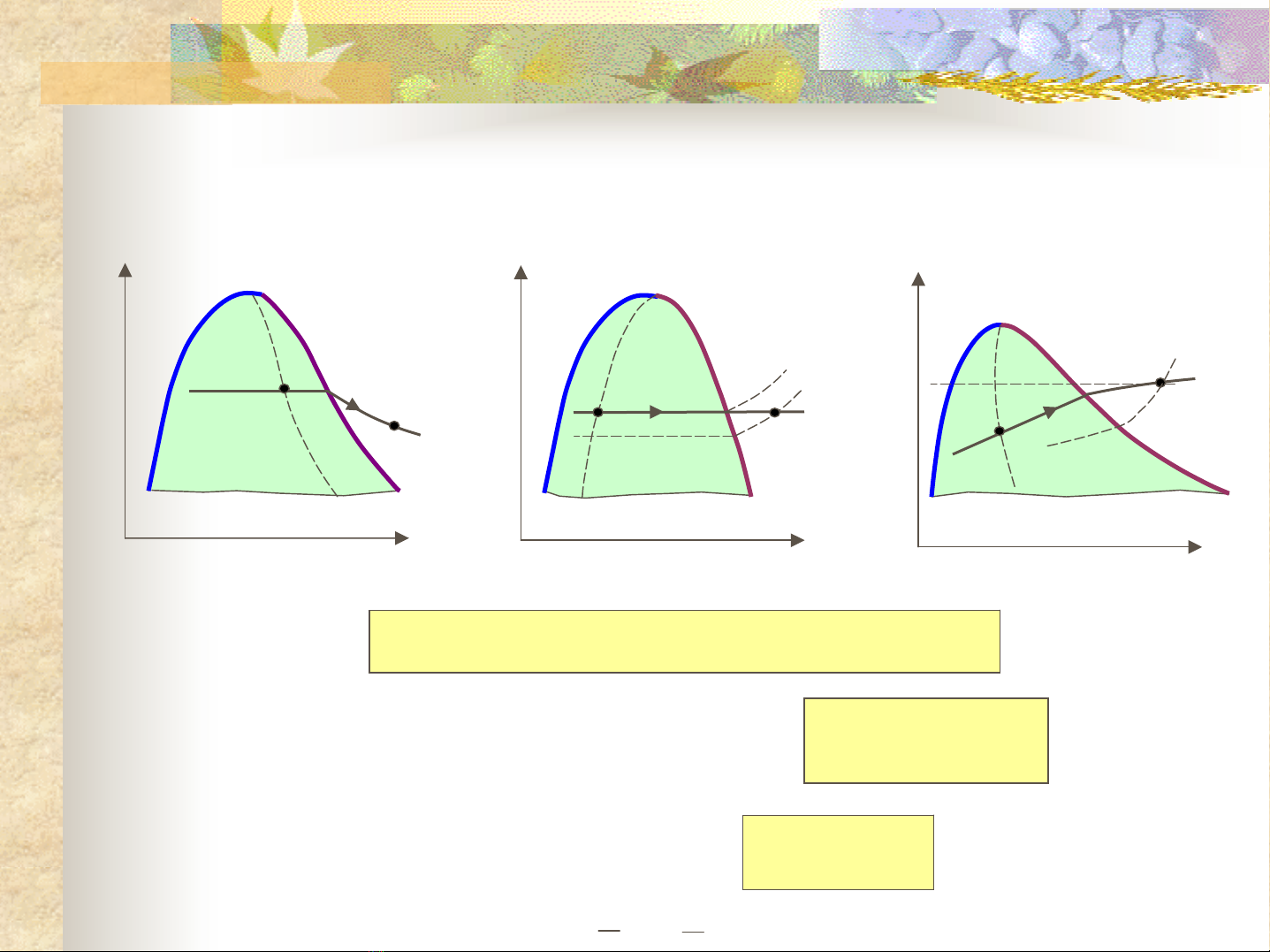
5.4 Các quá trình nhiệt động cơ bảncủa CTK
* Chú ý: CTK (ví dụ nước) ở trạng thái hơi là khí thựcÆkhông thểdùng
pt Khí lý tưởng
Bảng nước chưa
sôi và hơi quá nhiệt
Bảng hơi nước
bão hòa ẩm
HOẶC
Bảng hơi
nước bão
hòa ẩm
Trạng thái
-Lỏng chưa sôi
-Hơi bão hòa ẩm
-Hơi quá nhiệt
hay
hay
Các thông sốtrạng thái: p, T, v, i, s
Bước 2:Dựa vào đặc tính quá trình
+ Định luật Nhiệt động 1
Công W và
Nhiệt Q tham gia
trong quá trình
Bước 1: xác định các thông số trạng thái của quá trình: dùng BẢNG
Người soạn: TS. Hà anh Tùng
ĐHBK tp HCM
1/2009
p.2
p.2