
Phương Pháp Oxy Hóa – Khử
Redox Titrations, Titrations Based on Redox Reactions
PGS.TS. Nguyễn Đức Tuấn
Bộ môn Hóa Phân Tích – Kiểm Nghiệm
Khoa Dược – Đại học Y Dược TPHCM
Nguyễn Đức Tuấn Đại học Y Dược TPHCM

Phương Pháp Oxy Hóa – Khử
Mục tiêu
Trnh byđượcđịnh nghĩa phản ứng oxy hóa -khử;thế oxy hóa -khử và thế oxy
hóa – khử chuẩn;thế oxy hóa – khử hòa tan và thế chuẩn của cặp oxy hóa – khử hòa
tan; thế oxy hóa – khử biểu kiến và thế oxy hóa – khử chuẩn biểu kiến;ảnh hưởng của
pH, của sự tạo tủa và tạo phức trên thế oxy hóa -khử
Tính được hằng số cân bằng Kđể từ đó dự đoán chiều của phản ứng oxy hóa -
khử, thế oxy hóa -khử tại điểm tương đương và thế oxy hóa – khử tại từng thời điểm
chuẩn độ để từ đó vẽ được đường cong chuẩn độ oxy hóa – khử
Chọn được chỉ thị oxy hóa -khử dựa theo đường cong chuẩn độ oxy hóa -khử
Áp dụng được các phương pháp oxy hóa – khử để định lượng một số chất thường
được sử dụng trong ngành Dược
Đại học Y Dược TPHCMNguyễn Đức Tuấn

Phương Pháp Oxy Hóa – Khử
Nội dung
1. Sự oxy hóa – khử
2. Phương pháp chuẩn độ oxy hóa – khử
3. Một số phép đo oxy hóa – khử sử dụng trong ngành Dược
Đại học Y Dược TPHCMNguyễn Đức Tuấn
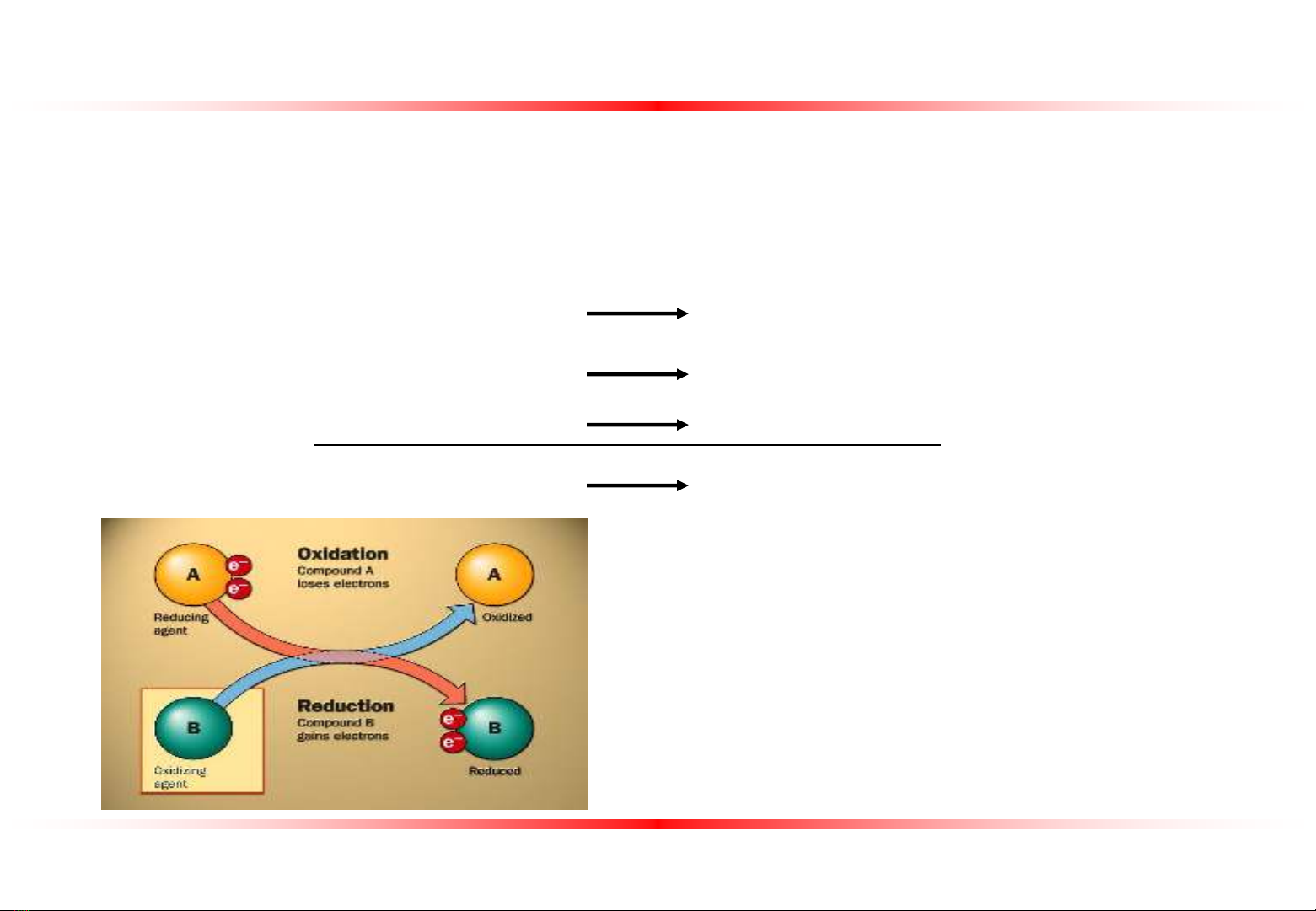
Sự Oxy Hóa – Khử
Phản ứng oxy hóa – khử là phản ứng trao đổi electron giữa hai hợp chất:một hợp chất
nhường electron (chất khử) và một hợp chất nhận electron (chất oxy hóa)
Đại học Y Dược TPHCM
•Sự oxy hóa:sự mất e-
•Sự khử:sự nhận e-
•Khi có sự oxy hóaxảyra là có sự khử và mi
e-nhậnđượcbởichất oxy hóalà do chấtkhử
bị mấtđi
Th d: Thêm dd st (III) clorid vothic (II) clorid
2FeCl3+ SnCl22FeCl2+ SnCl4
2Fe3+ + 2e 2Fe2+
Sn2+ - 2e Sn4+
2Fe3+ +Sn2+ 2Fe2+ +Sn4+
Nguyễn Đức Tuấn
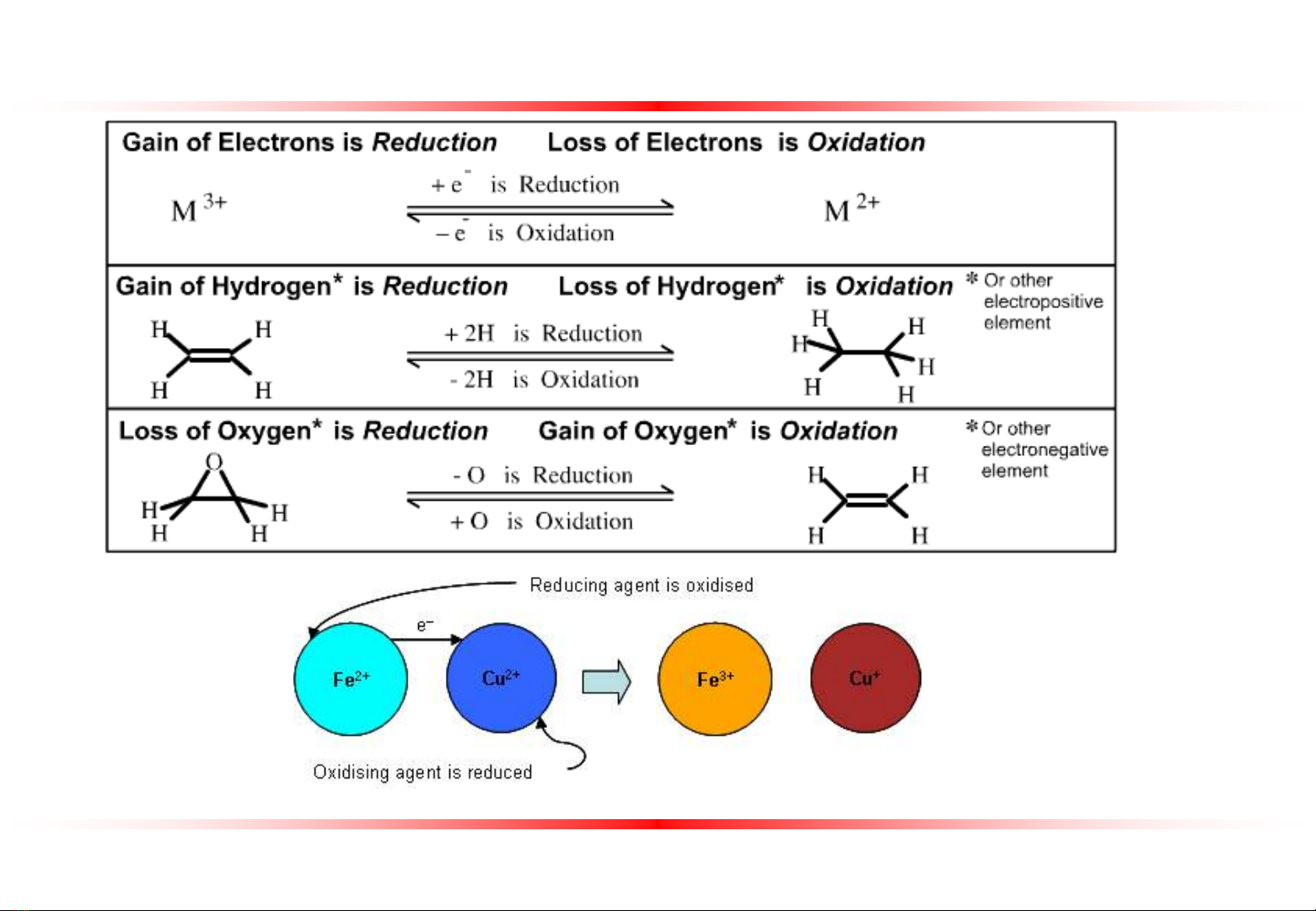
Sự Oxy Hóa – Khử
Đại học Y Dược TPHCM
http://www.meta-synthesis.com/webbook/15_redox/redox_06.gif
Nguyễn Đức Tuấn








![Bài giảng Hóa phân tích TS. Lê Thị Hải Yến: Tổng hợp kiến thức [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2023/20230607/phuong3129/135x160/2361686125460.jpg)











![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



