
HÓA HỌC: NGHỆ THUẬT, KHOA HỌC VÀ NHỮNG BẤT NGỜ THÚ VỊ
BÀI THI LÝ THUYẾT
ĐÁP ÁN VÀ THANG ĐIỂM
NGÀY 20 THÁNG 7, 2007
MATXCƠVA, NGA
Official English version
Simpo PDF Merge and Split Unregistered Version - http://www.simpopdf.com
2
Bài
1.
Hiệu ứng đường hầm đối với proton
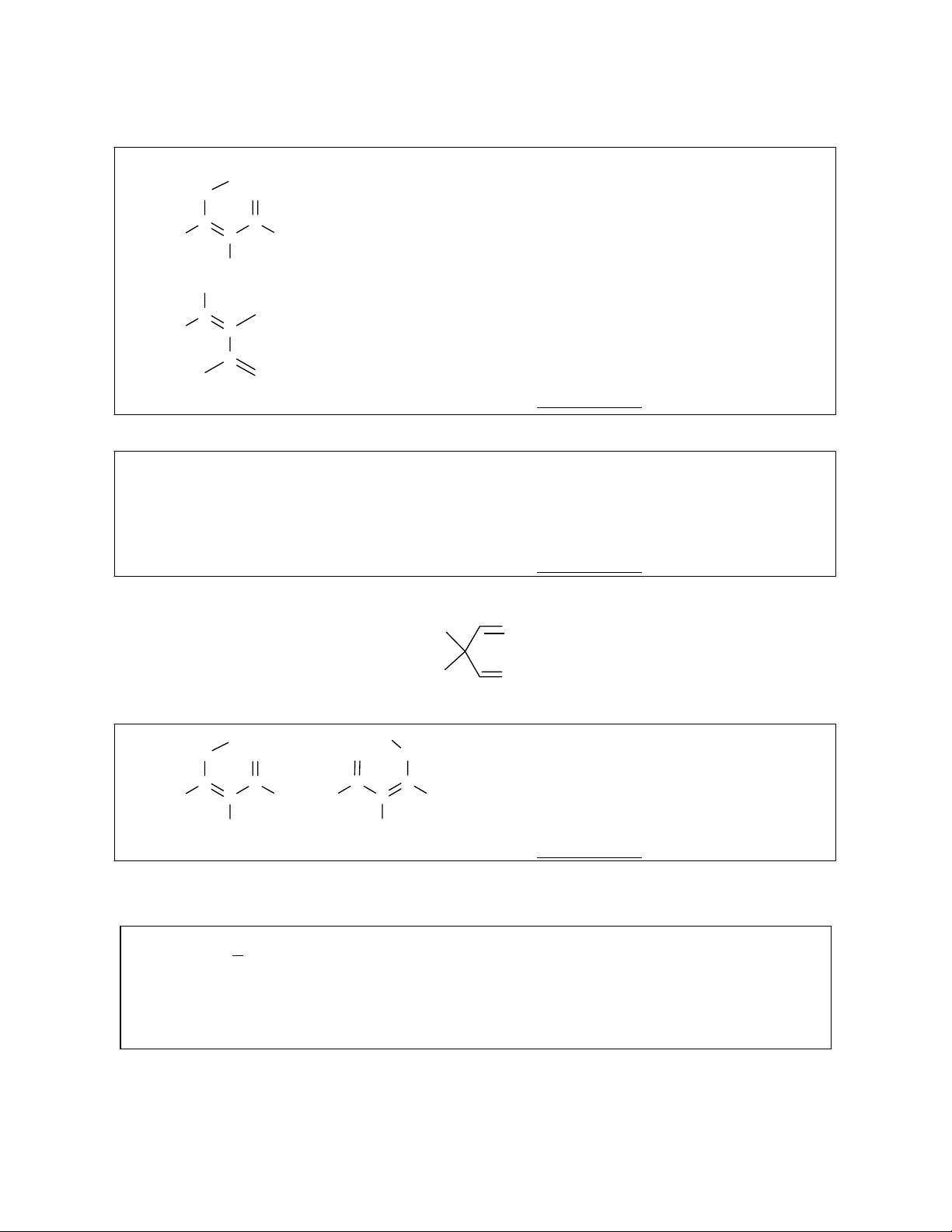
1.1.1 Cấu trúc của propandial và hai đồng phân của nó
O=CH−CH
2
−CH=O 1 mark
H
O O
C C
H C H
H
OH
C H
H C
C
1 mark
H O 1 mark
Tối đa 3 marks
1.1.2
Nguyên tử hydro axit của nhóm CH
2
(ở dạng enol thì nguyên tử hydro axit của nhóm OH).
1 mark
Tính axit của nhóm СН
2
được gây nên bởi sự ổn định của cacbanion liên hợp với hai nhóm cacbonyl
Câu trả lời thứ nhất là câu đúng.
2 marks
Tối đa 3 marks
1.2.1 Khoảng cách giữa hai cực tiểu trên đường cong năng lượng là 0,06nm. Đó là dạng andehit
H
O
H O
khoảng cách giữa hai proton ở dạng này là không khả thi. Hiệu ứng đường hầm chỉ xảy ra duy nhất ở
dạng enol – Z:
H H
O O O O
C C
H C H
H
C C
H C H
H
1 mark cho mỗi cấu trúc
Tối đa 2 marks
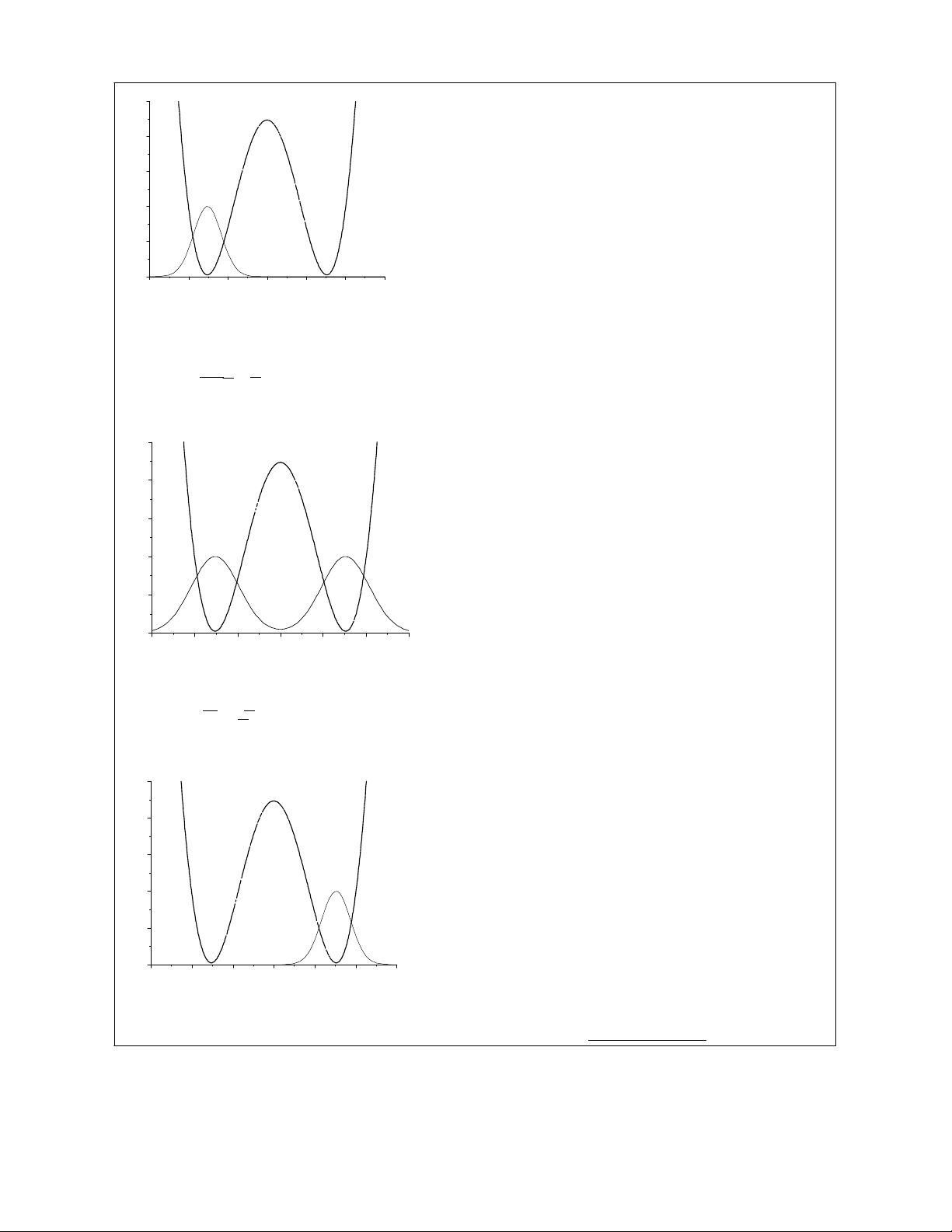
1.3.1 Biểu thức và đồ thị cho mật độ xác suất
[]
)()()()()(
2
1
)0,()( 222222 xxxxxxa LRLRL Ψ=Ψ−Ψ+Ψ+Ψ=Ψ 1 mark
Khả năng tìm thấy proton tập trung chủ yếu ở giếng bên trái
Simpo PDF Merge and Split Unregistered Version - http://www.simpopdf.com
3
Ψ
2
L
-0,06
-0,04
-0,02
0,00
0,02
0
,
04
0,06
L
Khoảng cách
nm
R
0.5 marks
(b) Vào khoảng giữa thời gian ta có
1 mark
Đồ thị mật độ xác suất có dạng đối xứng, proton dao động giữa hai giếng:
(
Ψ
2
+
Ψ
2
)
/2
L
R
-0,06
-0,04
-0,02
0,00
0,02
0
,
04
0,06
L
Khoảng cách,
nm
R
0.5 marks
Xác suất tìm thấy proton tập trung ở giếng bên phải:
Ψ
2
R
-0,06
-0,04
-0,02
0,00
0,02
0,04
0,06
L
Khoảng cách,
nm
R
0.5 marks
Tối đa 4.5 marks
1.3.2
Xác suất tìm thấy proton ở giếng bên trái là 1/2, do hàm mật độ xác suất có dạng đối xứng và
cả hai giếng đều đồng nhất.
2 marks
[]
)()(
2
1
2
,222 xxx RL Ψ+Ψ=
⎟
⎠
⎞
⎜
⎝
⎛
Ψ
ω
π
[]
)()()()()(
2
1
,)( 222222 xxxxxxc RRLRL Ψ=Ψ+Ψ−Ψ+Ψ=
⎟
⎠
⎞
⎜
⎝
⎛
Ψ
ω
π
1 mark
Simpo PDF Merge and Split Unregistered Version - http://www.simpopdf.com

4
=
1.3.3 Thời gian di chuyển từ một giếng sang một giếng khác là t = π / ω.
t =
3.14
4.85
×
10
−
12
s. 2 marks
6.48
×
10
11
Vận tốc proton:
0.06
×
10
−
9
V = = 12
4.85
×
10
−
12
m/s. 2 marks
Tối đa 4 marks
1.3.4
Độ bất định về vị trí của proton xấp xỉ bằng một nửa khoảng cách giữa hai cực tiểu là 0.03 nm (cũng
chấp nhận giá trị 0.06).
1 mark
Độ bất định cực tiểu về vận tốc có thể nhận được từ nguyên lý bất định:
So sánh độ bất định vận tốc với đáp số câu trên là 12m/s ta thấy rằng ý định xác định vận tốc proton
trong quá trình di chuyển giữa các giếng thế là không khả thi. Như vậy đường hầm proton là một hiện
tượng thuần túy lượng tử và không thể được giải thích bằng lý thuyết kinh điển. Câu trả lời thứ
hai là chính xác
2 marks
Tối đa 6 marks
sm
xm
V/1000
10.03,0.
10.02,6
001,0
.2
10.055,1
29
23
34
≈=
∆
=∆
−
−
h 3 marks
Simpo PDF Merge and Split Unregistered Version - http://www.simpopdf.com

5
a
a a a
Bài
2.
Hóa học nano
2.1.1
Năng lượng Gibbs và hằng số cân bằng của phản ứng (1)
∆rGo500 = ∆Gof, 500(CoO,r) - ∆Gof, 500(H2O,k)= -198,4 + 219,4 = 20,7kJ/mol
0
0
0
0
0.5 marks
−
∆
r
G
500
(1)
−
20700
K
=
e
RT
=
e
8.3
=
14
×
500
6.88
10
−
3
×
0.5 marks
1 mark maximum
2.1.2
Năng lượng Gibbs cho phản ứng (1) với tiểu phân coban nano hình cầu có bán kính r
a
là
đối với các tiểu phân hình cầu có r
a
= 10
–8
, 10
–9
m tương ứng ta có
2σ
Co-gas
V (Co)
r
a
o
= 210 và 2100 J/mol.
∆
r
G
500
(1, r
a
) bằng 20.5 (a), và 18.6 (b) kJ/mol.
Hằng số cân bằng đựơc tính từ phương trình sau
K
(1,
r
)
=
7.22
×
10
−
3
;
r
=
10
−
8
m
K
(1,
r
)
=
11.4
×
10
−
3
;
r
=
10
−
9
m
Tối đa 2 marks
∆rGo500 (1, ra) = Gokhối, 500(CoO,r)+Go 500(H2,k) - Go500(H2O,k) - Gocầu(Co) =
= Go 500(CoO,r)+Go 500(H2,k) - Go500(H2O,k) - =+ −
a
kCo
o
r
CoV
rCoG )(2
),(
500
σ
= ∆rGo500 -
a
kCo
r
CoV )(2 −
σ
molm
M
CoV
Co
Co /10.6,6
9,8
10.0,59
)( 36
6−
−
===
ρ
⎟
⎟
⎠
⎞
⎜
⎜
⎝
⎛∆
−= RT
rG
rK a
o
r
o
),1(
exp),1( 500
Simpo PDF Merge and Split Unregistered Version - http://www.simpopdf.com























![Tài liệu tham khảo Tiếng Anh lớp 8 [mới nhất/hay nhất/chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250806/anhvan.knndl.htc@gmail.com/135x160/54311754535084.jpg)










![Phiếu bài tập cuối tuần Tiếng Việt 1 tuần 2 đề 2: [Hướng dẫn chi tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250728/thanhha01/135x160/42951755577464.jpg)

