ĐỊNH LƢỢNG ACID AMIN MÁU VÀ DỊCH SINH HỌC BẰNG MÁY
SẮC KÝ LỎNG SIÊU HIỆU NĂNG (UPLC)
I. NGUYÊN LÝ
- Mẫu thử được khử protein bằng dung dịch acid sulfosalicylic (SSA) chứa
nội chuẩn norvaline (Nva). Phương pháp phân tích acid amin bao gồm các
giai đoạn sau:
o Kiềm hoá mẫu chuẩn, mẫu thử, mẫu trắng (blank) đã được khử tạp bởi
SSA bằng dung dịch NaOH/ borat.
o Phản ứng tạo dẫn xuất:
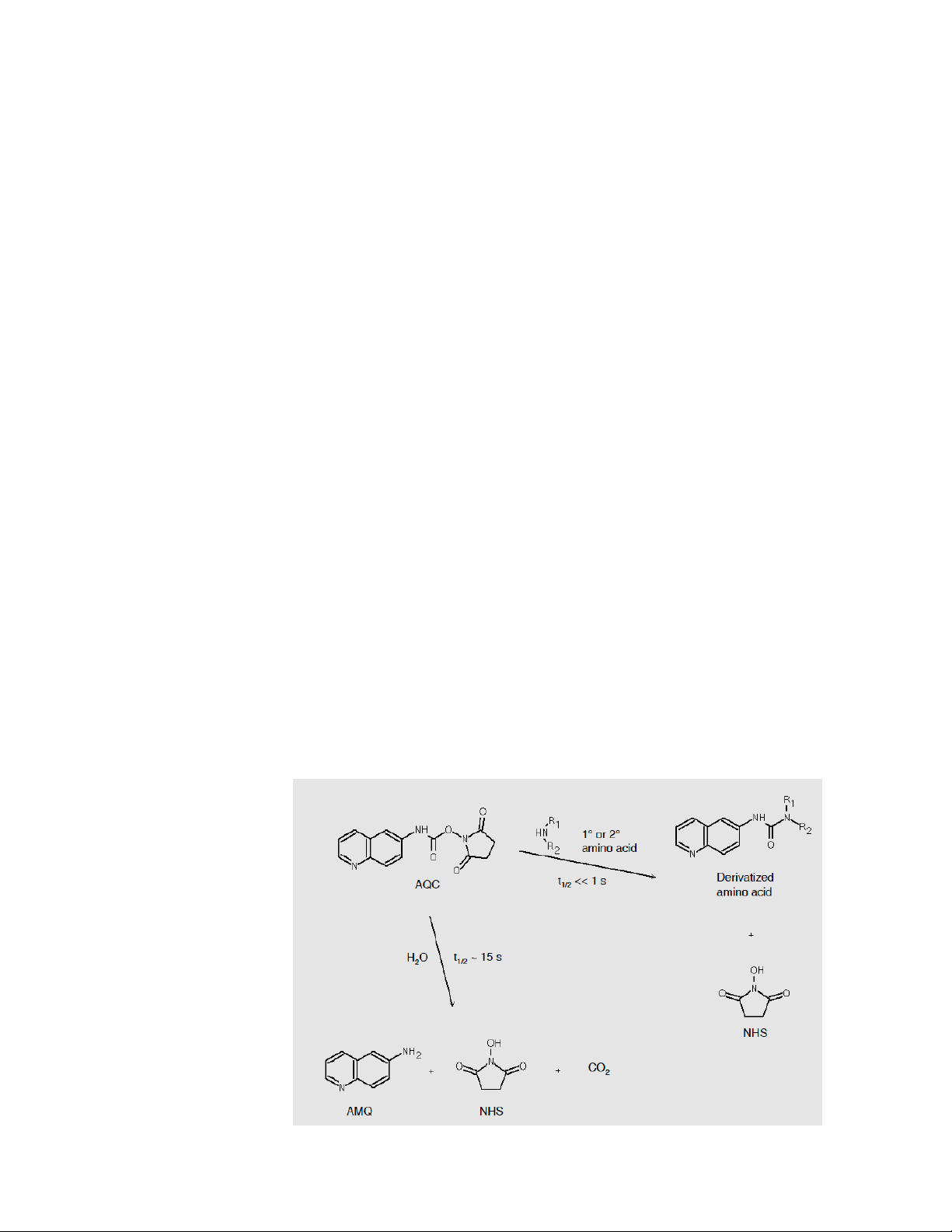
- Dẫn xuất hoá các acid amin trong mẫu thử bằng AQC (6-aminoquinolyl-N-
hydroxysuccinimidyl carbamate) để chuyển các acid amin bậc một và bậc hai
thành các chất có thể phát hiện được bằng đầu dò cực tím (UV).
- Phản ứng tạo dẫn xuất hoàn toàn đòi hỏi một lượng dư số mol AQC.
Lượng dư này sẽ bị thủy phân thành sản phẩm phụ là 6-aminoquinoline
(AMQ), N-hydroxysuccinimide (NSH) và CO2, những sản phẩm phụ này
không gây cản trở cho quá trình phân tích. Riêng AMQ sẽ tạo ra một peak
có ý nghĩa và dễ dàng nhận biết được. Phản ứng thủy phân này xảy ra
chậm hơn so với phản ứng tạo dẫn xuất.
- Lưu ý: Creatinin không được dẫn xuất bởi thuốc thử AMQ nên sẽ không
xuất hiện peak sắc ký đối với creatinin. Riêng urê sẽ được dẫn xuất kép
(do cấu tạo phân tử đặc biệt) để tạo nên dẫn xuất urê đối xứng. Peak của
urê sẽ được đánh dấu bằng chữ “Derivation Peak” trên sắc ký đồ.
- Phân tách các dẫn xuất AQC của acid amin bằng phương pháp UPLC,
định lượng bằng đầu dò TUV.
* Phản ứng tạo dẫn xuất
- Hệ thống UPLC ứng dụng trong phân tích acid amin có đặc điểm: sử dụng
áp suất cao chạy trên các cột phân tích có kích thước tiểu phần 1,7µm,
đường kính cột 2,1mm, chiều dài cột 150mm. Hệ thống cho phép phát hiện
và định lượng 42 loại acid amin phổ biến và các hợp chất có liên quan với
tốc độ 45 phút/ mẫu. Thời gian phân tích được rút ngắn trong khi độ nhạy,
độ đặc hiệu và hiệu năng phân tách được cải thiện là ưu điểm của hệ thống
UPLC so với các phương pháp khác.
II. CHUẨN BỊ
1. Ngƣời thực hiện
Người thực hiện kỹ thuật có trình độ phù hợp
2. Phƣơng tiện, hóa chất
2.1. Phương tiện:
o ACQUITY UPLC System: Hệ thống bao gồm:
Hệ thống bơm cao áp và quản lý dung môi
Bộ quản lý dung môi bốn dòng dung môi
Bộ quản lý mẫu với Flow Through Needle
Bộ ổn nhiệt cho cột với bộ tiền làm nóng linh hoạt
Khay chứa dung môi
Bộ kít hoạt động cho máy
Các sensors phát hiện rò rỉ
Detector
Phần mềm điều khiển, máy tính, máy in
Bộ phụ kiện cho chuẩn bị mẫu
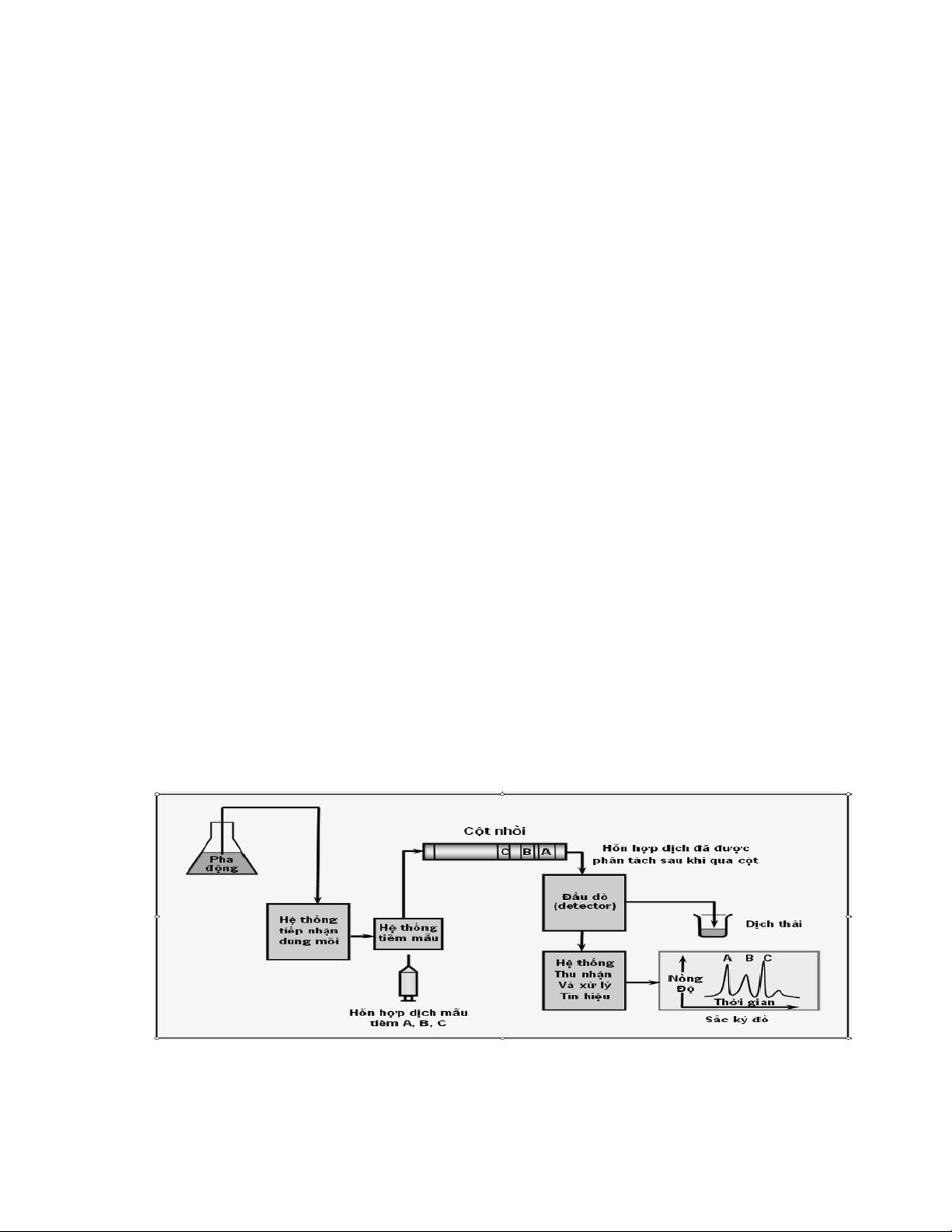
Hình: Sơ đồ hệ thống UPLC
o Máy li tâm thường và ly tâm tốc độ cao.
o Máy lắc.

o Tủ ấm.
o Máy rửa dụng cụ bằng sóng siêu âm.
o Bộ lọc dung môi.
o Cột sắc ký: cột phân tích có kích thước tiểu phần 1,7µm, đường kính cột
2,1mm, chiều dài cột 150mm.
o Giấy lọc với kích thước lọc 0,2 µm.
2.2. Hóa chất: tất cả các dung dịch và hóa chất sử dụng cho hệ thống đều phải là
chuẩn HPLC hoặc tốt hơn.
Acetonitrile đậm đặc.
Nƣớc cất
Methanol đậm đặc
Acid fomic đậm đặc
MasTrak AAA standards (bộ kít chuẩn): gồm có
Các amino acid tan trong acid.
Các amino acid tan trong base.
allo-Isoleucine
Glutamine
Norvaline
Tryptophan
MasTrak AAA eluent A: thành phần 8-10% acetonitrile, 4-6% formic acid,
84-88% ammonium acetate/water solution.
MasTrak AAA derivatization kit: bộ kít tạo dẫn xuất gồm có
Borate buffer: <5% sodium tetraborate and >95% water
Reagent powder (2A): 6-aminoquinolyl-N-hydroxy-succinimidyl
carbamate (AQC)
Reagent diluents (2B): acetonitrile
3.Ngƣời bệnh
Cần giải thích cho người bệnh và người nhà người bệnh hiểu về mục đích của
việc lấy máu làm xét nghiệm.
4. Phiếu xét nghiệm
- Phiếu xét nghiệm theo đúng quy định của Bộ Y tế và bệnh viện.
- Trên phiếu xét nghiệm cần ghi đầy đủ thông tin của người bệnh: họ và tên,
tuổi, giới tính, số giường, khoa phòng, chẩn đoán, xét nghiệm cần làm.
- Trên phiếu xét nghiệm cần có: chữ ký và họ tên bác sĩ chỉ định xét nghiệm, họ
tên người lấy mẫu, thời gian chỉ định xét nghiệm và thời gian lấy mẫu bệnh
phẩm.

III. CÁC BƢỚC TIẾN HÀNH
1. Lấy bệnh phẩm
Huyết tương, nước tiểu và dịch não tủy là mẫu bệnh phẩm sử dụng cho xét
nghiệm này.
- Thu thập, xử lý và bảo quản mẫu máu:Máu toàn phần tĩnh mạch được thu thập
vào ống chống đông bằng heparin với thể tích tối thiểu là 1 mL, tối đa là 2 mL. Sau
khi thu thập, mẫu được vận chuyển ngay tới phòng xét nghiệm. Tiến hành ly tâm
ngay sau khi nhận mẫu với tốc độ 3000 vòng/phút trong 5 phút, tách huyết tương và
bảo quản ở -20oC cho đến khi phân tích. Bệnh phẩm chỉ tan đông 1 lần và phải để
bệnh phẩm đạt nhiệt độ phòng trước khi phân tích. Trộn kỹ bệnh phẩm sau khi rã
đông.
- Thu thập, xử lý và bảo quản nước tiểu: Nước tiểu ngẫu nhiên được thu thập vào
các ống đựng bệnh phẩm sạch, không có chất bảo quản. Thể tích tối thiểu là 2 mL.
Vận chuyển ngay tới phòng xét nghiệm, ly tâm với tốc độ 3000 vòng/phút trong 5
phút, chắt dịch trong và bảo quản ở -20oC cho đến khi phân tích. Một phần nước tiểu
được sử dụng để định lượng
- Thu thập, xử lý và bảo quản dịch não tủy: Dịch não tủy được thu thập vào các
ống đựng bệnh phẩm sạch, không có chất bảo quản. Thể tích tối thiểu là 0,5 ml. Vận
chuyển ngay tới phòng xét nghiệm, ly tâm với tốc độ 3000 vòng/phút trong 5 phút,
chắt dịch trong và bảo quản ở -20oC cho đến khi phân tích.
- Mẫu huyết tương/ nước tiểu từ ngoài bệnh viện cần phải bảo quản đông lạnh.
2. Tiến hành kỹ thuật
- Máy phân tích cần chuẩn bị sẵn sàng để thực hiện phân tích mẫu: máy đã được
cài đặt chương trình xét nghiệm định lượng IgE đặc hiệu Alpha-lactalbumin
máu. Máy đã được chuẩn với xét nghiệm IgE đặc hiệu Alpha-lactalbumin. Kết
quả kiểm tra chất lượng với xét nghiệm IgE đặc hiệu Alpha-lactalbumin đạt yêu
cầu, không nằm ngoài dải cho phép và không vi phạm luật kiểm tra chất lượng.
- Người thực hiện phân tích mẫu nhập dữ liệu về thông tin người bệnh và chỉ
định xét nghiệm vào máy phân tích hoặc hệ thống mạng (nếu có)
- Thực hiện xét nghiệm theo protocol của máy.
IV. NHẬN ĐỊNH KẾT QUẢ
Khoảng tham chiếu
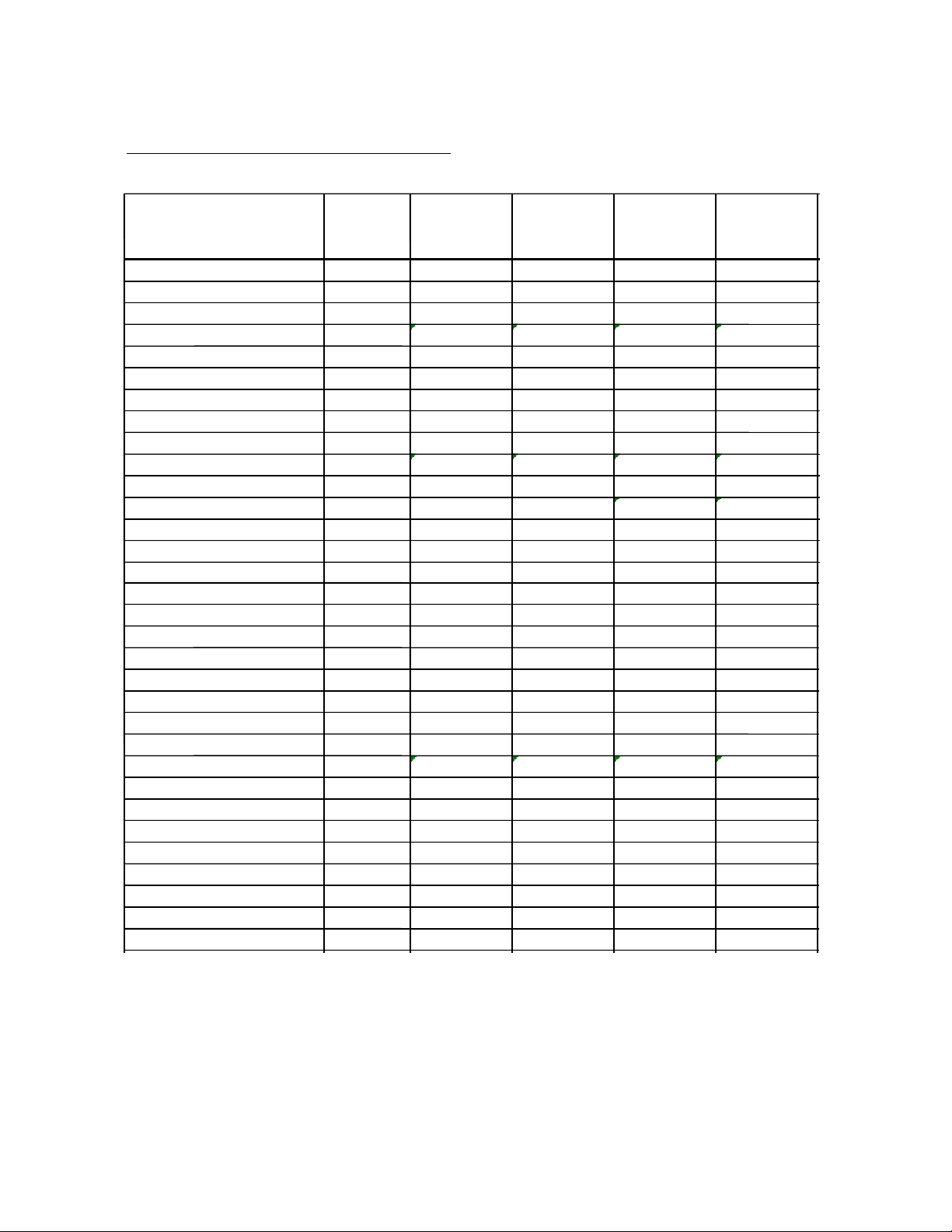
Bảng 1. Khoảng tham chiếu của acid amin huyết tương (đơn vị: umol/L):
Acid amin
Kết quả
thông báo
0-1 tháng
1-24 tháng
2-18 tuổi
>18 tuổi
Alanine
Có
131-710
143-439
152-547
177-583
Allo-isoleucine
Không
0-5
0-5
0-5
0-5
Alpha-aminoadipic acid
Không
0-1
0-1
0-1
0-6
Alpha-aminobutyric acid
Không
8-24
3-26
4-31
5-41
Arginine
Có
6-140
12-133
10-140
15-128
Argininosuccinic acid
Có
0-8
0-8
0-8
0-8
Asparagine
Có
29-132
21-95
23-112
35-74
Aspartic acid
Có
0-129
0-23
0-24
0-25
Beta-alanine
Không
0-10
0-7
0-7
0-12
Citrulline
Có
10-45
3-35
1-46
12-55
Cystathionine
Có
0-3
0-5
0-3
0-3
Cystine
Có
17-98
16-84
5-45
5-82
Ethanolamine
Không
0-115
0-4
0-7
0-153
Glutamic acid
Có
62-620
10-133
5-150
10-131
Glutamine
Có
376-709
246-1182
254-823
205-756
Glycine
Có
232-740
81-436
127-341
151-490
Histidine
Có
30-138
41-101
41-125
41-125
Homocitrulline
Không
0-15
0-8
0-8
0-8
Homocystine
Có
0-1
0-1
0-5
0-1
Hydroxylysine
Không
0-7
0-7
0-2
0-1
Isoleucine
Có
26-91
31-86
22-107
30-108
Leucine
Có
48-160
47-155
49-216
72-201
Lysine
Có
92-325
52-196
48-284
48-284
Methionine
Có
10-60
9-42
7-47
10-42
1-Methylhistidine
Không
0-43
0-44
0-42
0-42
Ornithine
Có
48-211
22-103
10-163
48-195
Phenylalanine
Có
38-137
31-75
26-91
35-85
Phosphoethanolamine
Không
0-27
0-6
0-69
0-40
Phosphoserine
Không
0-47
0-20
0-30
0-14
Serine
Có
99-395
71-186
69-187
58-181
Taurine
Không
46-492
15-143
10-170
54-210
Threonine
Có
90-329
24-174
35-226
60-225




















![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



