Bài 2
XÁC Đ NH PROTEIN THÔ CÓ TRONGỊ
TH C PH MỰ Ẩ
1. M c đíchụ
Xác đ nh hàm l ng protein t ng có trong th c ph mị ượ ổ ự ẩ
2. Nguyên t c, nguyên lýắ
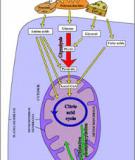
Vô c hóa m u th c ph m b ng Hơ ẫ ự ẩ ằ 2SO4 đ m đ c và ch t xúc tác. Dùng m tậ ặ ấ ộ
ki m m nh (NaOH ho c KOH) đ y NHề ạ ặ ẩ 3 t mu i (NHừ ố 4)2SO4 hình thành ra th t do.ể ự
Đ nh phân l ng Hị ượ 2SO4 d b ng dung d ch NaOH, t đó xác đ nh đ c l ngư ằ ị ừ ị ượ ượ
H2SO4 đã ph n ng và tính đ c hàm l ng nit t ng có trong m u.ả ứ ượ ượ ơ ổ ẫ
1. Vô c hoáơ
2. Quá trình ch ng c t:ư ấ
Sau đó l ng NHượ 3 đ c h i n c lôi cu n b ng máy ch ng c t đ m và đ cượ ơ ướ ố ằ ư ấ ạ ượ
d n đ n m t bình tam giác có ch a m t l ng th i Hẫ ế ộ ứ ộ ượ ờ 2SO4.T đây cho phép chúng ta xácừ
đ nh đ c l ng NHị ượ ượ 3 phóng thích ra, có nghĩa là xác đ nh đ c l ng đ m có trongị ượ ượ ạ
m u nguyên li uẫ ệ
3. Ch t xúc tácấ
4. Quá trình chu n đ :ẩ ộ
3. Hoá ch tấ
1. M u th c ph mẫ ự ẩ
2. Dung d ch ị

3. M u vô c hoáẫ ơ
4. Ch th MR 1%ỉ ị
5. Ch th Phenolphtalein 1%ỉ ị
6. Dung d ch NaOH 30%ị
7. N c c tướ ấ
8. Gi y pHấ
4. D ng cụ ụ
1. 1 b MicroKejedaltộ
2. 1 pipet 10ml
3. 3 erlen 250 ml
4. 1erlen 100ml
5. 1 bình đ nh m c 100 mlị ứ
6. 1 Becher 250 ml
7. 1 bóp cao su
8. 1 ph u thu tinh nhễ ỷ ỏ
5. Cách ti n hànhế
1. Chu n b hóa ch tẩ ị ấ
1. H n h p xúc tác CuSOỗ ợ 4 : K2SO4 theo t l 1:1ỷ ệ
2. Ch th MR 1%ỉ ị

2. Vô c hóa m uơ ẫ

3. Ch ng c t:ư ấ

6. K t qu thí nghi mế ả ệ
Hàm l ng nit toàn ph n tính b ng công th c:ượ ơ ầ ằ ứ
Trong đó:
•T: s ml NaOH dùng đ chu n đ m u tr ng.ố ể ẩ ộ ẫ ắ
•B: s ml NaOH dùng đ chu n đ m u th .ố ể ẩ ộ ẫ ử
•N: n ng đ đ ng l ng c a dd NaOH dùng chu n đ .ồ ộ ươ ượ ủ ẩ ộ
•m: kh i l ng m u vô c hóa (mg)ố ượ ẫ ơ
S ml NaOH s d ngố ử ụ
M u tr ngẫ ắ 23.4
L n 1ầ15,5
L n 2ầ15
Vây:
S ml NaOH trung bình dùng đ chu n đ m u th :ố ể ẩ ộ ẫ ử
Hàm l ng protein thô (%) = (nit toàn ph n)kượ ơ ầ
V i k là h s qui đ i t %N sang protein.ớ ệ ố ổ ừ
Hàm l ng protein thô (%) = 0,5708 = 3,5674%ượ
7. Tr l i câu h iả ờ ỏ
Câu 1: Vô c hoá m u là gì ? Vi t ph ng trình ph n ng x y ra trong quá trìnhơ ẫ ế ươ ả ứ ả
vô c hoá m uơ ẫ
Vô c hoá m u là đ a các h p ch t h u c trong m u v d ng các h p ch t vôơ ẫ ư ợ ấ ữ ơ ẫ ề ạ ợ ấ
cơ
Các ph n ng trong quá trình vô c hoá m uả ứ ơ ẫ
Câu 2: Vi t ph ng trình ph n ng x y ra trong quá trình ch ng c t và chu n đế ươ ả ứ ả ư ấ ẩ ộ
m uẫ
Các ph n ng trong quá trình ch ng c tả ứ ư ấ
Các ph n ng trong quá trình chu n đả ứ ẩ ộ
Câu 3





![Câu hỏi ôn tập hóa sinh thực phẩm [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2018/20181019/ayunn123/135x160/2711539952639.jpg)
![Ôn tập thực hành môn Thực vật [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2015/20151028/ngochunghcm/135x160/1692190693.jpg)

![Định lượng Vitamin C: Bài 8 [Hướng Dẫn Chi Tiết]](https://cdn.tailieu.vn/images/document/thumbnail/2014/20140222/minhtriet16/135x160/7291393079428.jpg)




![Bài giảng Giáp xác chân mái chèo [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250927/lethihongthuy2402@gmail.com/135x160/92891759114976.jpg)



![Tài liệu học tập Chuyên đề tế bào [mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250906/huutuan0/135x160/56151757299182.jpg)






