1
CÔ SÔÛ QUAÙ TRÌNH XÖÛ LYÙ HOÙA LYÙ
Qua
Quaùùtr
trì
ình
nh keo
keo tu
tuïï
ta
taïïo
oboâng
boâng
Qua
Quaùùtr
trì
ình
nh ha
haááp
p
phu
phuïï
Qua
Quaùùtr
trì
ình
nh
truye
truyeààn
nkh
khí
í
Qua
Quaùùtr
trì
ình
nh trao
trao
ñ
ño
oååi
iion
ion
Cơsởquá trình hấpphụ(Adsorption)
Định nghĩa
Là 1 hiệntượng bềmặt
Thu hút chấtbịhấpphụlên bềmặtchấthấpphụ,
làm giảmsứccăng bềmặtcủachấthấpphụ
Nhảhấpphụ: qt điracủachấtbịhấpphụkhỏi
bềmặtchấthấpphụ
2
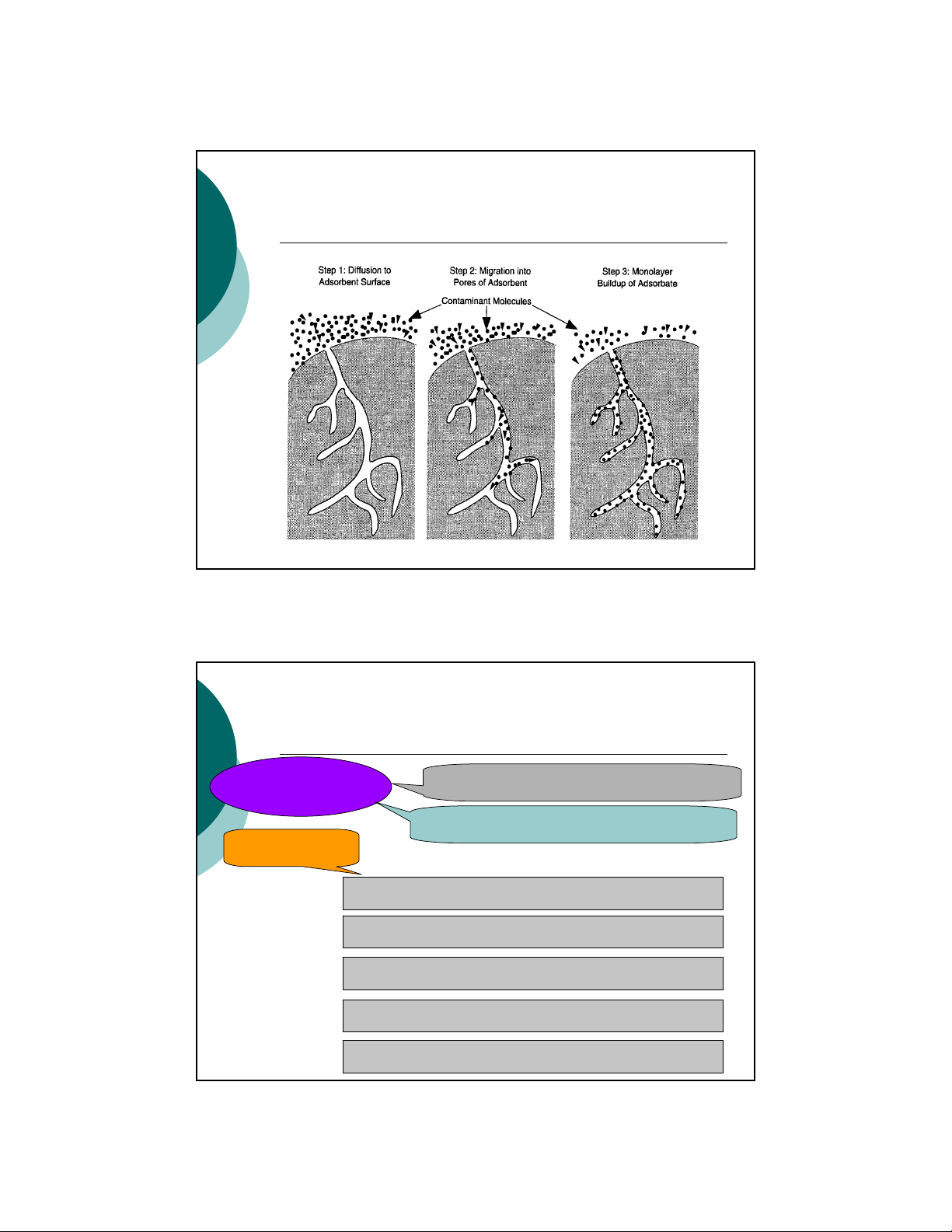
Cơchếquá trình hấpphụ
Cơsởquá trình hấpphụ
Phaân loaïi
HP
HP Ho
Hoùùa
aho
hoïïc
c(Chemical Adsorption)
(Chemical Adsorption)
HP
HP Va
Vaäät
tly
lyùù(Physical Adsorption)
(Physical Adsorption)
Nhô
Nhôøøca
caùùc
cl
löï
öïc
clieân
lieân ke
keáát
tva
vaäät
tly
lyùù
Ha
Haááp
pphu
phu đơn
đơnl
lớ
ớp
p,
, ñ
ña
alô
lôùùp
p,
, thua
thuaään
nnghòch
nghòch
HP
HP Va
Vaäät
tly
lyùù
Ca
Caááu
utru
truùùc
ccha
chaáát
tha
haááp
pphu
phuïïkhoâng
khoâng thay
thay ñ
ño
oååi
i
Í
Ít
tco
coùùt
tí
ính
nh cho
choïïn
nlo
loïïc
c, t
, t0
0tha
thaááp
p
VD:
VD: s
sự
ựHP
HP c
củ
ủa
aAC
AC đ
đ/v
/v CO
CO2
2, C
, C2
2H
H5
5OH,
OH,…
…
3
Cơsởquá trình hấpphụ
HP
HP ho
hoùùa
aho
hoïïc
c
Nhô
Nhôøøl
löï
öïc
clieân
lieân ke
keáát
tho
hoùùa
aho
hoïïc
c
Ha
Haááp
pphu
phuïïñ
ñôn
ôn lô
lôùùp
p
Ca
Caááu
utru
truùùc
ccha
chaáát
tha
haááp
pphu
phuïïthay
thay ñ
ño
oååi
i
Khoâng
Khoâng thua
thuaään
nnghòch
nghòch
T
Tí
ính
nh cho
choïïn
nlo
loïïc
ccao
cao, t
, t0
0cao
cao
VD:
VD: s
sự
ựHP
HP c
củ
ủa
ach
chấ
ất
tr
rắ
ắng
ng AgI
AgI đ
đ/v
/v Ag
Ag+
+trong
trong dd
dd
Cơsởquá trình hấpphụ
Kha
Khaûûnaêng
naêng ha
haááp
pphu
phuïïphu
phuïïthuo
thuoääc
c
Die
Dieään
nt
tí
ích
ch be
beààma
maëët
tcha
chaáát
tha
haááp
pphu
phuïï(m
(m2
2/g)
/g)
No
Noààng
ng ñ
ño
oääcu
cuûûa
acha
chaáát
tbò
bò ha
haááp
pphu
phuïï
Va
Vaään
nto
toáác
ct
tö
öông
ông ñ
ño
oáái
igi
giö
öõa
õa hai
hai pha
pha
Cô
Cô che
cheááh
hì
ình
nh tha
thaøønh
nh lieân
lieân ke
keáát
t:
: ho
hoùùa
ahay
hay ly
lyùùho
hoïïc
c
4
Cơsởquá trình hấpphụ
Ca
Caùùc
cda
daïïng
ng lieân
lieân ke
keáát
t
LK Van
LK Van der
der Waals
Waals
LK
LK t
tó
ónh
nh ñ
ñie
ieään
n
LK Hydro
LK Hydro
LK
LK ho
hoùùa
aho
hoïïc
c:
: lk
lk ion,
ion, ñ
ño
oààng
ng ho
hoùùa
atrò
trò,
, pho
phoáái
itr
trí
í
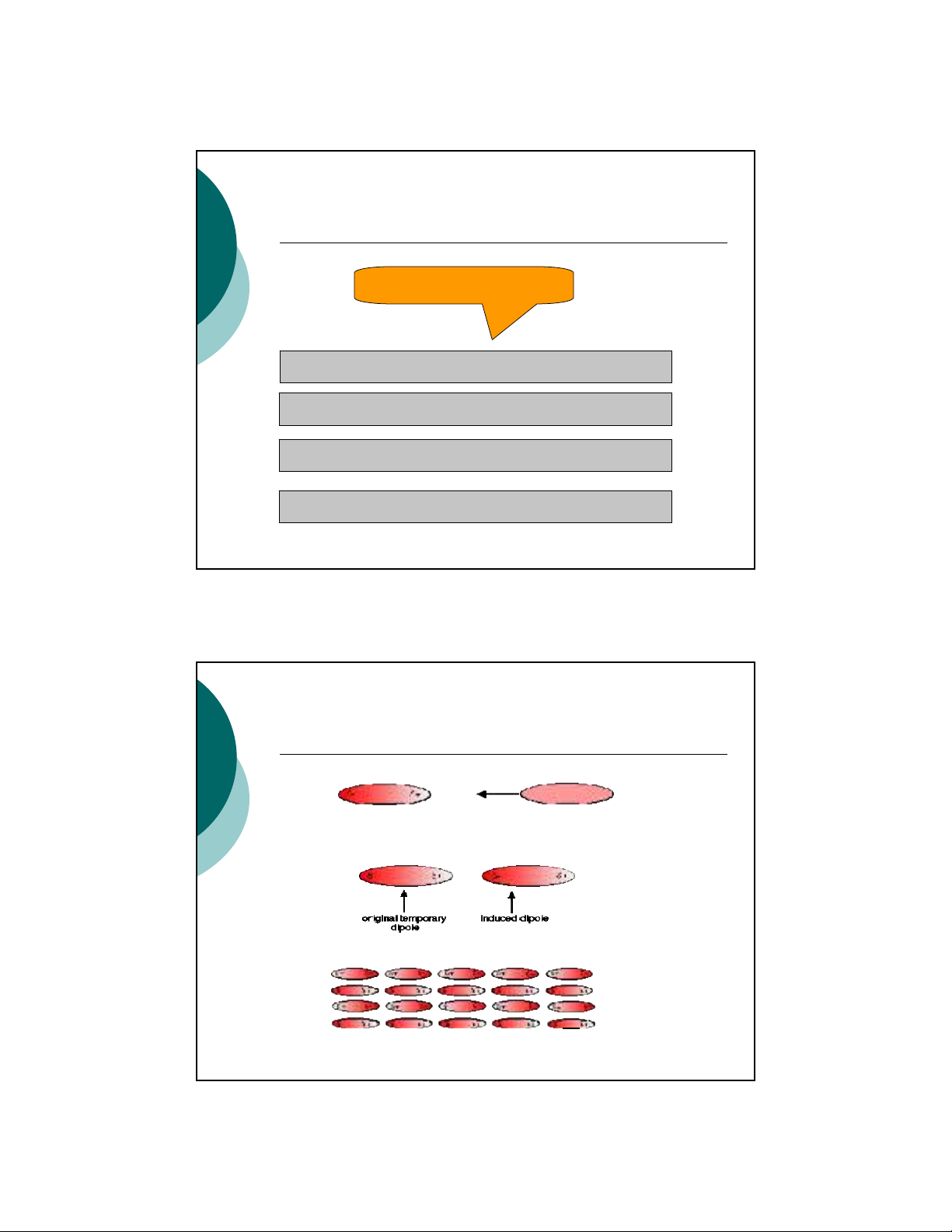
Liên kết Van der Waals
5
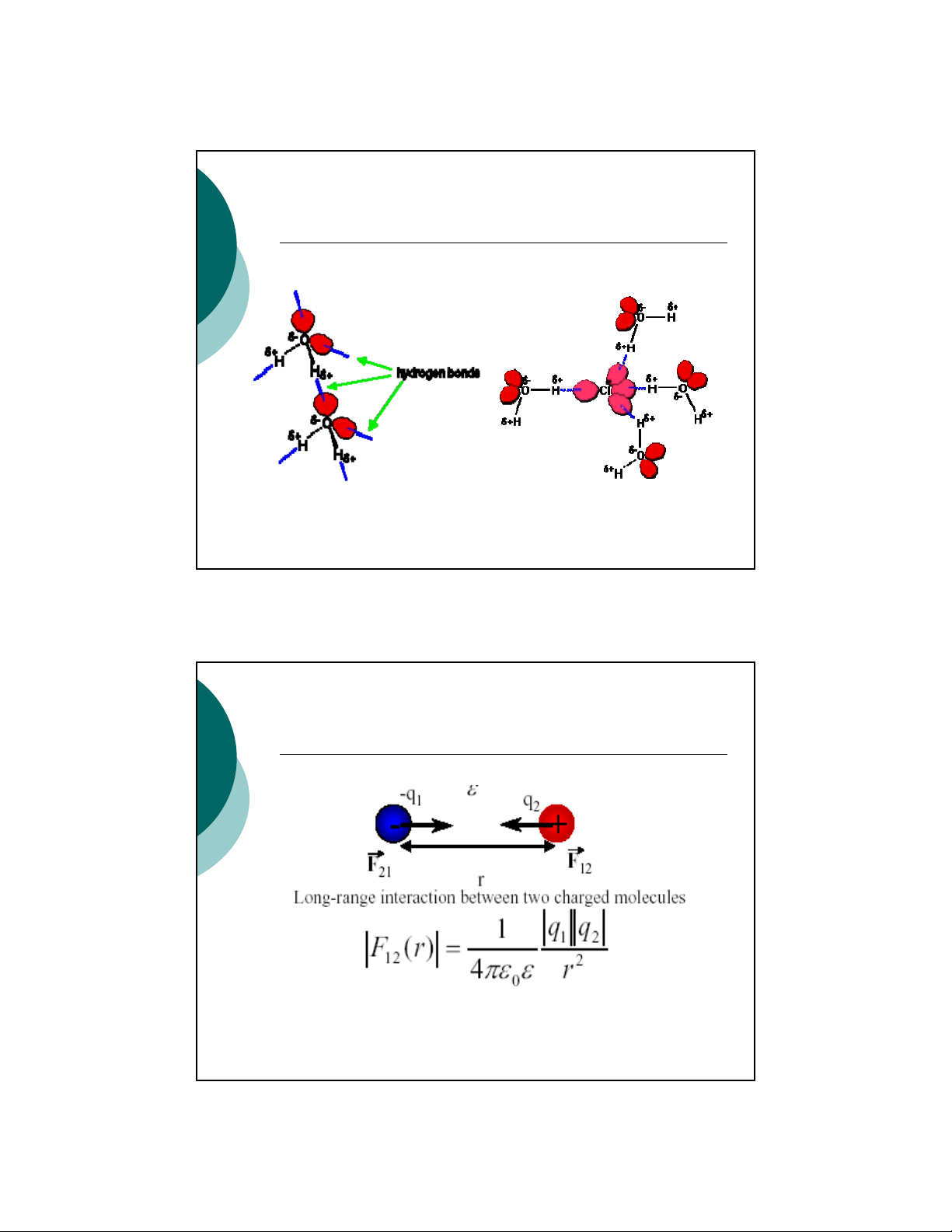
Liên kếtHydro
Liên kếttĩnh điện

![Câu hỏi ôn tập Hóa lý [chuẩn nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2025/20250709/kimphuong1001/135x160/51111752043440.jpg)

![Hệ Thống Bài Tập Phần I: [Thêm từ mô tả để tăng CTR]](https://cdn.tailieu.vn/images/document/thumbnail/2013/20131021/patrica1903/135x160/4851382347277.jpg)






![Dung Dịch: [Thêm từ khóa hoặc mô tả liên quan để tối ưu SEO]](https://cdn.tailieu.vn/images/document/thumbnail/2011/20110914/thiuyen12/135x160/pages_from_hoaly_tap2_tranvannhan_568.jpg)









![Đề thi trắc nghiệm giữa kì môn Hóa đại cương 2: [Kèm đáp án/ Tổng hợp đề thi/ Mới nhất]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260514/quangbinhmc2006@gmail.com/135x160/56141778723328.jpg)

![Tài liệu Hóa học đại cương Trường Đại học Công nghệ Giao thông Vận tải [PDF]](https://cdn.tailieu.vn/images/document/thumbnail/2026/20260511/vispacex_27/135x160/7711778501472.jpg)



